1 . 下列物质的微粒中:
A.NaCl B.NH4Cl C.MgCl2 D.干冰 E.Na2O2 F.CH4 G.H2O2 H.N2 I.Na2CO3 J.Ne
(1)只有非极性键的是___________ (填序号下同)。
(2)只有离子键的是___________ 。
(3)既有极性键又有非极性键的是___________ 。
(4)既有离子键又有非极性键的是___________ 。
(5)无任何化学键的是___________ 。
A.NaCl B.NH4Cl C.MgCl2 D.干冰 E.Na2O2 F.CH4 G.H2O2 H.N2 I.Na2CO3 J.Ne
(1)只有非极性键的是
(2)只有离子键的是
(3)既有极性键又有非极性键的是
(4)既有离子键又有非极性键的是
(5)无任何化学键的是
您最近一年使用:0次
2 . 下列物质既含离子键又含共价键的是
| A.HCl | B.Na2O2 | C.CaCl2 | D.Na2O |
您最近一年使用:0次
名校
3 . 下列有关化学用语使用正确的是
| A.过氧化钠是含有共价键的离子化合物 | B.中子数为20的钙原子: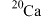 |
C.氯离子的结构示意图为: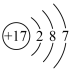 | D. 的电子式为 的电子式为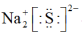 |
您最近一年使用:0次
解题方法
4 .  (离子化合物)是汽车尾气净化催化剂的关键成分,其在
(离子化合物)是汽车尾气净化催化剂的关键成分,其在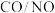 的氧化还原反应中发挥了巨大作用,该氧化还原反应的反应机理如图所示。下列说法正确的是
的氧化还原反应中发挥了巨大作用,该氧化还原反应的反应机理如图所示。下列说法正确的是
 (离子化合物)是汽车尾气净化催化剂的关键成分,其在
(离子化合物)是汽车尾气净化催化剂的关键成分,其在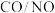 的氧化还原反应中发挥了巨大作用,该氧化还原反应的反应机理如图所示。下列说法正确的是
的氧化还原反应中发挥了巨大作用,该氧化还原反应的反应机理如图所示。下列说法正确的是
| A.转化过程中Ce元素的化合价未发生变化 |
| B.尾气中的CO浓度对NO的消除效果没有影响 |
| C.图中过程2涉及非极性共价键的断裂和形成 |
D.该过程的总反应方程式为 |
您最近一年使用:0次
名校
解题方法
5 . 下列物质的性质不能用化学键解释的是
A.沸点: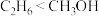 | B.稳定性: |
| C.硬度:金刚石>晶体硅 | D.熔点:氧化镁>氯化钠 |
您最近一年使用:0次
2024-07-25更新
|
52次组卷
|
3卷引用:北京市顺义区第一中学2025届高三上学期8月月考化学试题
解题方法
6 . 甲醛是家庭装修常见的污染物。一种催化氧化甲醛的反应: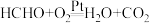 。下列有关叙述正确的是
。下列有关叙述正确的是
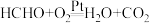 。下列有关叙述正确的是
。下列有关叙述正确的是| A.HCHO分子中σ键和π键的数目之比为3:1 |
| B.HCHO分子中存在分子间氢键 |
C. 是由极性键构成的非极性分子 是由极性键构成的非极性分子 |
D. 中碳原子的杂化方式为 中碳原子的杂化方式为 |
您最近一年使用:0次
解题方法
7 . 下列各组物质中,均是仅由极性键构成的极性分子的是
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
您最近一年使用:0次
名校
解题方法
8 . 水丰富而独特的性质与其结构密切相关。
(1)对于水分子中的共价键,依据原子轨道重叠的方式判断,属于___________ 键;依据O与 的电负性判断,属于
的电负性判断,属于___________ 共价键。
(2)水分子中,氧原子的价层电子对数为___________ ,杂化轨道类型为___________ 。
(3)下列事实可用“水分子间存在氢键”解释的是___________ (填字母序号)。
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(4)酸溶于水可形成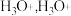 的电子式为
的电子式为___________ ;由于成键电子对和孤电子对之间的斥力不同,会对微粒的空间结构产生影响,如 中
中 的键角大于
的键角大于 中
中 的键角,据此判断
的键角,据此判断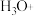 和
和 的键角大小:H3O+
的键角大小:H3O+______ H2O(填“>”或“<”)。
(1)对于水分子中的共价键,依据原子轨道重叠的方式判断,属于
 的电负性判断,属于
的电负性判断,属于(2)水分子中,氧原子的价层电子对数为
(3)下列事实可用“水分子间存在氢键”解释的是
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(4)酸溶于水可形成
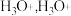 的电子式为
的电子式为 中
中 的键角大于
的键角大于 中
中 的键角,据此判断
的键角,据此判断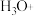 和
和 的键角大小:H3O+
的键角大小:H3O+
您最近一年使用:0次
9 . 一种以乙烯为原料制备乙二醇的合成方法如图:
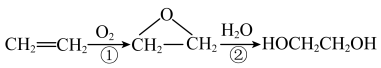
| A.反应①有非极性键的断裂和形成 |
B.反应①②的原子利用率均为 |
| C.上述3种有机物均能发生氧化反应 |
D. 最多能与 最多能与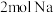 发生反应 发生反应 |
您最近一年使用:0次
名校
解题方法
10 . W可与 形成化合物Q,Q的结构如图所示,下列说法错误的是
形成化合物Q,Q的结构如图所示,下列说法错误的是
 形成化合物Q,Q的结构如图所示,下列说法错误的是
形成化合物Q,Q的结构如图所示,下列说法错误的是
| A.C、N、O均能与H形成既含极性键又含非极性键的分子 |
B.W与 结合前后,N原子的杂化方式发生了变化 结合前后,N原子的杂化方式发生了变化 |
| C.与Cu原子未成对电子数相同的同周期元素有4种 |
| D.Q中的作用力有配位键、共价键、氢键 |
您最近一年使用:0次
2024-07-14更新
|
111次组卷
|
2卷引用:湖北省荆州市沙市中学2023-2024学年(新)高三上学期7月月考化学试题



