23-24高二下·全国·课前预习
1 . 共价键的形成
(1)概念:原子间通过___________ 所形成的相互作用,叫做共价键。
(2)成键的粒子:一般为___________ 原子(相同或不相同)或金属原子与非金属原子。
(3)本质:原子间通过___________ (即原子轨道重叠)产生的强烈作用。
(1)概念:原子间通过
(2)成键的粒子:一般为
(3)本质:原子间通过
您最近一年使用:0次
2 . 化学与人类生产、生活密切相关,利用所学知识进行填空(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)下列物质能导电且属于电解质的是___________(填字母)。
(2)NaH可在野外作生氢剂,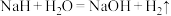 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为___________ 。
(3)标准状况下,44.8L 对应的物质的量是
对应的物质的量是___________ ,其含有的共价键类型为___________ 键。(填极性或者非极性)
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是___________ (填化学式)
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为_______ 。
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(1)下列物质能导电且属于电解质的是___________(填字母)。
| A.氯化钠固体 | B.熔融的氯化钠 | C.氯化钠溶液 | D.钠 |
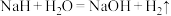 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)标准状况下,44.8L
 对应的物质的量是
对应的物质的量是(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
您最近一年使用:0次
名校
3 . 按要求完成下列填空。
I.下列物质:① ②
② ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
(1)含有共价键的离子化合物是___________ (填序号,下同)。
(2)属于共价化合物是___________ 。
(3)只含有非极性键的物质是___________ 。
(4)写出①的结构式___________ ,写出⑥的电子式___________ 。
II.下列变化:①蔗糖溶于水② 升华③烧碱熔化④NaCl溶解⑤
升华③烧碱熔化④NaCl溶解⑤ 溶解⑥硫酸氢钾溶于水
溶解⑥硫酸氢钾溶于水
(5)只有离子键被破坏的是___________ 。
(6)只有共价键被破坏的是___________ 。
(7)只破坏分子间作用力的是___________ 。
I.下列物质:①
 ②
② ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
(1)含有共价键的离子化合物是
(2)属于共价化合物是
(3)只含有非极性键的物质是
(4)写出①的结构式
II.下列变化:①蔗糖溶于水②
 升华③烧碱熔化④NaCl溶解⑤
升华③烧碱熔化④NaCl溶解⑤ 溶解⑥硫酸氢钾溶于水
溶解⑥硫酸氢钾溶于水(5)只有离子键被破坏的是
(6)只有共价键被破坏的是
(7)只破坏分子间作用力的是
您最近一年使用:0次
2024-02-07更新
|
279次组卷
|
2卷引用:甘肃省兰州第一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
4 . 完成下列问题
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
(3)关于新制饱和氯水,下列叙述正确的是_______
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2O
ii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是___________
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)_________
③配平反应i的化学方程式_________ 。
④标出反应ii中电子转移的方向和数目_________ 。
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾___________ 吨。
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
| A.钝化 | B.漂白 | C.固氮 | D.燃烧 |
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
| A.工业合成氨的过程是固氮的过程 |
| B.自然界中,氨是动物体特别是蛋白质腐败后的产物 |
| C.为防止粮食、罐头、水果等食品腐烂,常用氮气作保护气 |
| D.在雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
(3)关于新制饱和氯水,下列叙述正确的是_______
| A.加入适量NaOH,溶液黄绿色褪去,说明氯水中含有Cl2分子 |
| B.加入少量NaCl粉末,溶液漂白性增强 |
| C.加入少量的碳酸钠粉末,pH增大,溶液漂白性一定减弱 |
| D.光照过程中,有气泡冒出,溶液的导电性减弱 |
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
| A.向含足量NaOH的Na2S溶液中加入Na2SO3 |
| B.常温下,向试管中加入1mL浓硫酸和一小块铜片 |
| C.将0.5g硫粉和1.0g铁粉均匀混合,在石棉网上用红热玻璃棒触及粉末一端至粉末红热 |
| D.向Na2SO3固体中加入70%的浓硫酸制备SO2 |
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

| A.O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
| C.发生步骤②时,断裂的化学键既有极性键又有非极性键 |
| D.步骤③中,每生成1molBr2转移2mol电子 |
(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3
 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2Oii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)
③配平反应i的化学方程式
④标出反应ii中电子转移的方向和数目
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾
您最近一年使用:0次
解题方法
5 . 阅读下面一段材料,根据所学知识,回答下列问题:
将用砂纸打磨过的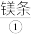 在空气中燃烧,生成
在空气中燃烧,生成 和
和 ,氮化镁溶于水得到
,氮化镁溶于水得到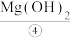 固体和
固体和 ,将Mg(OH)2固体溶于
,将Mg(OH)2固体溶于 ,得到无色溶液,将无色溶液经过一系列操作得到
,得到无色溶液,将无色溶液经过一系列操作得到 ,将
,将 在
在 气流中加热得到
气流中加热得到 。
。
(1)镁在元素周期表中的位置是___________ ,MgCl2中含有的化学键类型为___________ 。
(2)常温下,上述有标号的物质中,能导电的是___________ (填标号,下同),属于电解质的有___________ 。
(3)写出氮化镁固体溶于水发生反应的化学方程式:___________ 。
(4)实验1:将一块金属钠投入MgCl2溶液中,写出发生反应的离子方程式:___________ 。
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量 的稀硫酸中,相同时间内,观察到的现象为
的稀硫酸中,相同时间内,观察到的现象为___________ ,可得出的结论是___________ 。
将用砂纸打磨过的
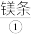 在空气中燃烧,生成
在空气中燃烧,生成 和
和 ,氮化镁溶于水得到
,氮化镁溶于水得到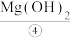 固体和
固体和 ,将Mg(OH)2固体溶于
,将Mg(OH)2固体溶于 ,得到无色溶液,将无色溶液经过一系列操作得到
,得到无色溶液,将无色溶液经过一系列操作得到 ,将
,将 在
在 气流中加热得到
气流中加热得到 。
。(1)镁在元素周期表中的位置是
(2)常温下,上述有标号的物质中,能导电的是
(3)写出氮化镁固体溶于水发生反应的化学方程式:
(4)实验1:将一块金属钠投入MgCl2溶液中,写出发生反应的离子方程式:
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量
 的稀硫酸中,相同时间内,观察到的现象为
的稀硫酸中,相同时间内,观察到的现象为
您最近一年使用:0次
6 . 实验室有如下物质:①熔融的氢氧化钠② 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体
(1)上述状态下可导电的是______ ;
(2)属于电解质的是______ ;
(3)属于非电解质的是______ ;
(4)上述状态下的电解质不能导电的是______ 。
 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)上述状态下的电解质不能导电的是
您最近一年使用:0次
名校
7 . 有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥氩气,回答下列问题(填序号):
⑥氩气,回答下列问题(填序号):
(1)不存在化学键的是___________
(2)只存在非极性键的是___________
(3)只存在离子键的是___________
(4)既存在离子键又存在极性键的是___________
(5)既存在离子键又存在非极性键的是___________
 ②
② ③
③ ④
④ ⑤
⑤ ⑥氩气,回答下列问题(填序号):
⑥氩气,回答下列问题(填序号):(1)不存在化学键的是
(2)只存在非极性键的是
(3)只存在离子键的是
(4)既存在离子键又存在极性键的是
(5)既存在离子键又存在非极性键的是
您最近一年使用:0次
名校
8 . 一定条件下,氨与氟气发生反应: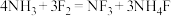 。其中
。其中 空间结构与
空间结构与 相似。
相似。
(1)写出反应物生成物中共价化合物的化学式___________ 。
(2)反应物、生成物中各原子均满足8电子稳定结构的是___________ 。
(3)书写 的电子式
的电子式___________ 。
(4) 所含的化学键为
所含的化学键为___________ 。
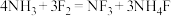 。其中
。其中 空间结构与
空间结构与 相似。
相似。(1)写出反应物生成物中共价化合物的化学式
(2)反应物、生成物中各原子均满足8电子稳定结构的是
(3)书写
 的电子式
的电子式(4)
 所含的化学键为
所含的化学键为
您最近一年使用:0次
名校
9 . 做导电性实验时发现熔化的氯化铝不导电,推测氯化铝是___________ (填“离子”或“共价”)化合物。
您最近一年使用:0次
名校
10 . 如图是氟元素在元素周期表中的信息及原子结构示意图,回答下列问题:
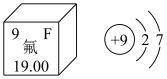
(1)图中“19.00”代表___________ ,请写出氟原子最外层的轨道表示式:___________ 。其最外层有___________ 种运动状态不同的电子,能量最高的能级的原子轨道的形状___________ 。
(2)氟气非常活泼,易与金属和某些非金属反应生成不同的化合物,如 、
、 ,请写出
,请写出 的电子式
的电子式___________ , 中的化学键类型为
中的化学键类型为___________ ; 是
是___________ 化合物, 是10电子微粒,请再写出两个10电子微粒
是10电子微粒,请再写出两个10电子微粒___________ 。

(1)图中“19.00”代表
(2)氟气非常活泼,易与金属和某些非金属反应生成不同的化合物,如
 、
、 ,请写出
,请写出 的电子式
的电子式 中的化学键类型为
中的化学键类型为 是
是 是10电子微粒,请再写出两个10电子微粒
是10电子微粒,请再写出两个10电子微粒
您最近一年使用:0次



