解题方法
1 . 构成微粒
离子晶体由_____ 构成。
离子晶体由
您最近一年使用:0次
解题方法
2 . 离子键的特征
离子键没有_____ 性和_____ 性。
阴、阳离子在各个方向上都可以与带相反电荷的离子发生静电作用,即没有_____ 性;在静电作用能够达到的范围内,只要空间条件允许,一个离子可以同时吸引多个带相反电荷的离子,即没有_____ 性。
离子键没有
阴、阳离子在各个方向上都可以与带相反电荷的离子发生静电作用,即没有
您最近一年使用:0次
解题方法
3 . 离子键的概念
阴、阳离子之间通过_____ 而形成的化学键叫离子键。
阴、阳离子之间通过
您最近一年使用:0次
4 . 铬元素是哺乳类代谢过程中必须的微量元素,目前六氟代乙酰丙酮铬(Ⅲ)螯合物(其结构如图)的检出极限已达到 。回答下列问题:
。回答下列问题:___________ ,H、C、O、F的电负性由大到小的顺序为___________ 。
(2)与 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有___________ 种,其中原子序数最大的元素在周期表中的位置是___________ 。
(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有___________ 。
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(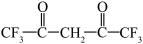 )中
)中 键有
键有___________ 个。
(5)分子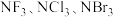 中键角由小到大的顺序是
中键角由小到大的顺序是___________ ,其原因是___________ 。
 。回答下列问题:
。回答下列问题: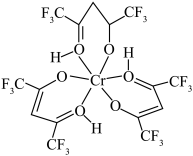
(2)与
 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(
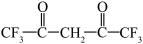 )中
)中 键有
键有(5)分子
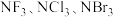 中键角由小到大的顺序是
中键角由小到大的顺序是
您最近一年使用:0次
名校
解题方法
5 . 能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是_______ (填“离子键”或“共价键”)。
(2)下列化学反应在理论上可以设计成原电池的是_______(填字母)。
(3)如图为某燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为_______ (填物质名称),电解质溶液中的OH-移向_______ (“负”或“正”)。
②写出此氢氧燃料电池工作时总反应方程式:_______ 。
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是
(2)下列化学反应在理论上可以设计成原电池的是_______(填字母)。
A.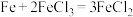 | B. |
C. | D.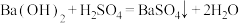 |

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
②写出此氢氧燃料电池工作时总反应方程式:
您最近一年使用:0次
6 . 非金属元素在生产生活中扮演着重要角色。请根据题意填空:
(1)为了达到更好的消毒效果,我国已开始使用新的自来水消毒剂,如臭氧、___________ (填“ ”或“HCl”)等。
”或“HCl”)等。
(2)硝酸是一种重要的化工原料,在浓硝酸的运输过程中,可选择___________ (填“铁”或“铜”)作为罐体材料。
(3)碳化硅(SiC)具有类似金刚石的结构,可用作砂纸和砂轮的磨料,其中碳原子和硅原子之间的相互作用为___________ (填“离子键”或“共价键”)。
(1)为了达到更好的消毒效果,我国已开始使用新的自来水消毒剂,如臭氧、
 ”或“HCl”)等。
”或“HCl”)等。(2)硝酸是一种重要的化工原料,在浓硝酸的运输过程中,可选择
(3)碳化硅(SiC)具有类似金刚石的结构,可用作砂纸和砂轮的磨料,其中碳原子和硅原子之间的相互作用为
您最近一年使用:0次
2023-06-28更新
|
156次组卷
|
2卷引用:2023年湖南省普通高中学业水平考试化学试题
名校
7 . 人类对原子结构的探索为科技发展带来了卓越贡献,门捷列夫发现的元素周期律也为研究物质性质,合成新的物质做出了重要的指导作用。
(1)工业焊接钢管时常用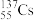 进行“无损探伤”,该原子___________
进行“无损探伤”,该原子___________
(2)下列变化中破坏共价键的是___________
(1)工业焊接钢管时常用
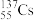 进行“无损探伤”,该原子___________
进行“无损探伤”,该原子___________| A.质子数是82 | B.中子数是55 | C.与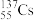 互为同位素 互为同位素 | D.摩尔质量是137 |
| A.冰融化 | B.NaOH融化 | C.HCl溶于水 | D.干冰升华 |
您最近一年使用:0次
解题方法
8 . I.有下列物质:①Na2O ②NaOH ③NH4Cl ④CO2 ⑤H2S ⑥Ar
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是___________ ,属于共价化合物的是___________ 。
(2)只含有离子键的是___________ ,既含有离子键又含有共价键的是___________ 。
(3)不存在化学键的是______________ 。
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于_ 晶体,KBr可能属于__ 晶体。
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于__ 晶体,写出BaCl2的电子式:____ 。
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是____ 晶体,而SiC可能是____ 晶体。
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;_____ 。
(8)______MnO +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;_____
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是
(2)只含有离子键的是
(3)不存在化学键的是
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;
(8)______MnO
 +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
您最近一年使用:0次
解题方法
9 . 能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是___________ (填“离子键”或“共价键”)。
(2)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。若断开1mol氢气中的化学键消耗的能量为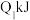 ,断开1mol氧气中的化学键消耗的能量为
,断开1mol氧气中的化学键消耗的能量为 ,形成1mol水中的化学键释放的能量为
,形成1mol水中的化学键释放的能量为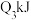 ,则下列关系正确的是___________(填字母)。
,则下列关系正确的是___________(填字母)。
(3)下列化学反应在理论上可以设计成原电池的是___________(填字母)。
(4)如图为某燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为___________ (填物质名称),电解质溶液中的OH-移向___________ (“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:___________ 。
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是
(2)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。若断开1mol氢气中的化学键消耗的能量为
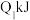 ,断开1mol氧气中的化学键消耗的能量为
,断开1mol氧气中的化学键消耗的能量为 ,形成1mol水中的化学键释放的能量为
,形成1mol水中的化学键释放的能量为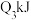 ,则下列关系正确的是___________(填字母)。
,则下列关系正确的是___________(填字母)。A.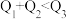 | B.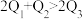 | C.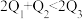 | D.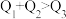 |
A.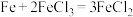 | B. |
C. | D.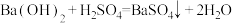 |

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
②写出此氢氧燃料电池工作时,负极的电极反应式:
您最近一年使用:0次
名校
10 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)从元素原子得失电子的角度看,元素⑤具有___________ (填“氧化性”或“还原性”)。
(2)元素②形成的单质气体含有___________ (填“极性”或“非极性”)共价键。
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为___________ 。
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),最高价氧化物对应的水化物具有两性的物质是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是___________ (填离子符号)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)从元素原子得失电子的角度看,元素⑤具有
(2)元素②形成的单质气体含有
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是
您最近一年使用:0次



