1 . W、X、Y、Z均为短周期元素,它们可以形成离子化合物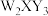 ,W和Y两种元素可以生成
,W和Y两种元素可以生成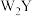 和
和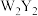 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
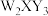 ,W和Y两种元素可以生成
,W和Y两种元素可以生成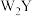 和
和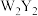 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是A.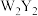 与Z的最高价氧化物反应,生成的产物中存在极性键、非极性键和离子键 与Z的最高价氧化物反应,生成的产物中存在极性键、非极性键和离子键 |
| B.同周期元素中,X的最高价氧化物的水化物酸性最强 |
| C.简单氢化物的稳定性Y大于Z |
D.W、X、Y的原子半径由大到小的顺序是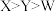 |
您最近一年使用:0次
解题方法
2 . 过氧化钠和氢化钙与水的反应分别为①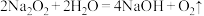 ;②
;② 。下列说法错误的是
。下列说法错误的是
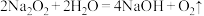 ;②
;② 。下列说法错误的是
。下列说法错误的是| A.①中水发生氧化反应,②中水发生还原反应 |
B. 中存在离子键和非极性键, 中存在离子键和非极性键, 中只存在离子键不存在非极性键 中只存在离子键不存在非极性键 |
C. 中阴、阳离子个数比为1:2, 中阴、阳离子个数比为1:2, 中阴、阳离子个数比为2:1 中阴、阳离子个数比为2:1 |
D.当反应①和②中转移的电子数相同时,产生的 和 和 的物质的量之比为1:2 的物质的量之比为1:2 |
您最近一年使用:0次
名校
解题方法
3 . 某种化合物(如图)由W、X、Y、Z四种短周期元素组成,其中W、Y、Z分别位于三个不同周期,Y核外最外层电子数是W核外最外层电子数的二倍;W、X、Y三种简单离子的核外电子排布相同,下列说法正确的是
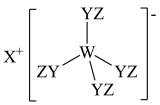

A.原子半径: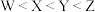 |
B.简单离子的氧化性: |
| C.X与Y、Y与Z均可形成具有漂白性的化合物 |
| D.W元素只能形成离子化合物 |
您最近一年使用:0次
名校
4 . 设NA表示阿伏加德罗常数的值。下列说法不正确的是
| A.0.1NASO2与足量氧气反应生成SO3的质量为8克 |
| B.标准状况下,11.2LCH4含共用电子对数为2NA |
| C.100mL0.1mol·L−1的NaHCO3溶液中含有H原子数为0.01NA |
| D.常温常压下,22g由N2O与CO2组成的混合气体含有的原子数目为1.5NA |
您最近一年使用:0次
解题方法
5 . W、X、Y、Z是四种原子序数依次增大的短周期主族元素,其中X和Y同周期,Y和Z同主族,由这四种元素形成的某种具有强氧化性的物质的结构如图。下列说法错误的是
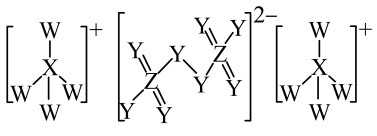
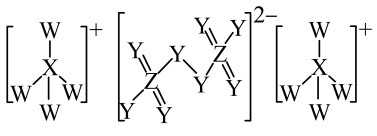
| A.其化学式为(XW4)2Z2Y8,其中Z显+7价 |
| B.X、Y、Z的第一电离能:Y>X>Z |
| C.四种元素均可与钠元素形成离子化合物 |
| D.该物质具有强氧化性是因为含有-Y-Y-键 |
您最近一年使用:0次
名校
6 . 工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
分子筛中含有的O和Na结合而成的Na2O2中含有的化学键包括
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.离子键 | B.非极性共价键 | C.极性共价键 | D.氢键 |
您最近一年使用:0次
7 . 下列物质中,含有极性共价键的是
| A.NaOH | B.NaCl | C.H2 | D.H2S |
您最近一年使用:0次
8 . 下列化合物中含有共价键的是
| A.HCl | B. | C. | D. |
您最近一年使用:0次
名校
9 .  的二聚体分子
的二聚体分子 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
中所有原子均满足8电子稳定结构,一定条件下可发生反应: ,下列说法正确的是
,下列说法正确的是
 的二聚体分子
的二聚体分子 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
中所有原子均满足8电子稳定结构,一定条件下可发生反应: ,下列说法正确的是
,下列说法正确的是A. 不存在离子键和非极性键 不存在离子键和非极性键 |
B. 分子中8个 分子中8个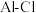 键键长和键能均相同 键键长和键能均相同 |
C. 在熔融状态下能导电 在熔融状态下能导电 |
D.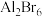 比 比 更难与 更难与 发生反应 发生反应 |
您最近一年使用:0次
名校
10 . 我国建成全球首套千吨级液态太阳能燃料合成示范装置,其原理如图所示。下列说法正确的是
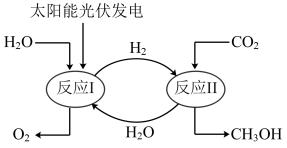

A. 中 中 键和 键和 键个数比是1:1 键个数比是1:1 |
| B.反应Ⅰ和Ⅱ中均存在极性键的断裂和形成 |
C.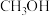 和 和 中碳原子的杂化方式不同 中碳原子的杂化方式不同 |
D.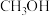 沸点比水低,说明 沸点比水低,说明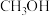 分子间不存在氢键 分子间不存在氢键 |
您最近一年使用:0次
2023-04-20更新
|
155次组卷
|
2卷引用:山东省淄博市沂源县第一中学2022-2023学年高二下学期4月期中考试化学试题



