名校
1 . 汽车尾气已造成严重的环境问题,原因是在电喷条件下,气缸中会发生反应:N2(g)+O2(g)=2NO(g)。如图所示为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是
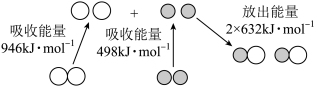

| A.NO分子中各原子均达到8电子稳定结构 |
| B.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
| C.1mol N2(g)和NA个O2(g)反应吸收的能量为180kJ |
| D.1mol N2(g)和1mol O2(g)具有的总能量小于2molNO(g)具有的总能量 |
您最近一年使用:0次
2022-08-29更新
|
206次组卷
|
2卷引用:甘肃省民勤县第一中学2022-2023学年高二上学期开学考试化学试题
名校
2 . 几种短周期元素的原子半径及主要化合价如下表:
下列说法不正确的是
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径/(10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要 化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | …… |
| 最低负价 | …… | -1 | …… | …… | -3 | -2 | |
| A.由元素X和Q组成的化合物可能含有共价键 |
| B.X元素的单质能从MY2溶液中置换出M单质 |
| C.X、Z、R的最高价氧化物对应水化物可彼此反应 |
| D.Z和Y形成的化合物为离子化合物 |
您最近一年使用:0次
解题方法
3 . SiCl4可发生水解反应,机理如下所示。下列说法错误的是
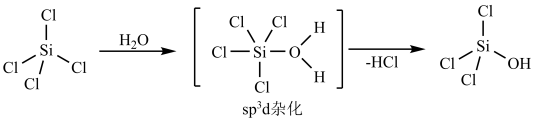
| A.CCl4与SiCl4均是正四面体结构,稳定性SiCl4大于CCl4 |
| B.CCl4与SiCl4均属于分子晶体,CCl4不能按照上述机理发生水解反应 |
| C.SiCl4与H2O的中心原子均采取sp3杂化,键角:SiCl4大于H2O |
| D.基态Si原子核外有8种能量不同的电子 |
您最近一年使用:0次
2022-07-08更新
|
340次组卷
|
2卷引用:山东省济南市2021-2022学年高二下学期期末考试化学试题
4 .  甲烷化是实现“碳达峰”的重要途径,通过氧空位催化剂将
甲烷化是实现“碳达峰”的重要途径,通过氧空位催化剂将 转化为
转化为 的过程如图所示。下列说法正确的是
的过程如图所示。下列说法正确的是
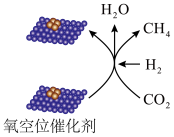
 甲烷化是实现“碳达峰”的重要途径,通过氧空位催化剂将
甲烷化是实现“碳达峰”的重要途径,通过氧空位催化剂将 转化为
转化为 的过程如图所示。下列说法正确的是
的过程如图所示。下列说法正确的是
A.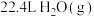 的分子数为 的分子数为 |
B.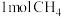 所含极性共价键数目为 所含极性共价键数目为 |
C.每消耗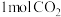 ,生成的 ,生成的 分子数为 分子数为 |
D.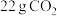 发生反应转移电子数为 发生反应转移电子数为 |
您最近一年使用:0次
5 .  (g)与
(g)与 (g)在催化剂表面经历如下过程生成
(g)在催化剂表面经历如下过程生成 (g):
(g):
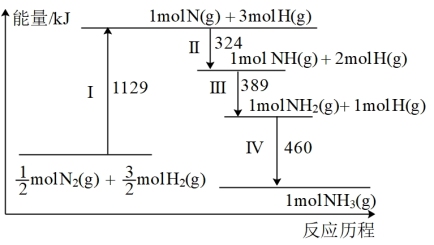
下列说法正确的是
 (g)与
(g)与 (g)在催化剂表面经历如下过程生成
(g)在催化剂表面经历如下过程生成 (g):
(g):
下列说法正确的是
| A.I中破坏的只有非极性键 | B.Ⅳ过程是 与 与 反应生成 反应生成 的过程 的过程 |
| C.Ⅱ、Ⅲ、Ⅳ均为放热过程 | D.合成氨的反应是吸热反应 |
您最近一年使用:0次
名校
6 . 有A、B、C、D、E五种元素,质子数都小于18,B原子的最外层电子数是其电子层数的3倍;C原子失去1个电子所得到的微粒具有与氖原子相同的电子层结构:D是地壳中含量最多的金属元素;E的最高正价与最低负价的代数和为6;A单质可以在E单质中燃烧,生成AE,燃烧时火焰呈苍白色。下列说法错误的是
| A.A2B中只含极性共价键 |
| B.B和C两种元素形成的化合物一定含有离子键和共价键 |
| C.E单质可以使干燥的红色布条褪色 |
| D.D单质常温下既能溶于稀盐酸也能溶于氢氧化钠溶液 |
您最近一年使用:0次
解题方法
7 . 下列有关化学键、氢键和范德华力的叙述中,不 正确的是
| A.在由分子所构成的物质中,分子间作用力越大,该物质越稳定 |
| B.共价键是原子之间通过共用电子对形成的化学键,共价键有方向性和饱和性 |
| C.范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大 |
| D.氢键不是化学键而是分子间的一种作用力,所以氢键只存在于分子与分子之间 |
您最近一年使用:0次
2022-04-14更新
|
163次组卷
|
2卷引用:海南省东方中学2021-2022学年高二下学期第一次月考化学试题
名校
8 . X、Y、Z、W为原子序数递增的四种短周期元素。已知X的阴离子电子层结构与氦原子电子层结构相同;Y原子的最外层电子数是其次外层电子数的两倍;Z有Z2和Z3两种常见的同素异形体;W+的电子层结构与Ne的电子层结构相同。下列说法正确的是
| A.化合物WXYZ3中含有离子键和极性共价键,属于离子化合物 |
| B.已知YZ2分子的空间结构是直线形,则分子中共价键键角为180° |
| C.化合物WX能与水反应生成强碱,该反应属于复分解反应 |
| D.元素X、Z形成的化合物中不可能含有非极性键 |
您最近一年使用:0次
9 . 下列有关H2S和H2O2性质的解释合理的是
| 选项 | 性质 | 解释 |
| A | 常温下,H2O2呈液态,H2S呈气态 | H2O2分子间存在氢键,而H2S分子间不存在氢键 |
| B | 双氧水中存在[H3O2]+ | H2O2中氧有孤电子对,H+有空轨道,能形成配位键 |
| C | H2O2能氧化H2S | H2O2中氧的化合价只能降低 |
| D | H2S溶液中存在S2- | H2S是离子化合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
10 . 很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
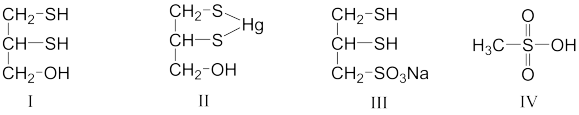
化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有___ 。
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C—C—C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C—C—C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次



