名校
1 . 下列变化:①烧碱熔化;② 升华;③
升华;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥
溶于水;⑥ 受热分解为
受热分解为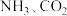 和
和 。其中仅离子键被破坏的是
。其中仅离子键被破坏的是_______ (填序号,下同)仅共价键被破坏的是_______ ;
 升华;③
升华;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥
溶于水;⑥ 受热分解为
受热分解为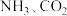 和
和 。其中仅离子键被破坏的是
。其中仅离子键被破坏的是
您最近一年使用:0次
名校
2 . 门捷列夫认为氮、碳、氧、氢是“四大天王”元素,它们与宇宙的形成都有密切联系。
(1)写出由这四种元素的形成的既含离子键又含共价键的化合物的化学式_______
(2)用电子式表示 的形成过程
的形成过程_______
(3)已知HCN中C、N都满足8电子稳定结构,则HCN的结构式为_______
(1)写出由这四种元素的形成的既含离子键又含共价键的化合物的化学式
(2)用电子式表示
 的形成过程
的形成过程(3)已知HCN中C、N都满足8电子稳定结构,则HCN的结构式为
您最近一年使用:0次
名校
3 . 按要求写出恰当的化学用语:
(1)钙原子的结构示意图_______ ;氧离子的电子式_______ ;铝离子的电子式_______ ;硼原子的电子式_______
(2)中子数为21、质子数为19的原子的核组成符号_______
(3)与 电子总数和质子总数都相等的微粒
电子总数和质子总数都相等的微粒_______ 、_______
(4)与Ne原子电子数相同的含有三个原子核的分子的电子式_______
(1)钙原子的结构示意图
(2)中子数为21、质子数为19的原子的核组成符号
(3)与
 电子总数和质子总数都相等的微粒
电子总数和质子总数都相等的微粒(4)与Ne原子电子数相同的含有三个原子核的分子的电子式
您最近一年使用:0次
名校
解题方法
4 . 按下列要求填空:
Ⅰ. 有下列物质:①Cl2 ②HCl ③ NaOH ④Na2O2 ⑤CO2 ⑥MgF2 ⑦NH4Cl
(1)含有共价键的离子化合物是___________ (填序号,下同)。
(2)属于共价化合物是___________ 。
(3)写出⑤的电子式___________ 。
Ⅱ.下列变化中:①蔗糖溶于水 ②Na2O2 溶于水 ③氨气液化 ④烧碱熔化 ⑤NaCl溶于水 ⑥SO2溶于水 ⑦硫酸氢钾溶于水
(4)只有离子键被破坏的是___________ ,只有共价键被破坏的是___________ 。
(5)既有离子键被破坏,又有共价键被破坏的是___________ 。
Ⅰ. 有下列物质:①Cl2 ②HCl ③ NaOH ④Na2O2 ⑤CO2 ⑥MgF2 ⑦NH4Cl
(1)含有共价键的离子化合物是
(2)属于共价化合物是
(3)写出⑤的电子式
Ⅱ.下列变化中:①蔗糖溶于水 ②Na2O2 溶于水 ③氨气液化 ④烧碱熔化 ⑤NaCl溶于水 ⑥SO2溶于水 ⑦硫酸氢钾溶于水
(4)只有离子键被破坏的是
(5)既有离子键被破坏,又有共价键被破坏的是
您最近一年使用:0次
5 . 在下列物质中:①CO2、②KCl、③CaBr2、④O2、⑤NH4Cl、⑥Ca(OH)2、⑦N2、⑧HBr、⑨NH3、⑩Na2O2、⑪金属铜,请用序号回答下列问题:
(1)只有非极性键的是___________ 。
(2)只有极性键的是___________ 。
(3)只有离子键的是___________ 。
(4)有离子键,也有非极性键的是___________ 。
(5)既有离子键,又有极性键的是___________ 。
(6)属于离子化合物的是___________ 。
(7)属于共价化合物的是___________ 。
(8)含有配位键的物质是___________ ,含有金属键的物质是___________ 。
(1)只有非极性键的是
(2)只有极性键的是
(3)只有离子键的是
(4)有离子键,也有非极性键的是
(5)既有离子键,又有极性键的是
(6)属于离子化合物的是
(7)属于共价化合物的是
(8)含有配位键的物质是
您最近一年使用:0次
名校
6 . 利用下列物质的序号填空
①HCl② ③Ne④
③Ne④ ⑤
⑤ ⑥NaOH⑦Ar
⑥NaOH⑦Ar
(1)不存在化学键的是___________ ;
(2)属于共价化合物的是___________ ;
(3)属于离子化合物的是___________ ;
(4)既含离子键,又含共价键的是___________ 。
①HCl②
 ③Ne④
③Ne④ ⑤
⑤ ⑥NaOH⑦Ar
⑥NaOH⑦Ar(1)不存在化学键的是
(2)属于共价化合物的是
(3)属于离子化合物的是
(4)既含离子键,又含共价键的是
您最近一年使用:0次
7 . NH3是制备氮肥的原料之一。
(1)写出NH3的电子式。___________
(2)下列关于NH3的说法错误的是___________。
(1)写出NH3的电子式。
(2)下列关于NH3的说法错误的是___________。
| A.极易溶于水 | B.可用作制冷剂 | C.属于电解质 | D.属于共价化合物 |
您最近一年使用:0次
8 . 过氧化氢(H2O2)又叫双氧水,其水溶液可用于制备工业上的漂白剂、特殊环境中燃料燃烧的助燃剂、医疗上的消毒剂、实验室里的制氧剂等。过氧化钠(Na2O2)可用于制备工业上的漂白剂、实验室里的制氧剂、呼吸面具或潜水艇中的制氧剂等。过氧原子团“O ”由2个氧原子共用1对电子形成。
”由2个氧原子共用1对电子形成。
(1)分别写出H2O2、Na2O2的电子式:___________ 、___________ 。
(2)①H2O、H2O2中化学键的不同点是___________ 。
②Na2O、Na2O2中化学键不同点是___________ 。
③H2O2的化合物类型是___________ (填“共价化合物”或“离子化合物”)。
(3)分别写出H2O2、Na2O2作供氧剂的化学方程式:H2O2:___________ 。Na2O2:___________ 。
(4)H2O2与Na2O2相比,化学键更稳定的是___________ (写物质的名称),主要根据是___________ 。
 ”由2个氧原子共用1对电子形成。
”由2个氧原子共用1对电子形成。(1)分别写出H2O2、Na2O2的电子式:
(2)①H2O、H2O2中化学键的不同点是
②Na2O、Na2O2中化学键不同点是
③H2O2的化合物类型是
(3)分别写出H2O2、Na2O2作供氧剂的化学方程式:H2O2:
(4)H2O2与Na2O2相比,化学键更稳定的是
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题:
(1)已知有下列物质:①HNO3;②NaOH;③液氦;④Na2O2;⑤H2O2;⑥CCl4;⑦NH4Cl;⑧KBr,分别将正确的序号填入相应的位置。以上物质中只含有离子键的是_______ ;只含有共价键的是_______ ;含有非极性共价键的离子化合物是_______ ;不含化学键的是_______ 。
(2)在完整的周期表中第三周期半径最大的主族元素,该元素单质与氧气在加热条件下反应,得到产物R,则R中阴离子与阳离子个数比为:_______ 。
(3)硒(Se)化铟(In)是一种新型半导体材料。下列说法正确的是_______(填序号)。
(4)已知短周期四种主族元素分别形成的离子X+、Y2+、Zˉ、W2ˉ均具有相同的电子层结构,则X、Y、Z、W这四种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(5)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ C+D↑,则A+的电子式为
C+D↑,则A+的电子式为_______ ;比较C和D的稳定性的强弱:_______ (用化学式表示)。
(6)质量相同的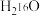 和
和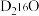 所含中子数之比为
所含中子数之比为_______ 。
(1)已知有下列物质:①HNO3;②NaOH;③液氦;④Na2O2;⑤H2O2;⑥CCl4;⑦NH4Cl;⑧KBr,分别将正确的序号填入相应的位置。以上物质中只含有离子键的是
(2)在完整的周期表中第三周期半径最大的主族元素,该元素单质与氧气在加热条件下反应,得到产物R,则R中阴离子与阳离子个数比为:
(3)硒(Se)化铟(In)是一种新型半导体材料。下列说法正确的是_______(填序号)。
| A.原子半径:In>Se | B.In比Se易失去电子 |
| C.In的金属性比Al弱 | D.硒化铟的化学式为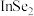 |
(5)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
 C+D↑,则A+的电子式为
C+D↑,则A+的电子式为(6)质量相同的
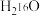 和
和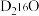 所含中子数之比为
所含中子数之比为
您最近一年使用:0次
解题方法
10 . 构成离子晶体的作用力
构成离子晶体的作用力是_____ 。
构成离子晶体的作用力是
您最近一年使用:0次



