1 . 有四种原子:① ②
②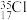 ③
③ ④
④ 。
。
(1)其中能与②形成离子键的是_______ (填序号)。
(2)①和②形成的化学键是_______ (填“极性键”或“非极性键”)。
(3)②和③互为同位素的本质原因是_______ 。
(4)④的原子结构示图是_______ 。
 ②
②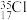 ③
③ ④
④ 。
。(1)其中能与②形成离子键的是
(2)①和②形成的化学键是
(3)②和③互为同位素的本质原因是
(4)④的原子结构示图是
您最近一年使用:0次
2 . 下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)画出①和③两种元素的原子1:2组成的化合物的电子式_______ 。
(2)元素①-⑩中化学性质最不活泼的元素是_______ (填元素符号)。
(3)⑧的离子结构示意图为_______ 。
(4)用电子式表示③与⑤形成的原子个数比为1 ∶2的化合物的形成过程_______ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在⑧的下方,下列推断正确的是_______(填字母序号)
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①-⑩中化学性质最不活泼的元素是
(3)⑧的离子结构示意图为
(4)用电子式表示③与⑤形成的原子个数比为1 ∶2的化合物的形成过程
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在⑧的下方,下列推断正确的是_______(填字母序号)
| A.SeO2具有还原性 | B.H2Se的稳定性比H2S强 |
| C.H2SeO4的酸性强于H2SO4 | D.SeO2在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
3 . 元素周期表的建立和元素周期律的发现,揭示了元素“位”“构”“性”之间的内在联系,可以根据“位”“构”的特点预测和解释元素的性质。下图是元素周期表的一部分,请回答下列问题:
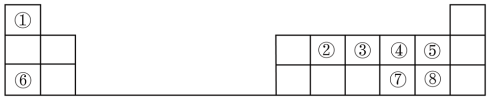
(1)元素⑦在周期表中的位置是
(2)元素③、④的原子半径大小关系正确的是
(3)元素④、⑦的非金属性强弱关系正确的是
(4)元素①、⑧形成化合物的电子式正确的是
(5)元素②有多种同位素,这些同位素具有相同的
(6)下列各组元素形成的化合物中只含有离子键的是

(1)元素⑦在周期表中的位置是
| A.第二周期、第ⅣA族 | B.第二周期、第ⅥA族 |
| C.第三周期、第ⅣA族 | D.第三周期、第ⅥA族 |
| A.③>④ | B.③<④ | C.③=④ | D.无法确定 |
| A.④>⑦ | B.④<⑦ | C.④=⑦ | D.无法确定 |
| A.HCl | B.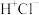 | C.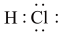 | D.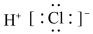 |
| A.质量数和电子数 | B.质子数和电子数 |
| C.质子数和中子数 | D.质量数和中子数 |
| A.①和④ | B.②和④ | C.①和⑤ | D.⑥和⑧ |
您最近一年使用:0次
名校
4 . 2020年有科学家通过观察金星的酸性云层,分析出金星存在磷化氢(PH3)气体,从而推测金星可能存在生命的迹象。
(1)P的原子结构示意图____ 。
(2)PH3中P原子与H原子之间的相互作用是____ (填“离子键”或“共价键”)。
(3)非金属性S强于P,从原子结构解释原因___ ,得电子能力S大于P。
(4)下列关于N、P元素及化合物的说法正确的是____ (填序号)。
①磷元素的最高正化合价为+5
②气态氢化物的稳定性:NH3<PH3
③磷的最高价氧化物对应的水化物属于酸
(1)P的原子结构示意图
(2)PH3中P原子与H原子之间的相互作用是
(3)非金属性S强于P,从原子结构解释原因
(4)下列关于N、P元素及化合物的说法正确的是
①磷元素的最高正化合价为+5
②气态氢化物的稳定性:NH3<PH3
③磷的最高价氧化物对应的水化物属于酸
您最近一年使用:0次
解题方法
5 . I.按下列要求填空
(1)下列变化:①碘的升华,②冰熔化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解
化学键未被破坏的是___________ ;仅共价键被破坏的是___________ 。
(2)写出 Na2O2的电子式:___________ 。其所含化学键类型为___________ 。
(3)用电子式表示 Na2S 的形成过程:___________ 。
II.被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。下图为氢氧燃料电池的结构示意图,
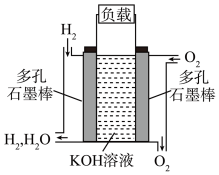
电解质溶液为 KOH 溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:
(4)写出氢氧燃料电池工作时正极电极反应方程式:___________ 。
(5)如果该氢氧燃料电池每转移 0.1mol 电子,消耗标准状况下___________ L 氧气。
(6)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________ 。电池总离子反应方程式为___________ 。
(1)下列变化:①碘的升华,②冰熔化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解
化学键未被破坏的是
(2)写出 Na2O2的电子式:
(3)用电子式表示 Na2S 的形成过程:
II.被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。下图为氢氧燃料电池的结构示意图,

电解质溶液为 KOH 溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:
(4)写出氢氧燃料电池工作时正极电极反应方程式:
(5)如果该氢氧燃料电池每转移 0.1mol 电子,消耗标准状况下
(6)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为
您最近一年使用:0次
6 . 下列物质:①N2②CO2③NH3④Na2O⑤Na2O2⑥NaOH⑦CaBr2⑧H2O2⑨NH4Cl⑩HBr。回答下列问题:(填序号)
(1)只含非极性键的是____ 。
(2)含有极性键和非极性键的是____ 。
(3)含有极性键的离子化合物是____ 。
(4)写出下列物质的电子式:
H2O____ 、KCl____ 、CH4____ 。
(5)用电子式表示NaCl和HCl的形成过程:
NaCl_____ ;HCl____ 。
(1)只含非极性键的是
(2)含有极性键和非极性键的是
(3)含有极性键的离子化合物是
(4)写出下列物质的电子式:
H2O
(5)用电子式表示NaCl和HCl的形成过程:
NaCl
您最近一年使用:0次
7 . 在一个小烧杯里加入研细的20gBa(OH)2·8H2O晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入10gNH4Cl晶体,并用玻璃棒快速搅拌。
(1)NH4Cl所含有的化学键类型有___________ 。
(2)该实验中产生的刺激性气味的气体为___________ ;试验中能观察到反应混合物呈糊状以外,还有玻璃片上因结冰而与小烧杯粘在一起,该反应为___________ (填“吸”或“放”)热反应,说明反应物的总能量___________ (填“大于”或“小于”)生成物的总能量。
(3)实验中要用玻璃棒搅拌的原因是___________ 。
(4)写出该反应的化学方程式___________ 。
(1)NH4Cl所含有的化学键类型有
(2)该实验中产生的刺激性气味的气体为
(3)实验中要用玻璃棒搅拌的原因是
(4)写出该反应的化学方程式
您最近一年使用:0次
8 . X、Y、Z是短周期主族元素,在元素周期表中相对位置如图所示:
已知:Y的最外层有4个电子。请回答下列问题:
(1)X元素的元素符号是_______ ;
(2)Y元素在周期表中位于第_______ 族;
(3)Z的氢化物中的化学键属于_______ (填“离子键”或“共价键”);
(4)化合物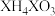 属于
属于_______ (填“酸”“碱”或“盐”)。
| X | ||
| Y | Z |
(1)X元素的元素符号是
(2)Y元素在周期表中位于第
(3)Z的氢化物中的化学键属于
(4)化合物
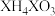 属于
属于
您最近一年使用:0次
名校
9 . 某汽车安全气囊的产气药剂主要含有 等物质。当汽车发生碰撞时,产生大量气体使气囊迅膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产生大量气体使气囊迅膨胀,从而起到保护作用。
(1) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 ,
, 的电子式为
的电子式为___________ 。
(2) 含有的化学键类型为
含有的化学键类型为___________ ,K在周期表中的位置为___________ 。
(3)氮和氧两种元素,非金属性较强的是___________ ,请用一个事实说明其强弱___________ 。
(4)某些安全气囊产气药剂中含有 ,碰撞时与
,碰撞时与 发生如下反应产生大量气体。写出完成配平的方程式并标明电子转移方向和数目
发生如下反应产生大量气体。写出完成配平的方程式并标明电子转移方向和数目_____ 。
_____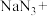 ______
______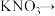 ______
______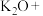 _______
_______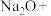 _____
_____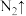
反应中被还原的元素为___________ 。反应中涉及各元素的简单离子半径由大到小排序为___________ 。
 等物质。当汽车发生碰撞时,产生大量气体使气囊迅膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产生大量气体使气囊迅膨胀,从而起到保护作用。(1)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 ,
, 的电子式为
的电子式为(2)
 含有的化学键类型为
含有的化学键类型为(3)氮和氧两种元素,非金属性较强的是
(4)某些安全气囊产气药剂中含有
 ,碰撞时与
,碰撞时与 发生如下反应产生大量气体。写出完成配平的方程式并标明电子转移方向和数目
发生如下反应产生大量气体。写出完成配平的方程式并标明电子转移方向和数目_____
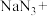 ______
______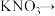 ______
______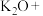 _______
_______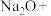 _____
_____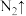
反应中被还原的元素为
您最近一年使用:0次
10 . “天宫”空间站是我国自主研发建造的,用于开展大规模空间科学实验与应用的太空实验基地,空间站的建设离不开各种新型材料的助力。
(1)碳化硅颗粒增强铝基复合材料用于空间站太阳翼伸展机构的关键部位。碳化硅属于_______ 材料,其中碳原子与硅原子之间的化学键属于_______ 键。制备碳化硅晶片的原料之一是高纯硅粉,用焦炭与石英砂(主要成分是 )在高温条件下反应生成硅的化学方程式是
)在高温条件下反应生成硅的化学方程式是_______ 。
(2)氮化硼陶瓷基复合材料电推进系统是一种先进的空间推进技术。根据原子结构和元素周期律的知识可知,氮化硼的化学式为_______ 。推进器中的放电腔内有高压电场、高温环境,用氮化硼陶瓷基复合材料制成放电腔,利用了氮化硼具有_______ 的性质(写一条)。
(1)碳化硅颗粒增强铝基复合材料用于空间站太阳翼伸展机构的关键部位。碳化硅属于
 )在高温条件下反应生成硅的化学方程式是
)在高温条件下反应生成硅的化学方程式是(2)氮化硼陶瓷基复合材料电推进系统是一种先进的空间推进技术。根据原子结构和元素周期律的知识可知,氮化硼的化学式为
您最近一年使用:0次



