名校
1 . 下列物质中含有共价键的离子化合物是
| A.H2O2 | B.NH4Cl | C.NaCl | D.H2S |
您最近一年使用:0次
22-23高一下·云南曲靖·阶段练习
名校
2 . 含氯消毒液(主要成分为NaClO)与含氯洁厕灵(主要成分为HCl)混用可能会引起中毒,其原因是 。下列说法中不正确的是
。下列说法中不正确的是
 。下列说法中不正确的是
。下列说法中不正确的是A.NaCl的电子式为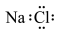 |
B.NaClO与 所含化学键种类完全相同(不考虑配位键) 所含化学键种类完全相同(不考虑配位键) |
C. 中各原子均达到2或8电子稳定结构 中各原子均达到2或8电子稳定结构 |
| D.该反应过程既形成了离子键,又形成极性键和非极性键 |
您最近一年使用:0次
名校
3 . 黑火药是中国古代四大发明之一。爆炸反应为
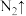 。下列说法不正确的是
。下列说法不正确的是

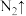 。下列说法不正确的是
。下列说法不正确的是A. 含离子键和共价键 含离子键和共价键 | B. 与 与 具有相同的电子层结构 具有相同的电子层结构 |
C. 的结构式为 的结构式为 | D.干冰的晶体类型为共价晶体 |
您最近一年使用:0次
2023-03-31更新
|
731次组卷
|
5卷引用:江苏省南通市2023届高三第二次调研测试化学试题
4 . NF3常用于微电子工业,可由反应4NH3+3F2 3NH4F+NF3制备。下列说法正确的是
3NH4F+NF3制备。下列说法正确的是
 3NH4F+NF3制备。下列说法正确的是
3NH4F+NF3制备。下列说法正确的是A.中子数为36的铜原子为 Cu Cu | B.NH3的电子式为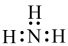 |
| C.NH4F中含有离子键和共价键 | D.NF3是非极性分子 |
您最近一年使用:0次
2023-03-14更新
|
265次组卷
|
3卷引用:江苏省盐城市五校2023届高三下学期3月联考化学试题
名校
解题方法
5 . 铁盐在生产生活中有重要的作用。
(1)绿矾(FeSO4·7H2O)常用作补血剂。
①绿矾中含有的化学键类型有_______ 。
②配制含FeSO4的溶液时,为防止FeSO4被氧化,应采取的措施是_______ 。
(2)工业中常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为_______ 。
(3)一种铁基脱硫剂脱除硫化氢(H2S)的方法包括吸收和再生两个阶段,其工艺流程原理如下:
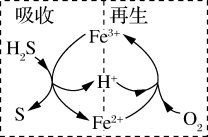
① 写出“再生”的反应的离子方程式:_______ 。
②当吸收224 mL(标准状况)H2S时,若要保持脱硫液中Fe3+的物质的量不变,则所通入的氧气的物质的量为_______ mol(写出计算过程)。
(1)绿矾(FeSO4·7H2O)常用作补血剂。
①绿矾中含有的化学键类型有
②配制含FeSO4的溶液时,为防止FeSO4被氧化,应采取的措施是
(2)工业中常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为
(3)一种铁基脱硫剂脱除硫化氢(H2S)的方法包括吸收和再生两个阶段,其工艺流程原理如下:

① 写出“再生”的反应的离子方程式:
②当吸收224 mL(标准状况)H2S时,若要保持脱硫液中Fe3+的物质的量不变,则所通入的氧气的物质的量为
您最近一年使用:0次
6 . 反应 可实现
可实现 的还原。下列说法正确的是
的还原。下列说法正确的是
 可实现
可实现 的还原。下列说法正确的是
的还原。下列说法正确的是A.中子数为20的氯原子: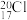 | B. 与 与 具有相同的电子层结构 具有相同的电子层结构 |
C. 的空间填充模型: 的空间填充模型: | D. 既含离子键又含共价键 既含离子键又含共价键 |
您最近一年使用:0次
名校
7 . 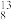 O、
O、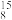 O的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
O的半衰期很短,自然界中不能稳定存在。人工合成反应如下: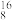 O+
O+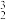 He
He
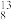 O+
O+ X;
X;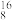 O+
O+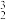 He
He
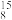 O+
O+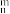 Y。下列说法正确的是
Y。下列说法正确的是
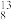 O、
O、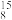 O的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
O的半衰期很短,自然界中不能稳定存在。人工合成反应如下: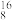 O+
O+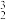 He
He
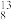 O+
O+ X;
X;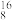 O+
O+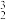 He
He
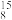 O+
O+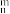 Y。下列说法正确的是
Y。下列说法正确的是| A.X的中子数为2 |
| B.X、Y互为同位素 |
C.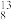 O、 O、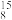 O可用作示踪原子研究化学反应历程 O可用作示踪原子研究化学反应历程 |
D.自然界不存在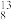 O2、 O2、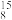 O2分子是因其化学键不稳定 O2分子是因其化学键不稳定 |
您最近一年使用:0次
2023-02-01更新
|
756次组卷
|
5卷引用:江苏省盐城市阜宁县2022-2023学年高一下学期4月期中考试化学试题
江苏省盐城市阜宁县2022-2023学年高一下学期4月期中考试化学试题(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)回归教材重难点05 元素周期律再熟悉-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)山东省泰安市宁阳县第一中学2023-2024学年高一下学期4月月考化学试题
解题方法
8 . 黑火药发生爆炸反应的化学方程式为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A. 中含有离子键和共价键 中含有离子键和共价键 | B. 分子中含有非极性键 分子中含有非极性键 |
C. 的电离方程式: 的电离方程式: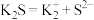 | D.中子数为8的氮原子: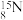 |
您最近一年使用:0次
名校
9 . 下表是元素周期表的一部分,请按要求回答问题:

(1)元素③的一种原子内有6个中子,该原子是___________ (用核素符号回答)。元素④在周期表中的位置为___________ 。
(2)元素⑤、⑨形成的化合物中所含的化学键为___________ 键(填“离子”或“共价”,下同);元素②、④形成的化合物属于___________ 化合物。
(3)元素⑦、⑧、⑨的最高价氧化物的水化物的酸性最强的是___________ (用化学式回答)。
(4)将足量 通入元素⑤的最高价氧化物的水化物的水溶液中,反应后溶液中主要的阴离子是
通入元素⑤的最高价氧化物的水化物的水溶液中,反应后溶液中主要的阴离子是___________ (用化学式回答)。
(5)将铜片投入到元素⑧的最高价氧化物水化物的浓溶液中,加热有气体产生,写出发生反应的化学方程式___________ 。
(6)常温下,单质⑤可与④的氢化物发生反应生成无色无味的气体。写出发生反应的离子方程式:___________ 。

(1)元素③的一种原子内有6个中子,该原子是
(2)元素⑤、⑨形成的化合物中所含的化学键为
(3)元素⑦、⑧、⑨的最高价氧化物的水化物的酸性最强的是
(4)将足量
 通入元素⑤的最高价氧化物的水化物的水溶液中,反应后溶液中主要的阴离子是
通入元素⑤的最高价氧化物的水化物的水溶液中,反应后溶液中主要的阴离子是(5)将铜片投入到元素⑧的最高价氧化物水化物的浓溶液中,加热有气体产生,写出发生反应的化学方程式
(6)常温下,单质⑤可与④的氢化物发生反应生成无色无味的气体。写出发生反应的离子方程式:
您最近一年使用:0次
解题方法
10 . 下列物质中,含有共价键的离子化合物的是
| A.HCl | B.KOH | C.MgF2 | D.CO2 |
您最近一年使用:0次



