名校
1 . 多酚氧化酶是自然界中分布极广的一种金属蛋白酶,与植物的抗病性有关。配合物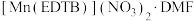 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。___________ 组峰,上述反应的反应类型为___________ ; 是碱性官能团,从结构角度解释原因:
是碱性官能团,从结构角度解释原因:___________ 。
(2)已知EDTA的相对分子质量为292,熔点为250℃,烃 (无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是
(无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是___________ 。
(3)图中有机物在镍催化及加热条件下,不能与 反应的是
反应的是___________ 。EDTA中存在的化学键有___________ (填字母)。
A.离子键 B. 键 C.非极性键 D.氢键
键 C.非极性键 D.氢键
(4)EDTB中氮原子的杂化类型是___________ ,X的VSEPR模型名称是___________ 。
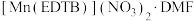 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。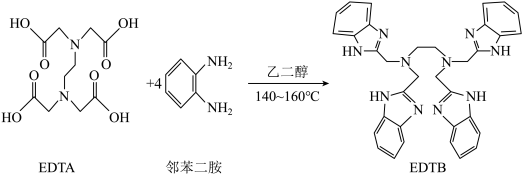 +8X
+8X
 是碱性官能团,从结构角度解释原因:
是碱性官能团,从结构角度解释原因:(2)已知EDTA的相对分子质量为292,熔点为250℃,烃
 (无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是
(无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是(3)图中有机物在镍催化及加热条件下,不能与
 反应的是
反应的是A.离子键 B.
 键 C.非极性键 D.氢键
键 C.非极性键 D.氢键(4)EDTB中氮原子的杂化类型是
您最近半年使用:0次
2 . 目前,全世界镍(Ni)的消费量仅次于铜、铝、铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于___________ 晶体;基态Ni原子的电子排布式为___________ 。
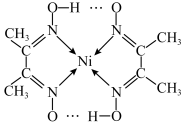
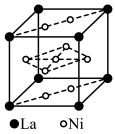
(2)某配合物结构如图所示,分子内含有的作用力有___________ (填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键___________ 。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)某配合物结构如图所示,分子内含有的作用力有
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
您最近半年使用:0次
3 . 下列化合物中既存在离子键,又存在极性键的是
| A.H2O | B.NH4Cl | C.Na2O | D.Na2O2 |
您最近半年使用:0次
名校
解题方法
4 . 下列叙述中正确的有句
①离子键没有方向性和饱和性,而共价键有方向性和饱和性
②配位键在形成时,是由成键双方各提供一个电子形成共用电子对
③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
④在冰晶体中,既有极性键、非极性键,又有氢键
⑤化合物NH4Cl和CuSO4·5H2O都存在配位键
⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同
①离子键没有方向性和饱和性,而共价键有方向性和饱和性
②配位键在形成时,是由成键双方各提供一个电子形成共用电子对
③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
④在冰晶体中,既有极性键、非极性键,又有氢键
⑤化合物NH4Cl和CuSO4·5H2O都存在配位键
⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同
| A.2句 | B.3句 | C.4句 | D.5句 |
您最近半年使用:0次
5 . 某铜(Ⅱ)配合物的结构如下图所示。其中元素X和Y均位于第二周期,X的第一电离能低于同周期相邻元素,Y元素基态原子p轨道电子排布是半充满状态,Z元素基态原子核外电子共有9种空间运动状态。下列说法正确的是

A.最简单氢化物的键角: |
B.基态原子的未成对电子数: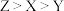 |
| C.X、Y、Z的最简单氢化物均存在分子间氢键 |
| D.该配合物中微粒间的相互作用有离子键、共价键和配位键 |
您最近半年使用:0次
名校
解题方法
6 . 氮氧化物、二氧化硫能引发酸雨、雾霾等。研究含氮、含硫物质的转化是工业、农业、医药、环保等领域的重要课题。回答下列问题:
(1)NO2产生硝酸型酸雨的化学方程式为___________ 。
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为___________ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下:
①“氧化”的目的是___________ 。
②图中产品中含硫成分为___________ (填化学式)。
(4)海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。___________ 种价态。反应③和⑤中,若生成等物质的量的N2,则转移的电子数之比为___________ 。
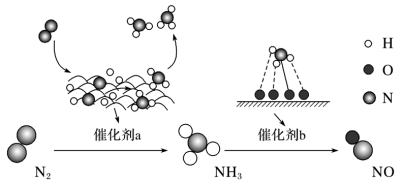
(5)氮及其化合物在催化剂a和催化剂b的作用下转化过程如图所示。下列分析合理的是___________ 。
B.N2与 H2反应属于氮的固定过程
C.在催化剂b表面形成氮氧键时不涉及电子转移
(1)NO2产生硝酸型酸雨的化学方程式为
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为
(3)目前工业上烟气脱硫脱硝的工艺流程如下:
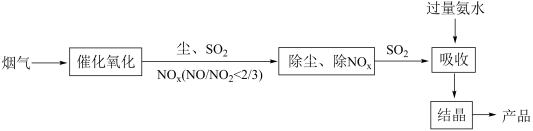
①“氧化”的目的是
②图中产品中含硫成分为
(4)海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。
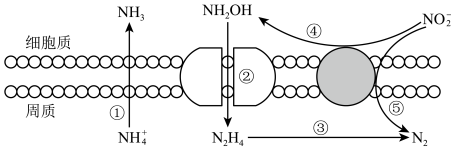
(5)氮及其化合物在催化剂a和催化剂b的作用下转化过程如图所示。下列分析合理的是
B.N2与 H2反应属于氮的固定过程
C.在催化剂b表面形成氮氧键时不涉及电子转移
您最近半年使用:0次
名校
7 . 过氧化钠常用作防毒面具的供氧剂,源自于: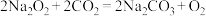 ,下列说法正确的是
,下列说法正确的是
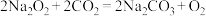 ,下列说法正确的是
,下列说法正确的是A.Na2O2的电子式为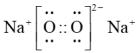 |
B.Na+的结构示意图: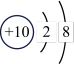 |
| C.16O2和18O3互为同位素 |
| D.碳酸钠属于离子化合物,既含离子键,也含共价键 |
您最近半年使用:0次
名校
8 . 下列有关化学键说法正确的是
| A.化学键是一种作用力,所有的物质都通过化学键形成 |
| B.金属原子和非金属原子间可能形成共价键,非金属元素间也能够形成离子键 |
| C.液态HCl吸热变成HCl气体的过程中有极性键断裂 |
D.硫酸溶于水完全电离成H+和SO ,说明硫酸分子由H+和SO ,说明硫酸分子由H+和SO 组成 组成 |
您最近半年使用:0次
9 . 某铜(Ⅱ)配合物的结构如下图所示。其中元素X和Y均位于第二周期,X的第一电离能低于同周期相邻元素,Y元素基态原子p轨道电子排布是半充满状态,Z元素基态原子核外电子共有9种空间运动状态。
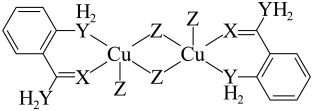
下列说法正确的是

下列说法正确的是
| A.最简单氢化物的键角:X>Y |
| B.基态原子的未成对电子数:Z<X<Y |
| C.X、Y、Z的最简单氢化物均存在分子间氢键 |
| D.该配合物中微粒间的相互作用有离子键、共价键和配位键 |
您最近半年使用:0次
名校
解题方法
10 . 侯德榜联合制碱法的原理之一是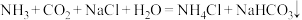 ,下列关于该原理涉及到的物质说法正确的是
,下列关于该原理涉及到的物质说法正确的是
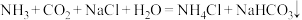 ,下列关于该原理涉及到的物质说法正确的是
,下列关于该原理涉及到的物质说法正确的是A. 晶体中只存在离子键 晶体中只存在离子键 | B. 分子中存在非极性共价键 分子中存在非极性共价键 |
C. 分子中碳原子采取 分子中碳原子采取 杂化 杂化 | D. 分子的空间结构是三角锥形 分子的空间结构是三角锥形 |
您最近半年使用:0次



