解题方法
1 . 人体必需的一些元素在周期表中的分布情况如下:
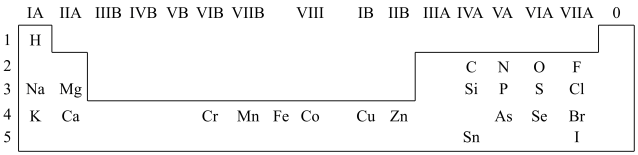
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
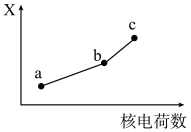
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
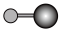 | 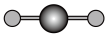 | 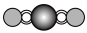 | 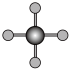 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
名校
解题方法
2 . W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为 的
的 分子。下列说法正确的是
分子。下列说法正确的是
 的
的 分子。下列说法正确的是
分子。下列说法正确的是| A.简单离子半径:Z>X>Y |
| B.X和Y的最简单氢化物的稳定性:X>Y |
| C.W与Y能形成含有非极性键的化合物 |
| D.由W、X、Y三种元素所组成化合物的水溶液均显酸性 |
您最近一年使用:0次
2023-01-01更新
|
582次组卷
|
3卷引用:河南省信阳市华中师大息县附中2022-2023学年高一下学期开学考试化学试题
名校
解题方法
3 . 下列说法中正确的是
| A.CH4和BCl3分子中所有原子的最外层都达到了8电子稳定结构 |
| B.Na2O2、NaClO中所含化学键类型不完全相同 |
| C.将某种化合物溶于水,若能导电说明这种化合物是离子化合物 |
| D.氯气与NaOH反应的过程中,同时有离子键、极性键和非极性键的断裂和形成 |
您最近一年使用:0次
2022-11-02更新
|
190次组卷
|
4卷引用:河南省宋基信阳实验中学2022-2023学年高三上学期11月月考化学试题
4 . 对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。请利用分类法结合所学知识完成下列各小题:
(1)现有下列9种微粒: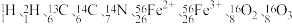 。形成上述9种微粒的核素有
。形成上述9种微粒的核素有___________ 种、元素有___________ 种。以上微粒所含某些元素构成的五核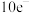 分子的空间构型是
分子的空间构型是___________ ,写出一种由以上两种元素构成含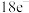 的微粒的电子式
的微粒的电子式___________
(2)现有以下物质:①稀盐酸 ② ③
③ 固体 ④NaOH溶液 ⑤熔融
固体 ④NaOH溶液 ⑤熔融 ⑥
⑥ ⑦铝条 ⑧蔗糖。以上物质中能导电的是
⑦铝条 ⑧蔗糖。以上物质中能导电的是___________ (填标号,下同),属于电解质的是___________ ,属于非电解质的是___________ 。
(3)已知有下列物质:① ②NaCl ③
②NaCl ③ ④
④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦ 这些物质中,只含有离子键的是
这些物质中,只含有离子键的是___________ ,含有非极性共价键的离子化合物是___________ ,属于共价化合物的是___________ 。用电子式表示 的形成过程
的形成过程___________ , 的结构式
的结构式___________
(1)现有下列9种微粒:
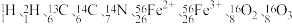 。形成上述9种微粒的核素有
。形成上述9种微粒的核素有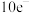 分子的空间构型是
分子的空间构型是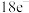 的微粒的电子式
的微粒的电子式(2)现有以下物质:①稀盐酸 ②
 ③
③ 固体 ④NaOH溶液 ⑤熔融
固体 ④NaOH溶液 ⑤熔融 ⑥
⑥ ⑦铝条 ⑧蔗糖。以上物质中能导电的是
⑦铝条 ⑧蔗糖。以上物质中能导电的是(3)已知有下列物质:①
 ②NaCl ③
②NaCl ③ ④
④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦ 这些物质中,只含有离子键的是
这些物质中,只含有离子键的是 的形成过程
的形成过程 的结构式
的结构式
您最近一年使用:0次
5 . 氧族元素包括氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)五种元素,是位于元素周期表中第16纵列VIA 族元素。请回答下列问题:
(1)Te的原子序数为______ ;
(2)写出氧族元素中一种含18个电子、4个原子的氢化物的电子式___________ ;
(3)O、S、Se三种元素的简单氢化物沸点由高到低的顺序是______ ;
(4)NaHSO4固体溶于水时,被破坏的化学键类型有_______ ;
(5)钋(Po)是原子序数最大的氧族元素,推测它及其化合物最不可能具有的性质是_____ (填字母)。
A. 钋是能导电的固体 B. 钋的氧化物的水化物至少有两种
C. 钋与氢气很容易化合 D. 钋的氢化物非常稳定
(1)Te的原子序数为
(2)写出氧族元素中一种含18个电子、4个原子的氢化物的电子式
(3)O、S、Se三种元素的简单氢化物沸点由高到低的顺序是
(4)NaHSO4固体溶于水时,被破坏的化学键类型有
(5)钋(Po)是原子序数最大的氧族元素,推测它及其化合物最不可能具有的性质是
A. 钋是能导电的固体 B. 钋的氧化物的水化物至少有两种
C. 钋与氢气很容易化合 D. 钋的氢化物非常稳定
您最近一年使用:0次
6 . 关于化学键的下列叙述中正确的是.
| A.离子化合物可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.离子化合物不能含共价键 |
您最近一年使用:0次



