名校
解题方法
1 . 甲酸在纳米级磁性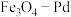 表面分解为活性
表面分解为活性 和
和 ,经下列历程实现
,经下列历程实现 方的催化还原,从而减少污染。已知:分子中的大
方的催化还原,从而减少污染。已知:分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )。下列说法错误的是
)。下列说法错误的是
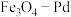 表面分解为活性
表面分解为活性 和
和 ,经下列历程实现
,经下列历程实现 方的催化还原,从而减少污染。已知:分子中的大
方的催化还原,从而减少污染。已知:分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )。下列说法错误的是
)。下列说法错误的是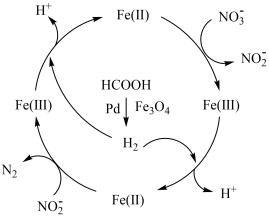
A.纳米级磁性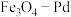 可以降低甲酸分解反应的活化能 可以降低甲酸分解反应的活化能 |
B.反应中 转化为 转化为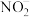 大 大 键的变化表示为 键的变化表示为 |
C.反应历程中生成的 可调节体系 可调节体系 ,有增强 ,有增强 氧化性的作用 氧化性的作用 |
D.总反应方程式为 |
您最近半年使用:0次
2 . 几种氧化物的化学键中离子键成分的百分数如下表所示:
根据表格信息,可推知:前四周期元素组成的离子晶体中,离子键成分的百分数最高的是
氧化物 |
|
|
|
|
离子键成分的百分数/ | 62 | 50 | 41 | 33 |
A.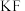 | B. | C. | D. |
您最近半年使用:0次
3 . 以粗盐和石英砂为原料制备纯碱和精硅的流程如下图所示,结合题意回答下列问题:
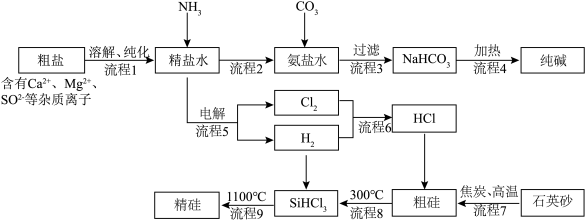
(1)流程1可在实验室完成,过程如下图所示,若只加一种试剂,则A化学式为________________ 。
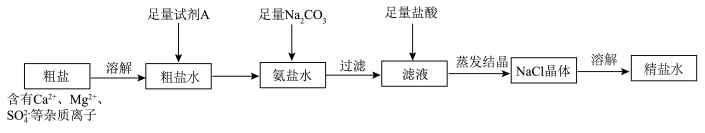
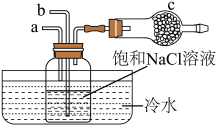
(2)流程2和流程3也可在实验室模拟完成,具体过程如图所示,则a口通入________________ 气体,c装置固体为________________ 。
(3)流程4生成的Na2CO3,其含有的化学键为________________ 。
(4)流程7的化学方程式________________ 。
(5)流程9整个制备过程必须严格控制无氧,若混入O2,可能引起的后果是________________ 。
(6)制得的精硅含有微量硼,会影响芯片性能。某实验室利用区域熔炼技术制高纯硅的装置剖面图如图1,将含微量杂质硼的硅晶棒装入石英保温管中,利用加热环自左向右缓慢移动对其进行加热熔炼,已知杂质硼在不同状态的硅中含量分布如图2所示。
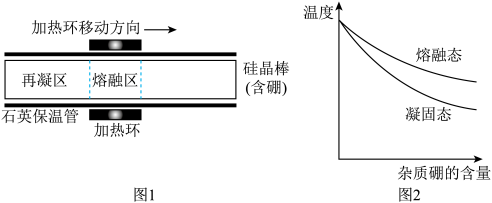
下列说法中错误的是________________。

(1)流程1可在实验室完成,过程如下图所示,若只加一种试剂,则A化学式为

(2)流程2和流程3也可在实验室模拟完成,具体过程如图所示,则a口通入

(3)流程4生成的Na2CO3,其含有的化学键为
(4)流程7的化学方程式
(5)流程9整个制备过程必须严格控制无氧,若混入O2,可能引起的后果是
(6)制得的精硅含有微量硼,会影响芯片性能。某实验室利用区域熔炼技术制高纯硅的装置剖面图如图1,将含微量杂质硼的硅晶棒装入石英保温管中,利用加热环自左向右缓慢移动对其进行加热熔炼,已知杂质硼在不同状态的硅中含量分布如图2所示。

下列说法中错误的是________________。
| A.混有杂质硼的硅晶棒熔点低于纯硅 |
| B.熔炼前,可以用普通玻璃管替换石英保温管 |
| C.熔炼时,加热环移动速度过快可能导致杂质硼分离不彻底 |
| D.熔炼后,硅晶棒纯度右端高于左端 |
您最近半年使用:0次
名校
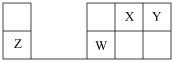
4 . 如图所示为元素周期表的一部分,其中X、Y、Z、W为四种短周期元素。Z元素原子核外K层与M层上的电子数相等。下列说法中正确的是

A.Y元素的最高价氧化物对应的水化物的化学式为 |
B.最高价氧化物对应水化物的酸性: |
C.原子半径由小到大的顺序为 |
| D.X、Z两种元素的氧化物中所含化学键的类型相同 |
您最近半年使用:0次
5 . 氧化基纳米催化剂可用于CO2选择性加氢制备CH3OH,其反应机理如图所示,下列说法错误的是
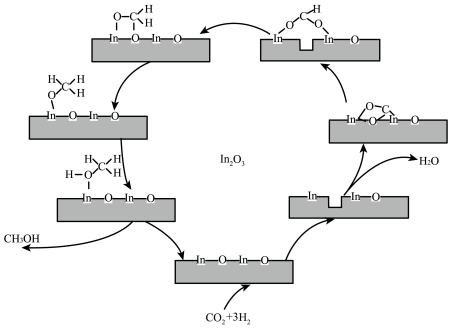

| A.In为49号元素,其价层电子排布式为5s25p1 |
| B.该反应过程中存在非极性键的断裂和形成 |
| C.CH3OH和CO2中,碳原子的杂化方式不同 |
D.该反应的总化学方程式为CO2+3H2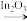 CH3OH+H2O CH3OH+H2O |
您最近半年使用:0次
6 . 下列说法正确的是
A.常温下白磷可自燃而氮气需在放电时才与氧气反应,则非金属性: |
B.第IA族元素铯的两种同位素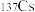 比 比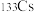 多4个质子 多4个质子 |
C.从上到下,卤族元素的非金属性逐渐减弱,所以酸性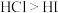 |
| D.离子化合物中既可以含有极性共价键又可以含有非极性共价键 |
您最近半年使用:0次
名校
7 . 冰晶石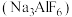 是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
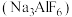 是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是| A.离子键 | B.配位键 | C. 键 键 | D. 键 键 |
您最近半年使用:0次
2023-05-21更新
|
114次组卷
|
2卷引用:江西省九江市湖口中学2022-2023学年高二下学期7月期末考试化学试题
名校
解题方法
8 . 按要求完成下列填空:
Cu2+能与NH3、H2O、OH-、Cl-等形成配位数为4的配合物
(1)向CuSO4溶液中加入过量NaOH溶液可生成 。
。
①画出配离子 的结构:
的结构:_______ 。
②写出该过程生成 的化学方程式
的化学方程式_______ 。
③ 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有_______ 。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)Cu2+可以与乙二胺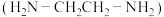 形成配离子(如图):
形成配离子(如图):
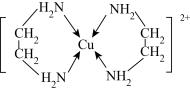
①乙二胺分子中N原子成键时采取的杂化类型是_______ 。
②乙二胺沸点高于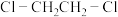 的主要原因是
的主要原因是_______ 。
Cu2+能与NH3、H2O、OH-、Cl-等形成配位数为4的配合物
(1)向CuSO4溶液中加入过量NaOH溶液可生成
 。
。①画出配离子
 的结构:
的结构:②写出该过程生成
 的化学方程式
的化学方程式③
 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)Cu2+可以与乙二胺
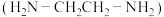 形成配离子(如图):
形成配离子(如图):
①乙二胺分子中N原子成键时采取的杂化类型是
②乙二胺沸点高于
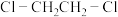 的主要原因是
的主要原因是
您最近半年使用:0次
2023-04-27更新
|
252次组卷
|
3卷引用:江西省高安市灰埠中学2022-2023学年高二下学期5月期中考试化学试题
名校
9 . 下列各组晶体物质中:① 和
和 ;②晶体硼和晶体铝;③NaBr和HBr;④晶体硅和金刚石;⑤晶体氖和晶体氮;⑥
;②晶体硼和晶体铝;③NaBr和HBr;④晶体硅和金刚石;⑤晶体氖和晶体氮;⑥ 和
和 ,化学键类型相同,晶体类型也相同的是
,化学键类型相同,晶体类型也相同的是
 和
和 ;②晶体硼和晶体铝;③NaBr和HBr;④晶体硅和金刚石;⑤晶体氖和晶体氮;⑥
;②晶体硼和晶体铝;③NaBr和HBr;④晶体硅和金刚石;⑤晶体氖和晶体氮;⑥ 和
和 ,化学键类型相同,晶体类型也相同的是
,化学键类型相同,晶体类型也相同的是| A.①②③ | B.②③④ | C.④⑥ | D.③⑤ |
您最近半年使用:0次
2023-03-30更新
|
300次组卷
|
4卷引用:江西省南昌市第十九中学2022-2023学年高二下学期期中考试化学试卷
名校
解题方法
10 . 铂(Pt)的单质又称白金,是常用的催化剂和电极材料,顺二氨环丁羧酸铂(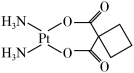 )又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:
)又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:
(1)用酒精把铂丝润湿点燃,酒精剧烈燃烧,使铂丝温度达到炽热程度,同时伴有很亮的光。产生上述现象可能的原因是___________ 。
(2)卡铂分子中非金属元素的电负性由大到小的顺序为___________ ,碳原子的杂化轨道类型有___________ 。
(3)卡铂静脉注射时需要注意的事项是___________ 。
(4)卡铂分子中存在的作用力有___________(填标号)。
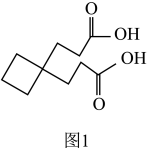
(5)合成卡铂的中间体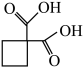 沸点比图1中化合物沸点低,原因是
沸点比图1中化合物沸点低,原因是___________ 。
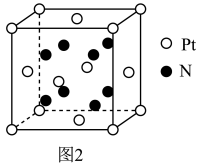
(6)超硬材料(仅次于金刚石)氮化铂的一种晶胞如图2所示,N的配位数是___________ 。
 )又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:
)又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:(1)用酒精把铂丝润湿点燃,酒精剧烈燃烧,使铂丝温度达到炽热程度,同时伴有很亮的光。产生上述现象可能的原因是
(2)卡铂分子中非金属元素的电负性由大到小的顺序为
(3)卡铂静脉注射时需要注意的事项是
(4)卡铂分子中存在的作用力有___________(填标号)。
| A.离子键 | B.配位键 | C.金属键 | D.非极性键 |
 沸点比图1中化合物沸点低,原因是
沸点比图1中化合物沸点低,原因是
(6)超硬材料(仅次于金刚石)氮化铂的一种晶胞如图2所示,N的配位数是

您最近半年使用:0次







