解题方法
1 . 有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。A、B、C、D、E五种元素的电负性分别为2.1,3.5,1.5,2.5,0.8,请回答下列问题:
(1)A是_______ ,B是_______ ,C是_______ ,D是_______ ,E是_______ (用化学符号填空,下同)。
(2)由电负性判断,以上五种元素中金属性最强的是_______ ,非金属性最强的是_______ 。
(3)当B与A、C、D分别形成化合物时,B显_______ 价(填“正”或“负”或“零”,下同),其他元素显_______ 价。
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是_______ (填化学式)。
(1)A是
(2)由电负性判断,以上五种元素中金属性最强的是
(3)当B与A、C、D分别形成化合物时,B显
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是
您最近一年使用:0次
解题方法
2 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W元素的气态氢化物能与最高价氧化物对应的水化物反应生成盐,X的原子最外层电子数是其电子层数的3倍,Y的原子半径在同周期金属元素中最大,Z与X同主族。下列说法正确的是
| A.四种元素的简单离子的半径大小依次为W>X>Y>Z |
| B.W和Z的最高价氧化物对应的水化物均为强酸 |
| C.Y2X与Y2X2所含化学键均为离子键 |
| D.Y2X2可与ZX2反应生成化合物Y2ZX3和X2 |
您最近一年使用:0次
名校
解题方法
3 . 下列变化中,不需要破坏化学键的是
| A.电解水 | B.碘升华 | C.加热氯酸钾使其分解 | D.氯化钠溶于水 |
您最近一年使用:0次
名校
4 . 与 晶体中所含化学键类型相同的物质是
晶体中所含化学键类型相同的物质是
 晶体中所含化学键类型相同的物质是
晶体中所含化学键类型相同的物质是A. | B. | C. | D. |
您最近一年使用:0次
2021-11-14更新
|
187次组卷
|
3卷引用:江西省安福县第三中学2021届高三下学期期中考试化学试题
江西省安福县第三中学2021届高三下学期期中考试化学试题上海市进才中学 2021-2022学年高一上学期期中考试化学试题(已下线)第12练 微观结构与物质的多样性-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)
名校
5 . 氮和氮的化合物与人类有密切关系。
(1)氮的固定有利于生物吸收氮。下列属于氮的固定的是___ (填序号)。
①工业上N2和H2合成NH3
②N2和O2放电条件下生成NO
③NH3催化氧化生成NO
(2)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮。下列物质可以用作氧化NO的是___ (填序号)。
A.NaCl溶液 B.NaOH溶液 C.Na2CO3溶液 D.KMnO4溶液
若以NaClO溶液氧化NO,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目___ 。
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如图:
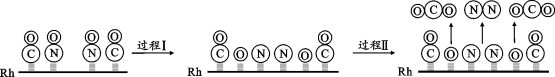
①过程Ⅰ为____ 过程(填“吸热”或“放热”)。过程Ⅱ生成的化学键有___ (填“极性键”、“非极性键”或“极性键和非极性键”)。
②已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为:___ 。
(1)氮的固定有利于生物吸收氮。下列属于氮的固定的是
①工业上N2和H2合成NH3
②N2和O2放电条件下生成NO
③NH3催化氧化生成NO
(2)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮。下列物质可以用作氧化NO的是
A.NaCl溶液 B.NaOH溶液 C.Na2CO3溶液 D.KMnO4溶液
若以NaClO溶液氧化NO,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如图:

①过程Ⅰ为
②已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为:
您最近一年使用:0次
2021-10-01更新
|
285次组卷
|
2卷引用:江西省吉安市(吉安县三中、泰和二中、安福二中、井大附中 )2021-2022学年高二上学期9月联考化学试题
名校
6 . 2021年6月17日,神舟十二号载人飞船成功将3名航天员送入中国空间站,这是中国人首次进入自己的空间站。下列说法错误的是
A.太阳电池翼伸展机构用到的 是一种新型硅酸盐材料 是一种新型硅酸盐材料 |
B.空间站中用 将 将 转化为 转化为 , , 含离子键和非极性键 含离子键和非极性键 |
C.运载火箭的燃料偏二甲肼( )燃烧过程中化学能转化为热能 )燃烧过程中化学能转化为热能 |
D.天和核心舱采用电推发动机“燃料”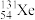 原子核含77个中子 原子核含77个中子 |
您最近一年使用:0次
2021-09-14更新
|
810次组卷
|
7卷引用:江西省九校2021-2022学年高二上学期期中联考化学试题
名校
7 . 已知四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示,下列说法中错误的是


| A.标况下,1 mol SiF4的体积约为22.4 L |
| B.SiX4的沸点依F、Cl、Br、I次序升高的原因是结构相似,分子间作用力依次增大 |
| C.图中所示的SiX4分子中,各原子均满足8电子稳定结构 |
| D.结合PbX2熔点的变化规律,可推断依F、Cl、Br、I次序,PbX2中的化学键的离子性增强、共价性减弱 |
您最近一年使用:0次
名校
解题方法
8 . 下列说法不正确的是
①化学键断裂的过程一定是化学变化②离子化合物中一定含有金属元素③单质中一定含有非极性共价键④HCl溶于水电离出H+和Cl-,因此HCl中含有离子键⑤含有共价键的化合物一定是共价化合物⑥双原子单质分子中的共价键是极性键
①化学键断裂的过程一定是化学变化②离子化合物中一定含有金属元素③单质中一定含有非极性共价键④HCl溶于水电离出H+和Cl-,因此HCl中含有离子键⑤含有共价键的化合物一定是共价化合物⑥双原子单质分子中的共价键是极性键
| A.①②③④⑤⑥ | B.②③④⑤⑥ | C.③④⑤ | D.①②③④ |
您最近一年使用:0次
名校
解题方法
9 . 下列说法中正确的是
| A.由于氢键作用,冰的密度比水的密度大 |
| B.已知CaC2、Mg3N2各原子均达到稳定结构,则两者化学键类型不完全相同 |
| C.将某种化合物溶于水,若能导电说明这种化合物是离子化合物 |
| D.氯气与NaOH反应的过程中,同时有离子键、极性键和非极性键的断裂和形成 |
您最近一年使用:0次
名校
解题方法
10 . 使用NC环金属化Ir(III)配合物催化甲酸脱氢的反应机理如下图。下列说法中错误的是
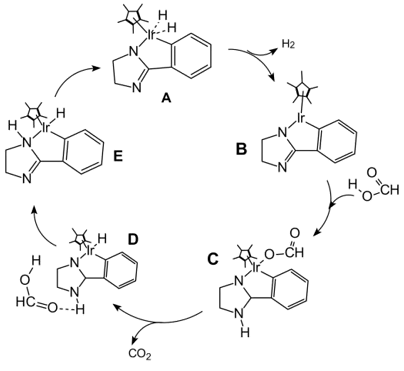

A.甲酸脱氢过程的总反应为HCOOH CO2↑+H2↑ CO2↑+H2↑ |
| B.反应过程中,Ir(III)配合物B为催化剂,Ir(III)配合物A为中间产物 |
| C.由D→E的过程,是甲酸协助转运H的过程 |
| D.反应过程中,HCOOH中的C=O键发生断裂 |
您最近一年使用:0次
2021-06-15更新
|
874次组卷
|
5卷引用:江西省临川一中暨临川一中实验学校2021届高三第三次模拟理科综合能力测试化学试题
江西省临川一中暨临川一中实验学校2021届高三第三次模拟理科综合能力测试化学试题(已下线)2022年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷A(已下线)考点01 物质的组成、分类及转化-备战2022年高考化学学霸纠错(全国通用)2021年湖南省高考化学试卷变式题11-19(已下线)进阶训练6



