名校
解题方法
1 . 下列各组物质中,其化学键类型完全相同的是
| A.NH3和H2O | B.HCl和KCl | C.H2O和H2O2 | D.NH4Cl和NaOH |
您最近半年使用:0次
名校
解题方法
2 . 过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一、
(1)CuCl的盐酸溶液能够与CO发生反应: 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有___________ 。
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2) 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角___________ (填“大于”“小于”或“等于”) 中C—C—O的键角,理由是
中C—C—O的键角,理由是___________ ;元素S、Cl、O的电负性由大到小的顺序为___________ 。
(3) 溶液与乙二胺(
溶液与乙二胺(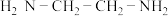 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写): 的配位原子为
的配位原子为___________ 。
②乙二胺分子中氮原子轨道的杂化类型为___________ ,乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是___________ 。
(1)CuCl的盐酸溶液能够与CO发生反应:
 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2)
 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角 中C—C—O的键角,理由是
中C—C—O的键角,理由是(3)
 溶液与乙二胺(
溶液与乙二胺(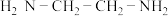 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写):
 的配位原子为
的配位原子为②乙二胺分子中氮原子轨道的杂化类型为
 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
您最近半年使用:0次
名校
3 . 下列说法正确的是
| A.构成物质的分子中一定含有化学键 |
B. 转化为 转化为 时,既有共价键的断裂,又有共价键的形成 时,既有共价键的断裂,又有共价键的形成 |
C. 和 和 分子中每个原子的最外层都具有8电子稳定结构 分子中每个原子的最外层都具有8电子稳定结构 |
D.在 、 、 晶体中,阳离子与阴离子个数比相同 晶体中,阳离子与阴离子个数比相同 |
您最近半年使用:0次
4 . 已知 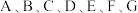 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和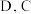 和
和  为同一主族元素,A与
为同一主族元素,A与 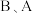 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是_____________ ,画出其原子结构示意图:_________________ .
(2)元素 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为_____________________________ 。
(3)元素B的最低价氢化物的电子式为_____________________ 。
(4)由 所形成的常见离子化合物是
所形成的常见离子化合物是_____________ (写化学式),其所含化学键类型为_____________ 。
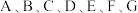 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和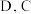 和
和  为同一主族元素,A与
为同一主族元素,A与 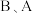 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:(1)七种元素中,非金属性最强的元素在周期表中的位置是
(2)元素
 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为(3)元素B的最低价氢化物的电子式为
(4)由
 所形成的常见离子化合物是
所形成的常见离子化合物是
您最近半年使用:0次
5 . 短周期主族元素  的原子序数依次增大,
的原子序数依次增大, 原子的最外层电子数是其内层电子数的2倍,Y和W同主族,
原子的最外层电子数是其内层电子数的2倍,Y和W同主族, 与
与 有相同的电子层结构,下列说法正确的是
有相同的电子层结构,下列说法正确的是
 的原子序数依次增大,
的原子序数依次增大, 原子的最外层电子数是其内层电子数的2倍,Y和W同主族,
原子的最外层电子数是其内层电子数的2倍,Y和W同主族, 与
与 有相同的电子层结构,下列说法正确的是
有相同的电子层结构,下列说法正确的是A.原子半径大小顺序: |
B. 的最高价氧化物对应水化物的酸性比W的弱 的最高价氧化物对应水化物的酸性比W的弱 |
C.Y分别与 、W形成的化合物中化学键类型相同 、W形成的化合物中化学键类型相同 |
| D.W单质的熔点比Y的低 |
您最近半年使用:0次
解题方法
6 . 下列说法错误的是
| A.离子化合物可能含共价键 |
B. 是共价化合物 是共价化合物 |
| C.只由非金属元素形成的化合物不可能是离子化合物 |
| D.稀有气体分子中不存在化学键 |
您最近半年使用:0次
名校
解题方法
7 . 我国科学家成功合成了世界上首个五氮阴离子盐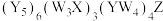 ,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
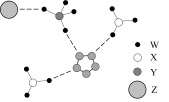
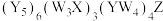 ,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
| A.该部分结构中共有两种氢键 |
B.若 的立体结构是平面五元环,则阴离子 的立体结构是平面五元环,则阴离子 中的键型为氮氮单键 中的键型为氮氮单键 |
| C.该化合物只存在共价键、氢键和配位键三种作用力 |
| D.该化合物中两种阳离子的空间构型分别为正四面体形和三角锥形 |
您最近半年使用:0次
名校
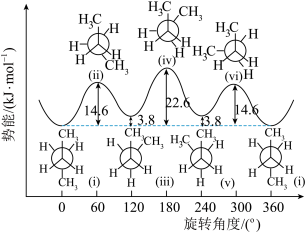
8 . 由单键旋转而产生的异构体称为构象异构体,将正丁烷分子中的 和
和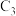 旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
 和
和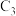 旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
| A.正丁烷的构象异构体中占比最大的是iv |
| B.原子或基团之间的排斥作用决定了构象异构体的稳定性 |
| C.相同条件下,i转化成iii的速率比逆向转化慢 |
| D.构象异构体间的转化存在化学键的断裂和生成 |
您最近半年使用:0次
解题方法
9 . 下列说法错误的是
| A.“雪花六出”体现了晶体的自范性 |
| B.防撞气囊中的NaN3是一种含有共价键的离子化合物 |
| C.钛镁合金的导电性和导热性是通过自由电子定向移动实现的 |
| D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子 |
您最近半年使用:0次
名校
解题方法
10 . 下列说法中正确的是
①非金属元素不可能形成离子化合物 ②位于第四周期第VA族的元素为非金属元素
③可用质谱法区分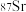 和
和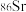 ④金属晶体的导电性、导热性均与自由电子有关
④金属晶体的导电性、导热性均与自由电子有关
⑤分子晶体中一定存在共价键 ⑥金刚石与石墨中的C―C―C夹角都为120°
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6
⑧NaClO和NaCl均为离子化合物,它们所含的化学键类型完全相同
①非金属元素不可能形成离子化合物 ②位于第四周期第VA族的元素为非金属元素
③可用质谱法区分
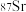 和
和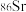 ④金属晶体的导电性、导热性均与自由电子有关
④金属晶体的导电性、导热性均与自由电子有关⑤分子晶体中一定存在共价键 ⑥金刚石与石墨中的C―C―C夹角都为120°
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6
⑧NaClO和NaCl均为离子化合物,它们所含的化学键类型完全相同
| A.①③④⑥ | B.②③④⑦ | C.②③④⑤ | D.②③④⑧ |
您最近半年使用:0次
2024-02-22更新
|
276次组卷
|
2卷引用:山东省青岛市2023-2024学年高二上学期1月期末化学试题



