解题方法
1 . 下列说法错误的是
| A.“雪花六出”体现了晶体的自范性 |
| B.防撞气囊中的NaN3是一种含有共价键的离子化合物 |
| C.钛镁合金的导电性和导热性是通过自由电子定向移动实现的 |
| D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法中正确的是
①非金属元素不可能形成离子化合物 ②位于第四周期第VA族的元素为非金属元素
③可用质谱法区分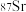 和
和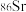 ④金属晶体的导电性、导热性均与自由电子有关
④金属晶体的导电性、导热性均与自由电子有关
⑤分子晶体中一定存在共价键 ⑥金刚石与石墨中的C―C―C夹角都为120°
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6
⑧NaClO和NaCl均为离子化合物,它们所含的化学键类型完全相同
①非金属元素不可能形成离子化合物 ②位于第四周期第VA族的元素为非金属元素
③可用质谱法区分
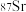 和
和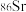 ④金属晶体的导电性、导热性均与自由电子有关
④金属晶体的导电性、导热性均与自由电子有关⑤分子晶体中一定存在共价键 ⑥金刚石与石墨中的C―C―C夹角都为120°
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6
⑧NaClO和NaCl均为离子化合物,它们所含的化学键类型完全相同
| A.①③④⑥ | B.②③④⑦ | C.②③④⑤ | D.②③④⑧ |
您最近一年使用:0次
2024-02-22更新
|
297次组卷
|
2卷引用:山东省青岛市2023-2024学年高二上学期1月期末化学试题
解题方法
3 . 下列各组物质中,所含化学键类型相同的是
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
您最近一年使用:0次
名校
4 . 原子序数依次增大的X、Y、Z、W四种元素形成化合物Z3[W(XY)6],其中X、Y、Z为主族元素。X最外层电子数是内层电子数的两倍,Y的简单气态氢化物能使酚酞溶液变红,W3+的3d轨道电子数为半满。下列说法正确的是
| A.Z和W一定位于同周期 |
| B.原子半径:Z>X>Y |
| C.四种元素基态原子中未成对电子数最多的是Y |
| D.该化合物中含有的化学键类型有:离子键、极性键和非极性键 |
您最近一年使用:0次
名校
5 . 青蒿素(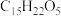 ,
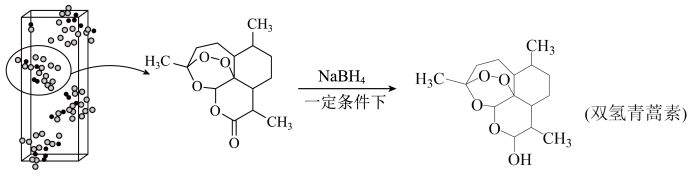
,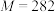 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体)及分子结构如下图所示。下列说法错误的是
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体)及分子结构如下图所示。下列说法错误的是
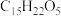 ,
, )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体)及分子结构如下图所示。下列说法错误的是
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体)及分子结构如下图所示。下列说法错误的是
| A.青蒿素分子中既有极性键又有非极性键 |
| B.双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好 |
C.若图中晶胞的棱长分别为 、 、 、 、 ,晶体的密度为 ,晶体的密度为 |
| D.利用红外光谱法测定原子的空间位置、原子间存在的化学键及键长和键角 |
您最近一年使用:0次
2023-09-07更新
|
237次组卷
|
2卷引用:山东省新高考联合质量测评2023-2024学年高三上学期开学考试化学试题
名校
解题方法
6 . 将CO合成甲醇是实现“碳达峰、碳中和”的一项重要措施,在此过程中可能涉及以下物质:
①H2②O2③CO④He⑤H2O2⑥Na2O2⑦KOH⑧CH3OH⑨K2CO3
请判断:
(1)含有极性共价键的离子化合物有___________ (填编号)。
(2)含有非极性共价键的共价化合物有___________ (填编号)。
(3)在实验室中模拟CO合成甲醇的反应,在2L密闭容器内,400℃时发生反应:CO(g)+2H2(g)⇌CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
已知每生成1molCH3OH(g),放出的热量为116kJ。计算上述反应达到平衡时放出的热量Q=___________ kJ(保留2位有效数字)。
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2 +6H2O。则电池放电时通入空气的电极为
+6H2O。则电池放电时通入空气的电极为___________ (“正”或“负”)极;从电极反应来看,每消耗1molCH3OH转移的电子数为___________ NA。
①H2②O2③CO④He⑤H2O2⑥Na2O2⑦KOH⑧CH3OH⑨K2CO3
请判断:
(1)含有极性共价键的离子化合物有
(2)含有非极性共价键的共价化合物有
(3)在实验室中模拟CO合成甲醇的反应,在2L密闭容器内,400℃时发生反应:CO(g)+2H2(g)⇌CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CH3OH)(mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2
 +6H2O。则电池放电时通入空气的电极为
+6H2O。则电池放电时通入空气的电极为
您最近一年使用:0次
2023-08-10更新
|
219次组卷
|
2卷引用:山东省济南市2022-2023学年高一下学期期中考试化学试题
名校
解题方法
7 . 下列说法有几项是正确的
①质子数相同的粒子一定属于同一种元素
②含金属元素的离子可能是阴离子
③化学键可存在于相邻的原子之间,也可存在于相邻的分子之间
④某化合物在水溶液中能导电,可以证明该化合物内一定存在离子键
⑤两种非金属元素形成AB型化合物,它一定含共价键
⑥物质中化学键被破坏,一定发生化学变化
⑦氢氟酸贮存在细口玻璃瓶里
①质子数相同的粒子一定属于同一种元素
②含金属元素的离子可能是阴离子
③化学键可存在于相邻的原子之间,也可存在于相邻的分子之间
④某化合物在水溶液中能导电,可以证明该化合物内一定存在离子键
⑤两种非金属元素形成AB型化合物,它一定含共价键
⑥物质中化学键被破坏,一定发生化学变化
⑦氢氟酸贮存在细口玻璃瓶里
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
2023-08-10更新
|
151次组卷
|
2卷引用:山东省实验中学2022-2023学年高一下学期3月月考化学试题
8 .  为白色结晶粉末,熔点为
为白色结晶粉末,熔点为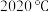 。用
。用 做电极材料,通过光电解可将
做电极材料,通过光电解可将 和
和 催化合成
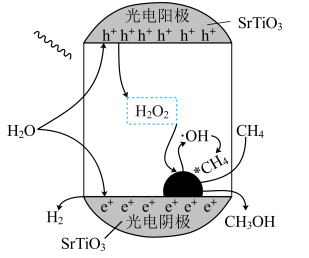
催化合成 ,其工作原理如图所示,下列说法不正确的是
,其工作原理如图所示,下列说法不正确的是
 为白色结晶粉末,熔点为
为白色结晶粉末,熔点为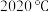 。用
。用 做电极材料,通过光电解可将
做电极材料,通过光电解可将 和
和 催化合成
催化合成 ,其工作原理如图所示,下列说法不正确的是
,其工作原理如图所示,下列说法不正确的是
A. 的晶体类型为离子晶体 的晶体类型为离子晶体 |
B.羟基自由基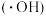 的电子式为 的电子式为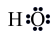 |
C.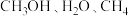 均为极性分子 均为极性分子 |
| D.反应过程中有极性键和非极性键的断裂与形成 |
您最近一年使用:0次
9 . 元素X、Y、Z、M、N、R均为短周期主族元素,且原子序数依次增大。X与Y可形成原子个数比为 的18电子分子A,X与Z可形成原子个数比为
的18电子分子A,X与Z可形成原子个数比为 的18电子分子B,M、N、R的最高价氧化物对应的水化物两两之间可以发生反应,
的18电子分子B,M、N、R的最高价氧化物对应的水化物两两之间可以发生反应, 常用作漂白剂、防腐剂、抗氧化剂。回答下列问题:
常用作漂白剂、防腐剂、抗氧化剂。回答下列问题:
(1)R在元素周期表中的位置为___________ 。
(2)R、Z、M、N的简单离子半径由大到小的顺序为___________ 。(填离子符号)。
(3)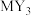 常用作汽车安全气囊的气体发生剂,该化合物中所含化学键的类型为
常用作汽车安全气囊的气体发生剂,该化合物中所含化学键的类型为___________ 。
(4)M、N的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(5)A能与B反应生成无毒气体,该反应的化学方程式为___________ 。
 的18电子分子A,X与Z可形成原子个数比为
的18电子分子A,X与Z可形成原子个数比为 的18电子分子B,M、N、R的最高价氧化物对应的水化物两两之间可以发生反应,
的18电子分子B,M、N、R的最高价氧化物对应的水化物两两之间可以发生反应, 常用作漂白剂、防腐剂、抗氧化剂。回答下列问题:
常用作漂白剂、防腐剂、抗氧化剂。回答下列问题:(1)R在元素周期表中的位置为
(2)R、Z、M、N的简单离子半径由大到小的顺序为
(3)
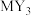 常用作汽车安全气囊的气体发生剂,该化合物中所含化学键的类型为
常用作汽车安全气囊的气体发生剂,该化合物中所含化学键的类型为(4)M、N的最高价氧化物对应的水化物反应的离子方程式为
(5)A能与B反应生成无毒气体,该反应的化学方程式为
您最近一年使用:0次
10 . 过氧化氢( )溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。
)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。 与
与 反应生成
反应生成 ,
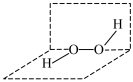
, 的分子结构如图所示。下列说法正确的是
的分子结构如图所示。下列说法正确的是
 )溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。
)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。 与
与 反应生成
反应生成 ,
, 的分子结构如图所示。下列说法正确的是
的分子结构如图所示。下列说法正确的是
A.过氧化氢的电子式为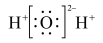 |
B. 为含有极性键和非极性键的共价化合物 为含有极性键和非极性键的共价化合物 |
C. 既有氧化性又有还原性 既有氧化性又有还原性 |
D. 与 与 反应过程中有共价键断裂,同时有共价键和离子键形成 反应过程中有共价键断裂,同时有共价键和离子键形成 |
您最近一年使用:0次
2023-07-12更新
|
140次组卷
|
2卷引用: 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末考试化学模拟卷(二)



