1 . 已知 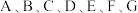 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和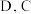 和
和  为同一主族元素,A与
为同一主族元素,A与 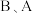 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是_____________ ,画出其原子结构示意图:_________________ .
(2)元素 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为_____________________________ 。
(3)元素B的最低价氢化物的电子式为_____________________ 。
(4)由 所形成的常见离子化合物是
所形成的常见离子化合物是_____________ (写化学式),其所含化学键类型为_____________ 。
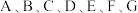 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和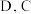 和
和  为同一主族元素,A与
为同一主族元素,A与 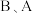 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:(1)七种元素中,非金属性最强的元素在周期表中的位置是
(2)元素
 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为(3)元素B的最低价氢化物的电子式为
(4)由
 所形成的常见离子化合物是
所形成的常见离子化合物是
您最近一年使用:0次
2 . 短周期主族元素  的原子序数依次增大,
的原子序数依次增大, 原子的最外层电子数是其内层电子数的2倍,Y和W同主族,
原子的最外层电子数是其内层电子数的2倍,Y和W同主族, 与
与 有相同的电子层结构,下列说法正确的是
有相同的电子层结构,下列说法正确的是
 的原子序数依次增大,
的原子序数依次增大, 原子的最外层电子数是其内层电子数的2倍,Y和W同主族,
原子的最外层电子数是其内层电子数的2倍,Y和W同主族, 与
与 有相同的电子层结构,下列说法正确的是
有相同的电子层结构,下列说法正确的是A.原子半径大小顺序: |
B. 的最高价氧化物对应水化物的酸性比W的弱 的最高价氧化物对应水化物的酸性比W的弱 |
C.Y分别与 、W形成的化合物中化学键类型相同 、W形成的化合物中化学键类型相同 |
| D.W单质的熔点比Y的低 |
您最近一年使用:0次
解题方法
3 . 下列说法错误的是
| A.离子化合物可能含共价键 |
B. 是共价化合物 是共价化合物 |
| C.只由非金属元素形成的化合物不可能是离子化合物 |
| D.稀有气体分子中不存在化学键 |
您最近一年使用:0次
解题方法
4 . 胍(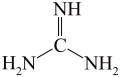 )是一元强碱,分子构型为平面型,其盐酸盐(
)是一元强碱,分子构型为平面型,其盐酸盐(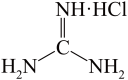 )是核酸检测液的主要成分。下列说法错误的是
)是核酸检测液的主要成分。下列说法错误的是
 )是一元强碱,分子构型为平面型,其盐酸盐(
)是一元强碱,分子构型为平面型,其盐酸盐( )是核酸检测液的主要成分。下列说法错误的是
)是核酸检测液的主要成分。下列说法错误的是| A.胍中C、N杂化方式均为sp2 | B.胍具有很强的吸湿性 |
| C.胍的熔点低于胍盐 | D.胍盐中含有的化学键均为极性键 |
您最近一年使用:0次
5 . 下列说法中不正确的是
A. 晶体溶于水时,离子键被破坏,共价键不受影响 晶体溶于水时,离子键被破坏,共价键不受影响 |
| B.“天宫课堂”中过饱和乙酸钠溶液析晶放热与形成新的化学键有关 |
| C.将熔融状态下的HCl和NaCl进行导电性实验可证明HCl由共价键形成而NaCl由离子键形成 |
| D.H元素与其他元素化合可能形成共价化合物也可能形成离子化合物 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.非金属元素组成的化合物一定是共价化合物 |
| B.共价化合物中一定只含有极性共价键 |
| C.离子化合物一定含有离子键 |
| D.一种金属元素与一种非金属元素一定能形成离子化合物 |
您最近一年使用:0次
7 .  的发现导致了一门新兴学科一碳球化学的兴起。
的发现导致了一门新兴学科一碳球化学的兴起。 与碱金属形成的一类化合物在低温下具有超导性能。其中
与碱金属形成的一类化合物在低温下具有超导性能。其中 与金属钾形成的化合物晶胞如图所示,下列说法不正确的是
与金属钾形成的化合物晶胞如图所示,下列说法不正确的是

 的发现导致了一门新兴学科一碳球化学的兴起。
的发现导致了一门新兴学科一碳球化学的兴起。 与碱金属形成的一类化合物在低温下具有超导性能。其中
与碱金属形成的一类化合物在低温下具有超导性能。其中 与金属钾形成的化合物晶胞如图所示,下列说法不正确的是
与金属钾形成的化合物晶胞如图所示,下列说法不正确的是
| A.该化合物中既有离子键又有共价键 |
B.该晶胞的棱上有12个 ,内部有9个 ,内部有9个 |
C.该晶体中与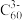 等距且最近的 等距且最近的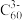 共12个 共12个 |
D.该化合物的熔点比 与金属铯形成的类似化合物的熔点低 与金属铯形成的类似化合物的熔点低 |
您最近一年使用:0次
解题方法
8 . 离子液体具有良好的化学稳定性、较低的熔点以及对多种物质有良好的溶解性,因此应用广泛,1-乙基-3-甲基咪唑四氟硼酸盐的结构如图:
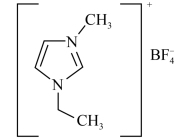
下列说法不正确的是

下列说法不正确的是
| A.五元环上的C、N均是sp2杂化 |
B.阳离子的化学式为 |
| C.该离子液体中存在的化学键类型:离子键、共价键、配位键 |
| D.阴离子的空间构型为正四面体 |
您最近一年使用:0次
9 . 氯化钠来自海水,工业上通过提纯 进一步获得钠单质和化合物,转化关系如图。下列说法正确的是
进一步获得钠单质和化合物,转化关系如图。下列说法正确的是
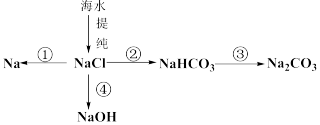
 进一步获得钠单质和化合物,转化关系如图。下列说法正确的是
进一步获得钠单质和化合物,转化关系如图。下列说法正确的是
| A.提纯过程主要涉及过滤、结晶、蒸馏等操作 |
| B.上述转化中只有反应①属于氧化还原反应 |
| C.反应②所得副产物中既含离子键又含共价键 |
| D.实验室可用氢氧化钙鉴别碳酸钠和碳酸氢钠 |
您最近一年使用:0次
2021-11-10更新
|
231次组卷
|
2卷引用:山东省德州市2021-2022学年高三上学期期中化学考试试题
10 . 短周期主族元素W、E、X、Y的原子序数依次增大,它们位于三个不同的周期,E和X同周期。由E、X、Y组成的一种化合物——百菌清(M),是一种广谱保护性杀菌剂,结构式如图所示。下列说法错误的是
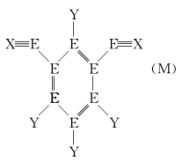

| A.M属于共价化合物 |
B.常温下,最简单氢化物在水中的溶解性: |
| C.Y的最高价氧化物对应的水化物是弱酸 |
| D.W、X、Y只能形成共价化合物 |
您最近一年使用:0次



