名校
1 . 表中①~⑥为短周期元素及相应部分原子半径的数据。下列说法正确的是
| 元素性质 | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径/nm | a | 0.075 | b | 0.110 | c | d |
| 最高化合价 | +6 | +5 | +5 | +7 | ||
| 最低化合价 | -2 | -3 | -2 | -3 | -1 | -1 |
| A.原子半径:a>d>b>c |
| B.元素①的最外层电子排布为2s22p4 |
| C.元素②氢化物与元素⑥氢化物反应形成化合物中只有价键 |
D.非金属性:元素⑤ 元素④ 元素④ 元素① 元素① |
您最近一年使用:0次
名校
解题方法
2 . 下列说法不正确的是
| A.离子化合物和金属单质的构成粒子中均含有阳离子 |
| B.离子键和金属键本质上都是静电作用,都没有方向性和饱和性 |
| C.熔点:MgO>NaCl>Hg>HBr |
| D.NaHSO4在水溶液中和熔融状态下都能导电,电离方程式相同 |
您最近一年使用:0次
2023-12-30更新
|
263次组卷
|
4卷引用:福建省三明市第一中学2023-2024学年高二下学期3月月考化学试题
福建省三明市第一中学2023-2024学年高二下学期3月月考化学试题北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷(已下线)3.3.1 金属晶体 离子晶体(提高)(已下线)题型突破05 结构化学基本概念和图示题-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(北京专用)
名校
3 . 《天工开物》中记载了中国古代火法炼锌的工艺,将炉甘石和煤炭饼在高温条件下反应可制得倭铅(即锌单质),反应的化学方程式可表示为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.该反应为置换反应 |
| B.CO只是氧化产物 |
C. 晶体中既含有离子键又含有共价键 晶体中既含有离子键又含有共价键 |
D.锌的基态原子外围电子排布式为 |
您最近一年使用:0次
2023-12-21更新
|
200次组卷
|
3卷引用:福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
4 . 下列说法中正确的是
| A.NH3和BF3分子中所有原子的最外层都达到了8电子稳定结构 |
| B.Na2O2、NaClO中所含化学键类型完全相同 |
| C.等物质的量的CaC2和NaCN中含有的共用电子对数不相等 |
| D.汽车防撞气囊中的NaN3分解:2NaN3=2Na+3N2↑有离子键、共价键的断裂,有金属键、共价键的形成 |
您最近一年使用:0次
名校
5 . 用下图表示的一些物质或概念间的从属头系中不正确的是
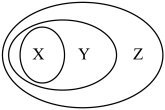

| X | Y | Z | |
| A | 极性键 | 共价键 | 化学键 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 离子化合物 | 化合物 |
| D | 氧化物 | 化合物 | 纯净物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列关于晶体的说法正确的组合是
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、 、
、 晶体的熔点依次降低
晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤ 晶体中每个硅原子与四个氧原子以共价键相结合
晶体中每个硅原子与四个氧原子以共价键相结合
⑥共价键的极性由强到弱: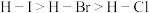
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、
 、
、 晶体的熔点依次降低
晶体的熔点依次降低④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤
 晶体中每个硅原子与四个氧原子以共价键相结合
晶体中每个硅原子与四个氧原子以共价键相结合⑥共价键的极性由强到弱:
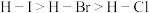
| A.①②⑥ | B.①②④ | C.③⑤⑥ | D.③⑤ |
您最近一年使用:0次
2023-04-25更新
|
277次组卷
|
2卷引用:福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
名校
7 . SiCl4可发生水解反应,机理如图:
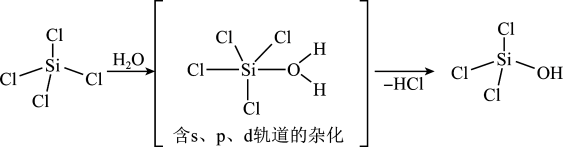
下列说法错误的是

下列说法错误的是
| A.将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液体流不会发生偏转 |
| B.中间体SiCl4(H2O)中Si采取的杂化类型可能为sp3d杂化 |
| C.SiCl4水解最终可生成H4SiO4 |
| D.中间体SiCl4(H2O)生成的过程中有极性键的断裂与生成 |
您最近一年使用:0次
2023-03-17更新
|
362次组卷
|
4卷引用:福建省莆田第一中学2022-2023学年高二下学期第二学段(期中)考试化学试题
名校
解题方法
8 .  为乙二胺四乙酸
为乙二胺四乙酸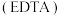 ,易与金属离子形成配合物。
,易与金属离子形成配合物。 为
为 与
与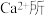 形成。下列叙述正确的是
形成。下列叙述正确的是

 为乙二胺四乙酸
为乙二胺四乙酸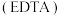 ,易与金属离子形成配合物。
,易与金属离子形成配合物。 为
为 与
与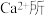 形成。下列叙述正确的是
形成。下列叙述正确的是
| A.b含有分子内氢键 | B.b中 的配位数为 的配位数为 |
C.a和b中的 原子均为 原子均为  杂化 杂化 | D.b含有共价键、离子键和配位键 |
您最近一年使用:0次
2023-02-17更新
|
401次组卷
|
11卷引用:2015-2016学年福建省厦门市高二上学期期末质检化学试卷
2015-2016学年福建省厦门市高二上学期期末质检化学试卷福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题福建省厦门市湖滨中学2018-2019学年高二(理)上学期期中考试化学试题福建省厦门市思明区厦门外国语学校2019-2020学年高二上学期周末练习10——化学试题天津市耀华中学2020-2021学年高二下学期期中检测化学试题山西省朔州市怀仁市2020-2021学年高二下学期期末考试化学试题湖北省罗田县第一中学2021-2022学年高二下学期6月月考化学试题(实验班)江西省景德镇一中2022-2023学年高二下学期期中考试(19班)化学试题湖北省当阳市第一高级中学2022-2023学年高三上学期期中考试化学试题(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(选择题11-13)江西省宜春市宜丰中学2022-2023学年高三下学期3月月考化学试题
解题方法
9 . 1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)预测周期表中电负性最大的元素应为_______ ;估计钙元素的电负性的取值范围:_______ <X<_______ 。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为_______ 。
(3)请你预测Br与I元素的X数值的大小关系:X(Br)_______ X(I)。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_______ 原子(填元素符号)。
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是_______ ;
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:_______ 。
(7)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
(3)请你预测Br与I元素的X数值的大小关系:X(Br)
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:
(7)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
您最近一年使用:0次
名校
10 . 设NA表示阿伏加德罗常数的数值,下列对应关系正确 的是
| A.14gC2H4和C3H6的混合物含2NA个共用电子对 |
| B.6gH2与过量的N2反应生成的NH3的数目为2NA |
| C.标准状况下,11.2LCCl4中含有原子的数目为2.5NA |
D.0.5mol 分子中极性键数目为4NA 分子中极性键数目为4NA |
您最近一年使用:0次
2022-03-28更新
|
79次组卷
|
2卷引用:福建省厦门外国语学校石狮分校2021-2022学年高二下学期3月月考化学试题



