名校
解题方法
1 . 下列描述正确的是
| A.14g14C中质子数目为8NA |
B.0.1mol/L1L酸性重铬酸钾溶液中 数目为0.1NA 数目为0.1NA |
| C.1mol石墨晶体中形成六元环的数目为0.5NA |
D.142gP4O10( )中含9NA个σ键 )中含9NA个σ键 |
您最近一年使用:0次
2 . NaOH活化过的 催化剂对甲醛氧化为
催化剂对甲醛氧化为 具有较好的催化效果,有学者提出该催化反应的机理如下。下列说法不正确的是
具有较好的催化效果,有学者提出该催化反应的机理如下。下列说法不正确的是
 催化剂对甲醛氧化为
催化剂对甲醛氧化为 具有较好的催化效果,有学者提出该催化反应的机理如下。下列说法不正确的是
具有较好的催化效果,有学者提出该催化反应的机理如下。下列说法不正确的是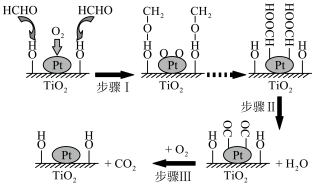
| A.步骤Ⅰ中存在非极性键的断裂 |
| B.步骤Ⅰ可理解为HCHO中带部分负电荷的O与催化剂表面的-OH发生作用 |
C.步骤Ⅱ中发生的反应可表示为 |
| D.该催化剂对苯的催化氧化效果优于对HCHO的催化氧化效果 |
您最近一年使用:0次
名校
3 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案 | 现象 | 结论 |
| A | 比较H2CO3和HClO的酸性强弱 | 用pH试纸测同浓度NaHCO3溶液和NaClO溶液的pH | NaClO溶液的pH比较大 | H2CO3的酸性强于HClO |
| B | 比较AgI与Ag2S的Ksp | 向2mL0.1mol/LAgNO3溶液中滴加2滴同浓度KI溶液,然后再滴加2滴同浓度的K2S溶液 | 先产生淡黄色沉淀,后出现黑色沉淀 | Ksp(AgI)>Ksp(Ag2S) |
| C | 判断AlCl3中化学键类型 | 将AlCl3固体溶于水,测溶液导电性 | 溶液能导电 | AlCl3中为离子键 |
| D | 比较Mg与Al的金属性 | 分别向MgCl2和AlCl3溶液中滴加足量的NaOH溶液 | 前者产生白色沉淀;后者先产生白色沉淀,后沉淀溶解 | 金属性:Mg>Al |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W、Z位于同主族,W、Z组成的一种二元化合物可作为漂白剂,Y的原子半径在短周期主族元素原子中最大。下列有关说法错误的是
A. 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 |
B.X的单质可直接与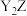 水溶液发生反应得到单质Z 水溶液发生反应得到单质Z |
| C.Y与Z形成的二元化合物中可能含有共价键 |
| D.W、Y、Z组成的化合物M与稀硫酸反应得到Z的单质和氧化物 |
您最近一年使用:0次
5 . 钛酸钡粉体是电子陶瓷元器件的重要基础原料。钛酸钡晶体与 的结构如图。
的结构如图。
 的结构如图。
的结构如图。
| A.钛酸钡晶体中Ba和Ti的配位数分别为12和6 |
B. 中含有的化学键为离子键、共价键、氢键、配位键 中含有的化学键为离子键、共价键、氢键、配位键 |
C. 中Ti的杂化方式为 中Ti的杂化方式为 |
D.1mol  通过螯合作用形成的配位键有5mol 通过螯合作用形成的配位键有5mol |
您最近一年使用:0次
6 . 研究发现Pt基催化剂载体表面的晶格氧可提高催化活性,甲醛在Pt基催化剂表面催化氧化的机理如图所示。下列说法错误的是
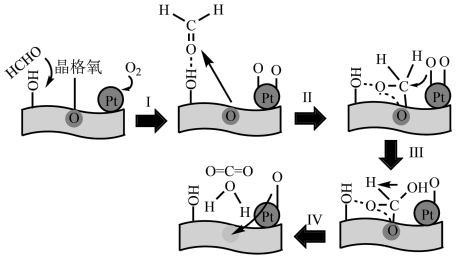
A.HCOOH、HCHO和 均为极性分子 均为极性分子 |
| B.反应中涉及氢键、非极性键和极性键的断裂 |
| C.催化中心的Pt的化合价发生变化 |
D.若将 替换为 替换为 ,则产物中含有 ,则产物中含有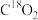 |
您最近一年使用:0次
名校
解题方法
7 . 下列物质含共价键的强电解质是
A. | B. | C. | D. |
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
8 . X、Y、Z、W为原子序数依次增大的短周期主族元素,原子序数之和为37。四种元素所形成的常见单质有三种在常温下为气体,在一定条件下,Z与X、Y、W均能形成原子个数比为1∶1的离子化合物。下列说法错误的是
| A.Y的简单氢化物在同主族元素中稳定性最强 |
| B.Y、Z所形成的物质中可能含不同种化学键 |
| C.简单离子半径:W>Z>Y>X |
| D.由X、Y两种元素组成的含18电子的分子能使酸性KMnO4溶液褪色 |
您最近一年使用:0次
9 .  是一种可吸附甲醇的材料,R、T、X、Y、Z为原子序数依次递增且为不同主族的短周期非金属元素,T、X、Y、Z位于同一周期且相邻,其中
是一种可吸附甲醇的材料,R、T、X、Y、Z为原子序数依次递增且为不同主族的短周期非金属元素,T、X、Y、Z位于同一周期且相邻,其中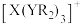 结构如图。下列说法一定正确的是
结构如图。下列说法一定正确的是
 是一种可吸附甲醇的材料,R、T、X、Y、Z为原子序数依次递增且为不同主族的短周期非金属元素,T、X、Y、Z位于同一周期且相邻,其中
是一种可吸附甲醇的材料,R、T、X、Y、Z为原子序数依次递增且为不同主族的短周期非金属元素,T、X、Y、Z位于同一周期且相邻,其中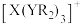 结构如图。下列说法一定正确的是
结构如图。下列说法一定正确的是
A.第一电离能: |
B.含氧酸的酸性: |
C.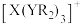 中X、Y原子均满足8电子稳定结构 中X、Y原子均满足8电子稳定结构 |
| D.该物质中含有离子键、配位键和极性键 |
您最近一年使用:0次
解题方法
10 . 下列物质只含有共价键且其水溶液显酸性的是
| A.HCl | B. | C. | D. |
您最近一年使用:0次



