解题方法
1 . 人体必需的一些元素在周期表中的分布情况如下:
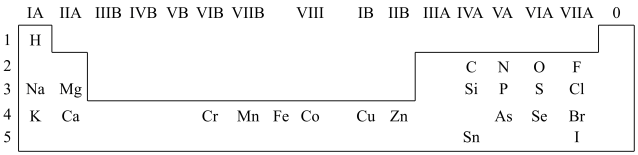
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
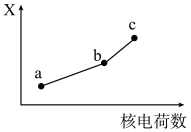
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
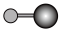 | 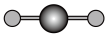 | 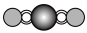 | 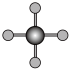 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
名校
2 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。下列说法正确的是


| A.D中含有的化学键类型只有离子键 |
| B.将E溶液滴入碳酸氢钠溶液中,有大量气泡产生 |
| C.A、B、C均属于电解质 |
| D.C的酸性和氧化性均强于E |
您最近一年使用:0次
解题方法
3 . 现有下列六种物质:
① ②过氧化钠 ③
②过氧化钠 ③ ④
④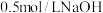 溶液 ⑤碳酸氢钠 ⑥
溶液 ⑤碳酸氢钠 ⑥ 。请根据上述物质回答下列问题:
。请根据上述物质回答下列问题:
(1)在上述物质中属于酸性氧化物的有___________ (填①~⑥序号)。
(2)含有 氧原子的②与足量①反应,产生的气体在标准状况下的体积为
氧原子的②与足量①反应,产生的气体在标准状况下的体积为___________ L。
(3)写出⑥在水溶液中的电离方程式___________ 。
(4)②所含化学键类型为___________ 。
(5)某同学帮助水质检测站配制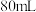 ④以备使用。
④以备使用。
①该同学应用托盘天平称取 固体
固体___________ g。
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、___________ 。
③定容时仰视刻度线,则所配制的溶液的浓度会___________ (填“偏高”、“偏低”、“不变”)。
(6)④和⑤的溶液混合,发生反应的离子方程式为___________ 。
①
 ②过氧化钠 ③
②过氧化钠 ③ ④
④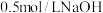 溶液 ⑤碳酸氢钠 ⑥
溶液 ⑤碳酸氢钠 ⑥ 。请根据上述物质回答下列问题:
。请根据上述物质回答下列问题:(1)在上述物质中属于酸性氧化物的有
(2)含有
 氧原子的②与足量①反应,产生的气体在标准状况下的体积为
氧原子的②与足量①反应,产生的气体在标准状况下的体积为(3)写出⑥在水溶液中的电离方程式
(4)②所含化学键类型为
(5)某同学帮助水质检测站配制
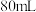 ④以备使用。
④以备使用。①该同学应用托盘天平称取
 固体
固体②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
③定容时仰视刻度线,则所配制的溶液的浓度会
(6)④和⑤的溶液混合,发生反应的离子方程式为
您最近一年使用:0次
名校
4 . 一定条件下,氨与氟气发生反应: 。其中NF₃结构与
。其中NF₃结构与 相似。下列有关说法错误的是
相似。下列有关说法错误的是
 。其中NF₃结构与
。其中NF₃结构与 相似。下列有关说法错误的是
相似。下列有关说法错误的是A.上述反应,当有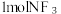 生成时,共转移6mol电子 生成时,共转移6mol电子 |
B.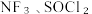 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 |
| C.NF₃中只含极性共价键 |
| D.NH₄F中既含有离子键又含有共价键 |
您最近一年使用:0次
名校
解题方法
5 . 很多含巯基(―SH)的有机化合物是重金属元素汞的解毒剂,如化合物Ⅰ、Ⅱ(结构如图)。下列说法正确的是
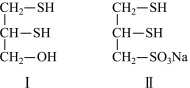

| A.在两个化合物中S原子均采取sp2杂化 |
| B.在两个化合物中C―C―C键角均是180° |
| C.两个化合物均为共价化合物 |
| D.化合物Ⅱ的水溶性好于化合物Ⅰ |
您最近一年使用:0次
名校
6 . 按要求完成下列填空。
I.下列物质:① ②
② ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
(1)含有共价键的离子化合物是___________ (填序号,下同)。
(2)属于共价化合物是___________ 。
(3)只含有非极性键的物质是___________ 。
(4)写出①的结构式___________ ,写出⑥的电子式___________ 。
II.下列变化:①蔗糖溶于水② 升华③烧碱熔化④NaCl溶解⑤
升华③烧碱熔化④NaCl溶解⑤ 溶解⑥硫酸氢钾溶于水
溶解⑥硫酸氢钾溶于水
(5)只有离子键被破坏的是___________ 。
(6)只有共价键被破坏的是___________ 。
(7)只破坏分子间作用力的是___________ 。
I.下列物质:①
 ②
② ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
(1)含有共价键的离子化合物是
(2)属于共价化合物是
(3)只含有非极性键的物质是
(4)写出①的结构式
II.下列变化:①蔗糖溶于水②
 升华③烧碱熔化④NaCl溶解⑤
升华③烧碱熔化④NaCl溶解⑤ 溶解⑥硫酸氢钾溶于水
溶解⑥硫酸氢钾溶于水(5)只有离子键被破坏的是
(6)只有共价键被破坏的是
(7)只破坏分子间作用力的是
您最近一年使用:0次
2024-02-07更新
|
263次组卷
|
2卷引用:甘肃省兰州第一中学2023-2024学年高一上学期1月期末化学试题
解题方法
7 . 下列化学用语或表述正确的是
A. 的空间结构名称:三角锥形 的空间结构名称:三角锥形 |
B.铝原子的结构示意图为: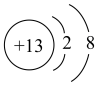 |
| C.基态硅原子的价层电子排布:1s22s22p63s23p2 |
| D.P4中的共价键类型:非极性键 |
您最近一年使用:0次
8 . 氯碱工业的原理为: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 的结构示意图: 的结构示意图: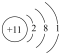 | B. 的空间填充模型: 的空间填充模型: |
C. 中既有离子键也有共价键 中既有离子键也有共价键 | D. 的电子式: 的电子式: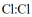 |
您最近一年使用:0次
解题方法
9 . 下列各组物质中,所含化学键类型相同的是
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
您最近一年使用:0次
10 . 用某硫铜矿煅烧后的废渣(主要含 )为原料制取
)为原料制取 ,操作如下:
,操作如下:
步骤一:粉碎废渣,将其投入到适量稀硫酸中,搅拌使其充分反应.
步骤二:向得到的混合物中加入适量 溶液,充分反应后调节
溶液,充分反应后调节 ,使
,使 完全沉淀.过滤得到
完全沉淀.过滤得到 溶液.
溶液.
步骤三:向 溶液中加入适量
溶液中加入适量 溶液和
溶液和 溶液,控制
溶液,控制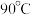 使其充分反应,过程中有
使其充分反应,过程中有 生成.过滤、洗涤、干燥,得到
生成.过滤、洗涤、干燥,得到 .
.
下列说法不正确 的是

 )为原料制取
)为原料制取 ,操作如下:
,操作如下:步骤一:粉碎废渣,将其投入到适量稀硫酸中,搅拌使其充分反应.
步骤二:向得到的混合物中加入适量
 溶液,充分反应后调节
溶液,充分反应后调节 ,使
,使 完全沉淀.过滤得到
完全沉淀.过滤得到 溶液.
溶液.步骤三:向
 溶液中加入适量
溶液中加入适量 溶液和
溶液和 溶液,控制
溶液,控制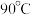 使其充分反应,过程中有
使其充分反应,过程中有 生成.过滤、洗涤、干燥,得到
生成.过滤、洗涤、干燥,得到 .
.下列说法

| A.步骤一中粉碎废渣且溶解时搅拌,可加快溶解的速率 |
B. 分子中的共价键既有极性键又有非极性键 分子中的共价键既有极性键又有非极性键 |
C.步骤三中消耗的 的物质的量之比为 的物质的量之比为 |
D. 的一种晶胞结构如题8图所示,其中“ 的一种晶胞结构如题8图所示,其中“ ”表示氧 ”表示氧 |
您最近一年使用:0次



