名校
1 . 一种用于合成治疗免疫疾病药物的物质,其结构如图所示,其中X、Y,Z、Q、W为1~20号元素且原子序数依次增大,Z与Q同主族,Q和W的简单离子具有相同的电子层结构。下列叙述错误的是
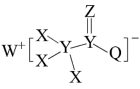
| A.上述物质中除X外均达到8电子稳定结构 |
| B.最高价氧化物对应的水化物的酸性:Q>Y |
| C.W与X、Z、Q形成的化合物中化学键类型均相同 |
| D.Z和X、Y、W、Q均形成至少两种二元化合物 |
您最近一年使用:0次
2 . 下列有关说法正确的是
A.古壁画颜料中的铁红,其主要成分是 |
| B.漂白粉、冰水混合物都是混合物 |
| C.火焰中的红色来源于钠盐的燃烧 |
| D.任何物质均含有化学键 |
您最近一年使用:0次
3 . 化学助力蓝天保卫战。工业上可利用氨水吸收SO2尾气,生成NH4HSO3,再将其氧化得到(NH4)2SO4化肥。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LNH3所含的分子数目为NA |
| B.64gSO2中所含的σ键数目为2NA |
C.2mol 完全氧化生成 完全氧化生成 ,转移的电子数目为2NA ,转移的电子数目为2NA |
D.1L0.1mol/L(NH4)2SO4溶液中所含的 数目为0.2NA 数目为0.2NA |
您最近一年使用:0次
4 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近一年使用:0次
5 . Ⅰ.食品添加剂能改善食物色香味、延长保质期、调整营养结构。我国对食品添加剂的品种、适用范围、最大用量及残留量都制定了严格的标准。
(1)下列关天食品添加剂的说法正确的是________ 。
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为________ 。
(3)与SO2所含化学键类型相同的是________。
(4)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是________(双选)。
(5)保鲜时若SO2不慎用量过大,会使水果表面明显褪色,上述现象说明SO2________ 。
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。
已知:ω(SO2残留量) =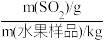 。
。
(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标______ (写出计算过程)。
(1)下列关天食品添加剂的说法正确的是
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为
(3)与SO2所含化学键类型相同的是________。
| A.NH4Cl | B.CaCl2 | C.AlCl3 | D.NaOH |
| A.热稳定性:H2S>SiH4 | B.溶解度:SO2> SiO2 |
| C.单质的熔点:Si > S | D.酸性:H2SO4> H2SiO3 |
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、
 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。已知:ω(SO2残留量) =
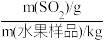 。
。(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标
您最近一年使用:0次
解题方法
6 . 一种工业用缓冲剂由前四周期原子序数依次递增、且在不同周期的X、Y、Z、W四种元素组成,结构如图所示。已知Z的单质常温下为固体。下列说法正确的是
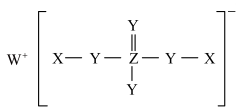
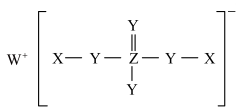
| A.Y元素的非金属性强于与Z同族短周期元素的非金属性 |
B.简单氢化物的沸点: |
| C.该化合物中所有原子均满足8电子稳定结构 |
| D.Y和W不可能形成既含有离子键又含有共价键的化合物 |
您最近一年使用:0次
7 . 实验室用电石(主要成分为 )与水反应制备的
)与水反应制备的 中混有
中混有 ,可用
,可用 溶液净化,反应的化学方程式为
溶液净化,反应的化学方程式为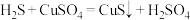 。下列说法正确的是
。下列说法正确的是
 )与水反应制备的
)与水反应制备的 中混有
中混有 ,可用
,可用 溶液净化,反应的化学方程式为
溶液净化,反应的化学方程式为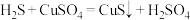 。下列说法正确的是
。下列说法正确的是A. 仅含有离子键 仅含有离子键 | B. 中碳原子的杂化轨道类型为 中碳原子的杂化轨道类型为 |
C. 中心原子上有孤电子对 中心原子上有孤电子对 | D.上述反应原理为强酸制备弱酸 |
您最近一年使用:0次
名校
解题方法
8 .  是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是
 是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是A.该化合物中 的中心原子的杂化轨道类型为 的中心原子的杂化轨道类型为 |
| B.该化合物中存在的化学键有离子键,共价键,配位键和氢键 |
| C.组成该化合物的元素N、O、S中,第一电离能最大的是N |
D.根据VSEPR模型预测的 的空间结构是正四面体形 的空间结构是正四面体形 |
您最近一年使用:0次
9 . 已知反应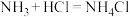 ,下列说法正确的是
,下列说法正确的是
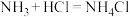 ,下列说法正确的是
,下列说法正确的是| A.离子化合物可能含有共价键 |
| B.该反应只涉及极性共价键的断裂和生成 |
| C.由非金属元素组成的化合物一定是共价化合物 |
D.用电子式表示 的形成为 的形成为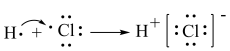 |
您最近一年使用:0次
名校
解题方法
10 . N4分子是一种不稳定的多氮分子,N4分解后产生无毒的氮气并释放出大量能量,可应用于制造推进剂或炸药,N4分子结构如图所示。下列关于N4和N2的说法错误的是
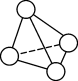

| A.1 mol N4分子含有6 mol N-N键 |
| B.两者互为同素异形体,物理性质不同,化学性质相似 |
| C.相同物质的量的N4和N2所含分子数相等 |
| D.N4是一种新型化合物 |
您最近一年使用:0次



