1 . 下列说法正确的是
| A.物质中一定存在化学键,干冰升华断裂共价键 |
B.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
C.向某溶液中滴加氯水,再滴加 溶液,溶液变成红色,说明溶液中含有 溶液,溶液变成红色,说明溶液中含有 |
D.漂白粉在空气中久置变质的原因是漂白粉中的 与空气中的 与空气中的 反应生成 反应生成 |
您最近半年使用:0次
2 . 已知共价键的极性越强,该共价键在反应中越容易发生断裂,下列事实中不能用上述观点解释的是
A. |
B. |
C.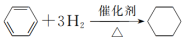 |
D. |
您最近半年使用:0次
解题方法
3 . 作为元素周期律表现形式的元素周期表,反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表中的一部分,请参照以下六种元素(每种字母分别代表一种元素)在表中的位置,回答下列问题:
回答下列问题:
(1)M的原子结构示意图为________ 。
(2)M与Z可形成一种离子化合物 ,其电子式为
,其电子式为________ 。
(3)原子半径:X________ Z(填“大于”或“小于”,下同);简单氢化物的稳定性:Z________ N。
(4)X、Y的最高价氧化物对应水化物的酸性:________ 
________ (填化学式)。
(5)由M和Z组成的一种化合物可用作核潜艇中氧气的来源,该化合物的名称是________ ,其中含有的化学键类型是________ 、________ 。
| 族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | X | Y | Z | |||||
3 | M | N | W |
(1)M的原子结构示意图为
(2)M与Z可形成一种离子化合物
 ,其电子式为
,其电子式为(3)原子半径:X
(4)X、Y的最高价氧化物对应水化物的酸性:

(5)由M和Z组成的一种化合物可用作核潜艇中氧气的来源,该化合物的名称是
您最近半年使用:0次
名校
4 . X、Y、Z、M、Q为五种短周期主族元素,原子序数依次增大。Y元素的最高正价为+4价,Y元素在元素周期表中与Z元素相邻,与M元素同族;化合物 的1个分子中的电子总数为18;Q元素的原子最外层电子数比次外层电子数少1。下列说法错误的是
的1个分子中的电子总数为18;Q元素的原子最外层电子数比次外层电子数少1。下列说法错误的是
 的1个分子中的电子总数为18;Q元素的原子最外层电子数比次外层电子数少1。下列说法错误的是
的1个分子中的电子总数为18;Q元素的原子最外层电子数比次外层电子数少1。下列说法错误的是| A.元素的原子半径:M>Y>Z |
| B.M、Y、Z的简单气态氢化物的稳定性依次增强 |
C. 分子中既有极性共价键又有非极性共价键 分子中既有极性共价键又有非极性共价键 |
| D.X、Z和Q三种元素形成的化合物一定是共价化合物 |
您最近半年使用:0次
2024-02-22更新
|
214次组卷
|
3卷引用:山西省长治市上党好教育联盟2023-2024学年高一上学期1月期末化学试题
解题方法
5 . 阅读下面一段材料,根据所学知识,回答下列问题:
将用砂纸打磨过的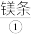 在空气中燃烧,生成
在空气中燃烧,生成 和
和 ,氮化镁溶于水得到
,氮化镁溶于水得到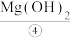 固体和
固体和 ,将Mg(OH)2固体溶于
,将Mg(OH)2固体溶于 ,得到无色溶液,将无色溶液经过一系列操作得到
,得到无色溶液,将无色溶液经过一系列操作得到 ,将
,将 在
在 气流中加热得到
气流中加热得到 。
。
(1)镁在元素周期表中的位置是___________ ,MgCl2中含有的化学键类型为___________ 。
(2)常温下,上述有标号的物质中,能导电的是___________ (填标号,下同),属于电解质的有___________ 。
(3)写出氮化镁固体溶于水发生反应的化学方程式:___________ 。
(4)实验1:将一块金属钠投入MgCl2溶液中,写出发生反应的离子方程式:___________ 。
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量 的稀硫酸中,相同时间内,观察到的现象为
的稀硫酸中,相同时间内,观察到的现象为___________ ,可得出的结论是___________ 。
将用砂纸打磨过的
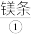 在空气中燃烧,生成
在空气中燃烧,生成 和
和 ,氮化镁溶于水得到
,氮化镁溶于水得到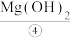 固体和
固体和 ,将Mg(OH)2固体溶于
,将Mg(OH)2固体溶于 ,得到无色溶液,将无色溶液经过一系列操作得到
,得到无色溶液,将无色溶液经过一系列操作得到 ,将
,将 在
在 气流中加热得到
气流中加热得到 。
。(1)镁在元素周期表中的位置是
(2)常温下,上述有标号的物质中,能导电的是
(3)写出氮化镁固体溶于水发生反应的化学方程式:
(4)实验1:将一块金属钠投入MgCl2溶液中,写出发生反应的离子方程式:
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量
 的稀硫酸中,相同时间内,观察到的现象为
的稀硫酸中,相同时间内,观察到的现象为
您最近半年使用:0次
名校
解题方法
6 . 中国传统文化博大精深,蕴含着丰富的化学知识。下列说法错误的是
A.《石灰吟》中记载:“要留清白在人间。”石灰中 的结构示意图为 的结构示意图为 |
B. 和 和 均属于离子化合物 均属于离子化合物 |
| C.“曾青得铁则化为铜”,铁位于元素周期表的第四周期第Ⅷ族 |
| D.“取井火煮之,一斛水得五斗盐”是通过蒸发结晶的方式使氯化钠析出 |
您最近半年使用:0次
2023-12-26更新
|
132次组卷
|
2卷引用:山西运城盐湖五中2023-2024学年高一上学期期末检测化学模拟试卷
名校
解题方法
7 . 下列关于钠及其化合物的说法正确的是
| A.Na2O2与水反应,Na2O2是还原剂,H2O是氧化剂 |
B.新切开的金属钠暴露在空气中,迅速变暗是因为: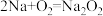 |
| C.Na2O2中阴、阳离子的个数比是1:1 |
| D.将一小块钠投入盛有硫酸铁溶液的烧杯中,既有气体产生又有红褐色沉淀生成 |
您最近半年使用:0次
2023-11-06更新
|
135次组卷
|
4卷引用:山西运城盐湖五中2023-2024学年高一上学期期末检测化学模拟试卷
名校
解题方法
8 . 在抗击新冠病毒中“84消毒液(有效成分是NaClO)”发挥了重要作用。工业上,制备“84消毒液”的原理为:NaCl+H2O NaClO+H2↑。下列说法不正确的是
NaClO+H2↑。下列说法不正确的是
 NaClO+H2↑。下列说法不正确的是
NaClO+H2↑。下列说法不正确的是| A.该反应每转移4mol电子生成149g的NaClO |
| B.NaClO的消毒原理利用了其强氧化性 |
C.NaClO的电子式为 |
| D.上述制备消毒液的反应过程中有离子键、极性共价键的断裂和形成 |
您最近半年使用:0次
2023-09-23更新
|
50次组卷
|
2卷引用:山西运城盐湖五中2023-2024学年高一上学期期末检测化学模拟试卷
名校
解题方法
9 . 设 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.乙醛催化氧化生成1mol乙酸的过程中,断裂的C—H键的数目为 |
B.50mL1 溶液中含有的O原子数为0.1 溶液中含有的O原子数为0.1 |
C.熔融状态下,1mol 中含有的 中含有的 的数目为 的数目为 |
D.标准状况下,5.6L 中含有的 中含有的 键的数目为 键的数目为 |
您最近半年使用:0次
10 . 下列各组晶体中:① 和
和 ②氖晶体和氮气晶体 ③
②氖晶体和氮气晶体 ③ 和
和 ④冰和干冰,化学键类型相同,晶体类型也相同的是
④冰和干冰,化学键类型相同,晶体类型也相同的是
 和
和 ②氖晶体和氮气晶体 ③
②氖晶体和氮气晶体 ③ 和
和 ④冰和干冰,化学键类型相同,晶体类型也相同的是
④冰和干冰,化学键类型相同,晶体类型也相同的是| A.②③④ | B.①③④ | C.③④ | D.②③ |
您最近半年使用:0次
2023-07-15更新
|
64次组卷
|
2卷引用:山西省应县第四中学校2022-2023学年高二下学期7月期末考试化学试题



