1 . 硅原子核外电子运动状态为___________ 种;基态Si原子,若其电子排布式表示为 违背了
违背了___________ 。
 违背了
违背了
您最近一年使用:0次
2024-04-23更新
|
60次组卷
|
2卷引用:上海市华东师范大学第三附属中学2023-2024学年高二下学期期中考试 化学试题(等级考)
名校
解题方法
2 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
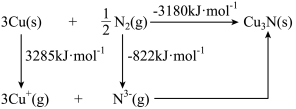
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
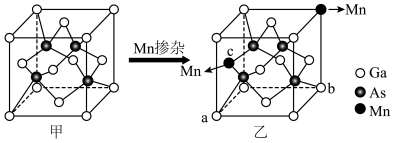
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近一年使用:0次
2023高三·全国·专题练习
3 . 谷氨酸[HOOC—CH(NH2)—CH2—CH2—COOH]的钠盐——谷氨酸钠(C5H8NO4Na)是味精的主要成分,谷氨酸分子中C原子的杂化方式为___________ ,C原子与O原子所形成的化学键中σ键与π键的数目比N(σ)∶N(π)=___________ ,π键的特征是两块电子云呈___________ 对称。
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)某元素原子的基态电子排布式为[Ar]3d104s24p1,该元素处于元素周期表的位置______ 。
(2)Ti基态原子的电子排布式为______ ,Ti元素位于____ 区,基态Ti原子核外有_____ 种不同运动状态的电子。
(3)铝原子核外电子云有_____ 种不同的伸展方向,其基态电子有_____ 种空间运动状态。
(4)基态Fe2+与Fe3+离子中未成对的电子数之比为______ 。与H2O分子互为等电子体一种阴离子为______ (填化学式)。
(1)某元素原子的基态电子排布式为[Ar]3d104s24p1,该元素处于元素周期表的位置
(2)Ti基态原子的电子排布式为
(3)铝原子核外电子云有
(4)基态Fe2+与Fe3+离子中未成对的电子数之比为
您最近一年使用:0次
5 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
(2)基态V原子中具有_______ 种不同能量的电子,具有_______ 种不同空间运动状态的电子,具有_______ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为_______ ,基态Se原子的价电子轨道表示式为_______ ,基态Mn2+的价电子排布式为_______ 。
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为_______ kJ·mol-1,O=O键键能为_______ kJ·mol-1。
(1)下列有关说法错误的是_______。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为
您最近一年使用:0次
2022-04-04更新
|
566次组卷
|
3卷引用:湖南省湖南师范大学附属中学2021-2022学年高二上学期期末考试化学试题
湖南省湖南师范大学附属中学2021-2022学年高二上学期期末考试化学试题四川省成都市武侯高级中学2021-2022学年高二下学期期中考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)



