名校
1 . 按要求填空。
(1)已知钴元素在周期表中的信息如下,回答下列问题:___________ ,基态原子核外有___________ 种不同运动状态的电子,画出该原子的原子结构示意图___________ 。
(2)已知高温下 比CuO更稳定,试从核外电子排布角度解释原因
比CuO更稳定,试从核外电子排布角度解释原因___________ 。
(3)氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知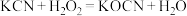 ,则
,则 中所含三种元素的电负性由大到小的顺序为
中所含三种元素的电负性由大到小的顺序为___________ (用元素符号表示,下同),第一电离能从大到小顺序为___________ ,基态氮原子的电子排布式为___________ ,其能量最高的电子所在原子轨道的电子云轮廓图为___________ 形。
(1)已知钴元素在周期表中的信息如下,回答下列问题:

(2)已知高温下
 比CuO更稳定,试从核外电子排布角度解释原因
比CuO更稳定,试从核外电子排布角度解释原因(3)氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知
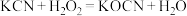 ,则
,则 中所含三种元素的电负性由大到小的顺序为
中所含三种元素的电负性由大到小的顺序为
您最近一年使用:0次
名校
2 . 如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:__________ 种不同空间运动状态。⑨号元素在周期表中的位置是__________ ,基态时其最高能层的电子占据的原子轨道电子云轮廓为__________ 形。第二周期所有元素中第一电离能介于①②之间的有__________ 种。基态⑩原子的简化电子排布式__________ ,该元素位于__________ 区。
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式__________ ,该分子为__________ (填“极性”或“非极性”)分子。
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
| A.非金属性:②>③ |
| B.气态最简单氢化物的稳定性:③>⑦ |
| C.最高价氧化物对应的水化物的碱性:④>⑤ |
| D.最简单氢化物的沸点:③>⑦ |
您最近一年使用:0次
3 . 近年来,我国航空航天事业成果显著,航空航天材料技术快速发展。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。基态钛原子的价层电子排布图为___________ 。
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,基态镓原子电子占据最高能级的电子云轮廓图为____________ 形。
(3)“C919”飞机机身使用复合材料——碳纤维和环氧树脂。
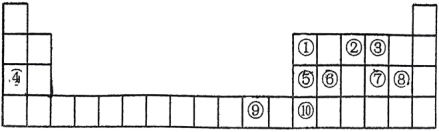
①下列电子排布图能表示碳原子的能量最低状态的是___________ (填字母)。
A.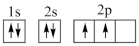 B.
B. 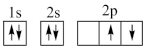 C.
C.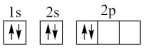 D.
D.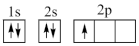
②氧原子的基态原子核外有___________ 个未成对电子。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。基态钛原子的价层电子排布图为
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,基态镓原子电子占据最高能级的电子云轮廓图为
(3)“C919”飞机机身使用复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的能量最低状态的是
A.
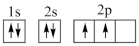 B.
B.  C.
C.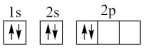 D.
D.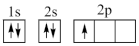
②氧原子的基态原子核外有
您最近一年使用:0次
名校
4 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是___________。
(2)基态V原子中具有____ 种不同能量的电子,具有_____ 种不同空间运动状态的电子,具有____ 种不同运动状态的电子。
(3)基态Cr原子的简化电子排布式为_________ ,基态Se原子的价电子轨道表示式为______ 。
(4)元素Cu在元素周期表中的位置_____ ,属于_____ 区,化合物 在加热条件下容易转化为
在加热条件下容易转化为 ,从原子结构的角度解释原因
,从原子结构的角度解释原因___________ 。
(5) 是离子晶体,其形成过程中的能量变化如图所示。
是离子晶体,其形成过程中的能量变化如图所示。
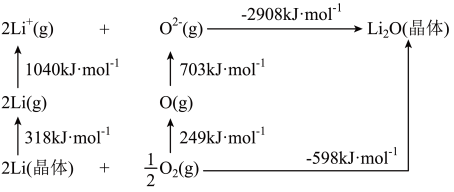
可知,Li原子的第一电离能为____  ,
, 键键能为
键键能为_____  。
。
(1)下列有关说法错误的是___________。
A.简单离子的还原性: |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(2)基态V原子中具有
(3)基态Cr原子的简化电子排布式为
(4)元素Cu在元素周期表中的位置
 在加热条件下容易转化为
在加热条件下容易转化为 ,从原子结构的角度解释原因
,从原子结构的角度解释原因(5)
 是离子晶体,其形成过程中的能量变化如图所示。
是离子晶体,其形成过程中的能量变化如图所示。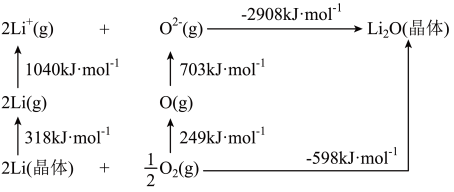
可知,Li原子的第一电离能为
 ,
, 键键能为
键键能为 。
。
您最近一年使用:0次
5 . 磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:
(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为________ 形。
(2)Fe元素位于周期表_____ 周期_____ 族;原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为___________ 。
(3)基态Mn2+的价电子排布式为___________ ,锰的第三电离能高于铁的第三电离能,其原因是___________ 。
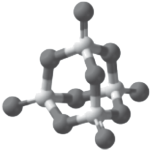
(4)P4S10的分子结构如图所示,其中含有________ 个六元环;______ g P4S10含有8molσ键。
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为
(2)Fe元素位于周期表
 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为(3)基态Mn2+的价电子排布式为
(4)P4S10的分子结构如图所示,其中含有
您最近一年使用:0次
2023-12-26更新
|
143次组卷
|
3卷引用:青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题
解题方法
6 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子中,占据最高能级电子的电子云轮廓图形状为___________ 。
(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是___________ 。
(ii)离子半径:Li+___________ H-(填“>”“=”或“<”)。
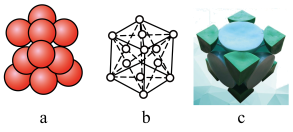
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:
(i)晶胞中锂的配位数为___________ 。
(ii)若锂原子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为___________  (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是
(ii)离子半径:Li+
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:

(i)晶胞中锂的配位数为
(ii)若锂原子的半径为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为 (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
2023-10-28更新
|
93次组卷
|
2卷引用:山西省朔州市怀仁市第九中学高中部2023-2024学年高三上学期11月期中考试化学试题
7 . 元素a、b、c、d、e、f在元素周期表的前四周期。
(1)元素a位于第二周期,其最高能层只有1个电子,该电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形。其离子半径___________ H-离子(填“大于”、“小于”或“等于”)。
(2)元素b的价电子排布式为nsnnpn,它的轨道表示式为___________ 。
(3)元素c、d、e为从上至下的卤族元素,关于其元素及对应单质,随核电荷数的性质变化不正确的是___________。
(4)元素f在第三周期,其各级电离能数据如下表,结合数据说明判断该元素是___________ 。
(1)元素a位于第二周期,其最高能层只有1个电子,该电子占据最高能级的符号是
(2)元素b的价电子排布式为nsnnpn,它的轨道表示式为
(3)元素c、d、e为从上至下的卤族元素,关于其元素及对应单质,随核电荷数的性质变化不正确的是___________。
A.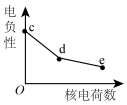 | B. | C. | D.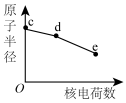 |
| 元素 | 电离能(kJ∙mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次
8 . 过波金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一。
(1)基态Cu原子核外K、L层电子的电子云有_____ 种不同的伸展方向。
(2)锌化铜是一种金属互化物,元素铜的第二电离能_____ (填“大于”、“小于”或“等于”)锌的第二电离能,理由是______ 。
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为(CH3)2SO。(CH3)2SO中C-S-O的键角______ (填“大于”、“小于”或“等于”)CH3COCH3中C-C-O的键角,理由是_____ ;元素S、Cl、O的电负性由大到小的顺序为______ 。
(4)利用CuSO4和NaOH制备的Cu(OH)2悬浊液检验醛基时,生成红色的Cu2O,其晶胞结构如图所示。
①该晶胞原子坐标参数A为(0,0,0);C为( ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为______ 。

②若Cu2O晶体密度为dg•cm-3,晶胞参数为apm,则阿伏加德罗常数值NA为______ (用含d和a的式子表示)。
(1)基态Cu原子核外K、L层电子的电子云有
(2)锌化铜是一种金属互化物,元素铜的第二电离能
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为(CH3)2SO。(CH3)2SO中C-S-O的键角
(4)利用CuSO4和NaOH制备的Cu(OH)2悬浊液检验醛基时,生成红色的Cu2O,其晶胞结构如图所示。
①该晶胞原子坐标参数A为(0,0,0);C为(
 ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为
②若Cu2O晶体密度为dg•cm-3,晶胞参数为apm,则阿伏加德罗常数值NA为
您最近一年使用:0次
名校
9 . “物质的性质、性能,不仅与组成有关,还与晶体结构有关。完成如下有关的问题。
(1)原子中电子有两种自旋状态,可分别用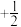 和
和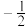 表示,称为电子的自旋磁量子数。则
表示,称为电子的自旋磁量子数。则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为________ ;从结构上分析基态 、
、 ,
,_______ 更稳定,原因是___________ 。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为______ ,其中Fe的配位数为_________ 。
(3)Cu-Mn-Al合金的晶胞如图1所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,如图2是沿立方格子对角面取得的截图。
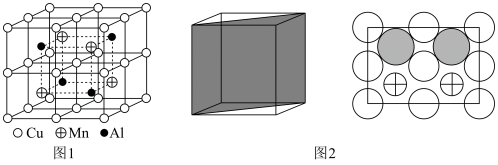
将Cu-Mn-Al合金晶胞沿棱投影于垂直面的是________。(填字母序号)
(1)原子中电子有两种自旋状态,可分别用
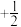 和
和 表示,称为电子的自旋磁量子数。则
表示,称为电子的自旋磁量子数。则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为 、
、 ,
,(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(3)Cu-Mn-Al合金的晶胞如图1所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,如图2是沿立方格子对角面取得的截图。

将Cu-Mn-Al合金晶胞沿棱投影于垂直面的是________。(填字母序号)
A.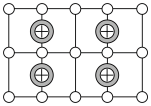 | B. | C.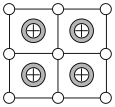 | D.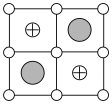 |
您最近一年使用:0次
解题方法
10 . 吡咯( ,沸点:129℃~131℃,微溶于水),吡啶(
,沸点:129℃~131℃,微溶于水),吡啶( ,沸点:15.2℃,易溶于有机溶剂,且能和水以任意比互溶),二者均可从骨焦油中分离得到,是重要的化工原料。
,沸点:15.2℃,易溶于有机溶剂,且能和水以任意比互溶),二者均可从骨焦油中分离得到,是重要的化工原料。
(1)吡咯、吡啶中的C-H键均是______ (填标号)σ键。
a.sp-s b.sp2-s c.sp3-s
1mol吡咯中含______ molσ键,1mol吡啶中含______ molσ键。
(2)N原子中有______ 种不同运动状态的电子。
(3)吡咯与吡啶的混合物可通过______ 的方法将二者分离,该方法所用的主要仪器有______ 。
(4)吡咯有微弱的酸性,可与活泼金属反应生成盐,写出吡咯与金属钾反应生成 的化学方程式:
的化学方程式:______ 。
(5)吡咯经聚合反应可得到聚吡咯,聚吡咯结构如图所示,其具有导电性,请根据结构分析聚吡咯具有导电性的可能原因:_____ 。

 ,沸点:129℃~131℃,微溶于水),吡啶(
,沸点:129℃~131℃,微溶于水),吡啶( ,沸点:15.2℃,易溶于有机溶剂,且能和水以任意比互溶),二者均可从骨焦油中分离得到,是重要的化工原料。
,沸点:15.2℃,易溶于有机溶剂,且能和水以任意比互溶),二者均可从骨焦油中分离得到,是重要的化工原料。(1)吡咯、吡啶中的C-H键均是
a.sp-s b.sp2-s c.sp3-s
1mol吡咯中含
(2)N原子中有
(3)吡咯与吡啶的混合物可通过
(4)吡咯有微弱的酸性,可与活泼金属反应生成盐,写出吡咯与金属钾反应生成
 的化学方程式:
的化学方程式:(5)吡咯经聚合反应可得到聚吡咯,聚吡咯结构如图所示,其具有导电性,请根据结构分析聚吡咯具有导电性的可能原因:

您最近一年使用:0次



