解题方法
1 . 下列说法正确的是
A.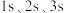 能级的电子云形状相同但大小不同 能级的电子云形状相同但大小不同 |
B.基态 的外围电子排布图为: 的外围电子排布图为: |
| C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
您最近半年使用:0次
2 . 下列说法中错误的是
| A.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道 |
| B.2p、3p、4p能级的轨道数依次增多 |
| C.2p和3p轨道形状均为哑铃形 |
D.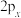 、 、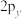 、 、 轨道相互垂直,但能量相等 轨道相互垂直,但能量相等 |
您最近半年使用:0次
3 . 下列说法正确的是
①Be与Al在周期表中处于对角线位置,可推出:Be(OH)2+2OH-=BeO +2H2O
+2H2O
②最外层电子数为ns2的元素都在元素化学性质都相似
③充有氖气的霓虹灯管通电时会发出红色光的主要原因,是电子由基态向激发态跃迁
时吸收除红光以外的光线
④某价层电子排布为4d54s1的基态原子,该元素位于周期表中第四周期第ⅠB族
⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
①Be与Al在周期表中处于对角线位置,可推出:Be(OH)2+2OH-=BeO
 +2H2O
+2H2O②最外层电子数为ns2的元素都在元素化学性质都相似
③充有氖气的霓虹灯管通电时会发出红色光的主要原因,是电子由基态向激发态跃迁
时吸收除红光以外的光线
④某价层电子排布为4d54s1的基态原子,该元素位于周期表中第四周期第ⅠB族
⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
| A.③⑤ | B.①②⑤ | C.②③④ | D.①⑤ |
您最近半年使用:0次
4 . 下列表示正确的是
A.醛基的电子式: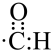 |
B. 的空间填充模型: 的空间填充模型: |
C.氯气的共价键电子云轮廓图: |
D.基态 的价层电子排布图: 的价层电子排布图: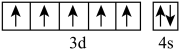 |
您最近半年使用:0次
5 . 非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有_______ 种。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点_______ (填“高于”或“低于”)Cl2O。
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。

(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性由大到小的顺序为
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有

您最近半年使用:0次
6 . 下列说法中正确的是
| A.s轨道电子云呈球形,表示电子绕原子核做圆周运动 |
| B.电子云图中的小黑点密度越大,说明该原子核外空间电子数目越多 |
C.ns能级的原子轨道图可表示为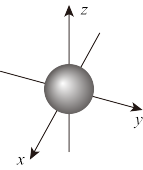 |
| D.3d表示d能级有3个轨道 |
您最近半年使用:0次
7 . 如图是s轨道和p轨道的原子轨道图,试回答问题:
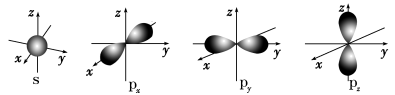
(1)s电子的原子轨道呈_______ 形,每个s轨道有_______ 个原子轨道;p电子的原子轨道呈_______ 形,每个p轨道有_______ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______ 电子,其电子云在空间有_______ 个伸展方向;元素X的名称是_______ ,它的氢化物的化学式是_______ 。若元素X的原子最外层电子排布式为nsn−1npn+1,那么X的元素符号应为_______ ,原子的轨道表示式为_______ 。

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
您最近半年使用:0次
2022-12-12更新
|
251次组卷
|
2卷引用:河北省保定市崇德实验中学2020-2021学年度高二下学期期中考试化学试题
解题方法
8 . 元素H、N、O、S、Ni、Fe之间可形成多种化合物。请回答下列问题:
(1)基态Fe2+原子的价电子排布式为____________ ;Fe原子最外层电子的电子云形状为__________ 。
(2)N、O、S三种元素的第一电离能由大到小的顺序为___________ ;下列状态的O中,最容易失去最外层电子的是___________ (填字母)。
A.1s22s22p3 B.1s22s22p4 C.1s22s22p33s1 D.1s22s22p23s1
(3)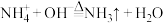 ,
, 转化为NH3的过程中,没有发生变化的有
转化为NH3的过程中,没有发生变化的有________ (填字母)。
A.键角 B.粒子的空间构型 C.杂化轨道类型
(4)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①若晶胞a中Fe原子直径为d pm,设该晶胞边长x,则x=_________ cm。(用含d的代数式表示)。
②晶胞b中与一个Fe原子最邻近的Fe原子共有_________ 个。
③若晶胞c的密度为ρ g/cm3,则铁的原子半径r=_________ cm。(NA表示阿伏加德罗常数的值,用含ρ、NA的式子表示)。
(1)基态Fe2+原子的价电子排布式为
(2)N、O、S三种元素的第一电离能由大到小的顺序为
A.1s22s22p3 B.1s22s22p4 C.1s22s22p33s1 D.1s22s22p23s1
(3)
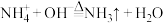 ,
, 转化为NH3的过程中,没有发生变化的有
转化为NH3的过程中,没有发生变化的有A.键角 B.粒子的空间构型 C.杂化轨道类型
(4)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①若晶胞a中Fe原子直径为d pm,设该晶胞边长x,则x=
②晶胞b中与一个Fe原子最邻近的Fe原子共有
③若晶胞c的密度为ρ g/cm3,则铁的原子半径r=
您最近半年使用:0次
9 . 本章第1、2节主要讲述了原子核外电子的运动状态。请用图示的方法总结下列描述核外电子运动状态的概念间的关系:电子排布式、轨道表示式、电子层、能级、原子轨道、电子云图、自旋运动状态、能量最低原理、电子在原子轨道上的排布顺序、泡利不相容原理、洪特规则____ 。
您最近半年使用:0次
解题方法
10 . 玻尔原子结构模型的主要内容是什么____ ?请简述其成功之处和不足之处____ 。
您最近半年使用:0次



