名校
解题方法
1 . 下列关于 轨道电子云示意图的说法中,错误的是
轨道电子云示意图的说法中,错误的是
 轨道电子云示意图的说法中,错误的是
轨道电子云示意图的说法中,错误的是A. 轨道上的电子在空间出现的概率分布呈z轴对称 轨道上的电子在空间出现的概率分布呈z轴对称 |
| B.点密集的地方表明电子出现的机会大 |
| C.电子先沿z轴正半轴运动,然后沿负半轴运动 |
D. 轨道电子云示意图的形状为纺锤形 轨道电子云示意图的形状为纺锤形 |
您最近一年使用:0次
2022-08-22更新
|
242次组卷
|
8卷引用:(人教版2019)选择性必修2第一章 原子结构与性质 第一节 原子结构 第3课时 电子云与原子轨道
(人教版2019)选择性必修2第一章 原子结构与性质 第一节 原子结构 第3课时 电子云与原子轨道鲁科版2019选择性必修2第1章 原子结构与元素性质 第1节 原子结构模型 第2课时 量子力学对原子核外电子运动状态的描述(已下线)2011-2012学年河南省偃师高中高二3月月考化学试卷山东省泰安市新泰第一中学(东校)2020-2021学年高二上学期第二次质量检测化学试题(已下线)1.1 原子结构模型-2020-2021学年高二化学课时同步练(鲁教2019选择性必修2)专题2 原子结构与元素性质 第一单元 原子核外电子的运动 第1课时 人类对原子结构的认识 原子核外电子的运动特征安徽省滁州市定远县民族中学2021-2022学年高二下学期第一次教学检测化学试题2.1.1原子核外电子的运动特征 课后
解题方法
2 . 下面有关“核外电子的运动状态”的说法,错误的是
| A.各原子轨道的伸展方向种数按p、d、f的顺序分别为3、5、7 |
| B.只有在电子层、原子轨道、原子轨道伸展方向及电子的自旋方向都确定时,才能准确表示电子的运动状态 |
| C.p轨道呈纺锤形,随着电子层的增加,p轨道的数量也在增多 |
| D.原子轨道伸展方向与能量大小是无关的 |
您最近一年使用:0次
名校
解题方法
3 . 第四周期中的18 种元素具有重要的用途,在现代工业中备受青睐。
(1)其中,未成对电子数最多的元素名称为_______ ,该元素的基态原子中,电子占据的最高能层具有的原子轨道数为_______ 。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是_______ 。
(3)AsH3 中心原子杂化的类型为_______ ,分子构型为_______
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为_______ 。
(5)与CN-互为等电子体的一种分子为_______ (填化学式);1.5mol [Fe(CN)6]3-中含有键的数目为_______
(1)其中,未成对电子数最多的元素名称为
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是
(3)AsH3 中心原子杂化的类型为
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为
(5)与CN-互为等电子体的一种分子为
您最近一年使用:0次
2021-05-29更新
|
112次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题
解题方法
4 . 老师在黑板上写出“Cr: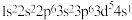 ”,下列各同学的判断中正确的是
”,下列各同学的判断中正确的是
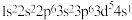 ”,下列各同学的判断中正确的是
”,下列各同学的判断中正确的是| A.甲同学认为是激发态Cr原子的核外电子排布式 |
| B.乙同学认为Cr元素位于第四周期第ⅥB族,处于d区,属过渡金属 |
| C.丙同学认为1s、2s、3s和4s的电子云形状相同,属同一种能级 |
D.丁同学认为Cr原子的价层电子排布式为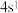 |
您最近一年使用:0次
名校
5 . 以下核外电子的表示方法中,能表示该微粒处于能量最低状态的是
A.N: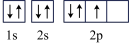 | B.F-: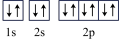 |
| C.Fe:[Ar]3d54s2 | D.Cu:3d94s2 |
您最近一年使用:0次
2021-04-15更新
|
248次组卷
|
2卷引用:四川省成都市新津中学高2020-2021学年高二下学期4月月考试题
解题方法
6 . 下列说法正确的是
| A.3p2表示3p能级上有两个轨道 |
| B.M层中的原子轨道数目为3 |
| C.价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 |
D.基态Cl原子的轨道表示式为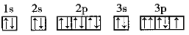 |
您最近一年使用:0次
名校
解题方法
7 . 有A、B、C、D、E五种元素。其相关信息如下:
请回答下列问题。
(1)D是___________ (填元素名称), D的基态原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________
(2) 若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为___________ (填序号);
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(3)元素E所在的周期,未成对电子数最多的元素是___________ (填元素符号)
(4)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是___________

(5)向溶液中滴加氨水,首先出现蓝色沉淀,氨水过量后沉淀逐渐溶解,加入乙醇后析出深蓝色晶体。请写出氨水过量后沉淀逐渐溶解的离子方程式:___________ 。
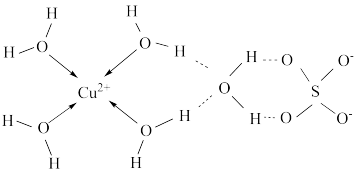
(6)科学家推测胆矾结构示意图可简单表示如图:胆矾的化学式用配合物的形式表示为___________ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有一个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和EO两种氧化物 |
请回答下列问题。
(1)D是
(2) 若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(3)元素E所在的周期,未成对电子数最多的元素是
(4)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(5)向溶液中滴加氨水,首先出现蓝色沉淀,氨水过量后沉淀逐渐溶解,加入乙醇后析出深蓝色晶体。请写出氨水过量后沉淀逐渐溶解的离子方程式:
(6)科学家推测胆矾结构示意图可简单表示如图:胆矾的化学式用配合物的形式表示为

您最近一年使用:0次
名校
8 . 铍(4Be)的某些化合物与铝的同类化合物具有相似的性质。下列描述正确的
| A.Be原子核外电子有3种不同的运动状态 |
| B.Be原子核外电子共占有3个原子轨道 |
| C.1 mol Be(OH)2能与含2molH2SO4的溶液反应 |
| D.1 mol Be(OH)2能与含2 mol NaOH的溶液反应 |
您最近一年使用:0次
解题方法
9 . 已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,D,B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属于同一周期,两者可以形成许多种共价化合物,C、F属于同一主族,B原子最外电子层的p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E的最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为__ 。
(2)F元素基态原子的价电子轨道表示式为__ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的分子式为__ 。
(4)A、C形成的两种常见分子中,其中一种为绿色氧化剂,电子式为__ 。
(5)基态G原子中,电子占据的最高电子层符号是__ ,该电子层有__ 个能级,电子数是__ 。该原子有__ 种运动状态不同的电子,最高能级符号是__ ,未成对电子数为__ 。
(6)与E同族且有4个电子层的元素的符号为__ ,它的简化电子排布式为__ ,与该元素同周期且核电荷数比该元素小7的元素在周期表中的位置是__ ,该元素基态原子的价电子排布式为__ ,__ (填“满足”或“不满足”)构造原理。
(1)E元素基态原子电子排布式为
(2)F元素基态原子的价电子轨道表示式为
(3)F、G元素对应的最高价含氧酸中酸性较强的分子式为
(4)A、C形成的两种常见分子中,其中一种为绿色氧化剂,电子式为
(5)基态G原子中,电子占据的最高电子层符号是
(6)与E同族且有4个电子层的元素的符号为
您最近一年使用:0次
解题方法
10 . 下列有关构造原理的说法错误的是
| A.原子核外电子填充3p、3d、4s能级的顺序一般为3p→4s→3d |
B.某基态原子部分核外电子的排布式为 |
| C.在多电子原子中,电子最后填入的能级不一定是原子最外能层上的能级 |
| D.从第三能层开始出现能级交错现象,即电子填入能级的顺序与能层顺序不同 |
您最近一年使用:0次



