1 . 以下说法中错误的是
| A.在①N、P、As和②Na、P、Cl中,元素的电负性随原子序数增大而递增的是② |
| B.同一原子中,2p、3p、4p能级的轨道依次增多 |
C.某元素原子的部分逐级电离能 分别为738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 分别为738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 |
| D.在共价键F-I、F-Cl和C-C,极性最强的是F-I |
您最近半年使用:0次
名校
2 . 下列说法正确的是
| A.在同一能级上运动的电子,其运动状态可能相同 |
| B.第三电子层有3s、3p、3d三个轨道 |
C.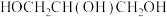 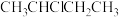 都是手性分子 都是手性分子 |
D.当碳原子的核外电子排布由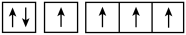 转变为 转变为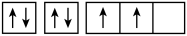 这一过程释放能量 这一过程释放能量 |
您最近半年使用:0次
3 . 光伏材料是指能将太阳能直接转换成电能的材料,光伏材料又称太阳能材料,只有半导体材料具有这种功能。硅(Si)、镓(Ga)、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:___________ 。硅烷很难像烷烃一样形成长链,这是因为硅的原子半径___________ (填“大于”“小于”或“等于”)碳的原子半径,因此键长___________ (填“长”或“短”),键能小。丁硅烯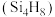 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是___________ 。
(3)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是___________ 。
(4)硅和锗都能与氯元素形成四氯化物 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:___________ 。
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
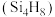 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近半年使用:0次
名校
解题方法
4 . 下列化学用语或说法中正确的是
A. 的名称:3-甲基丁烷 的名称:3-甲基丁烷 |
B.总共含有4个能级的能层符号: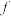 |
C. 的VSEPR模型为: 的VSEPR模型为: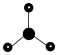 |
D.在氨水中, 与 与 分子间的氢键主要形式可表示为: 分子间的氢键主要形式可表示为: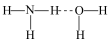 |
您最近半年使用:0次
5 . 下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。试回答下列问题:
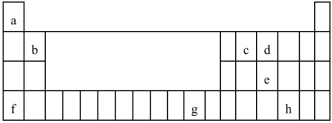
(1)基态f原子中,其占据的最高能层的符号是___________ 。
(2)元素a、c、d以原子个数比1∶1∶1形成的分子的电子式为___________ 。
(3)元素h的基态原子的价电子排布式为___________ 。
(4)元素g的基态g+核外电子的空间运动状态有___________ 种。
(5)某些不同族的元素因电负性相近,其性质也有一定的相似性。如元素b的最高价氧化物对素应的水化物和f的最高价氧化物对应的水化物能相互反应,其离子方程式是___________ 。

(1)基态f原子中,其占据的最高能层的符号是
(2)元素a、c、d以原子个数比1∶1∶1形成的分子的电子式为
(3)元素h的基态原子的价电子排布式为
(4)元素g的基态g+核外电子的空间运动状态有
(5)某些不同族的元素因电负性相近,其性质也有一定的相似性。如元素b的最高价氧化物对素应的水化物和f的最高价氧化物对应的水化物能相互反应,其离子方程式是
您最近半年使用:0次
名校
解题方法
6 . 对原子结构的认识是理解元素周期律和元素周期性的理论基础。下列说法错误的是。
| A.s电子的电子云轮廓图是球形 |
| B.同一原子中,3s电子的能量大于4s电子的能量 |
| C.处于最低能量状态的原子叫基态原子 |
| D.同一原子中,3p能级的轨道数等于4p能级的轨道数 |
您最近半年使用:0次
解题方法
7 . 下列说法不正确的是
| A.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道 |
| B.原子核外电子排布,先排满K层再排L层、先排满M层再排N层 |
| C.2p、3p、4p的轨道形状均为哑铃形 |
D.能层含有的原子轨道数为 (n为能层序数) (n为能层序数) |
您最近半年使用:0次
名校
解题方法
8 . 回答下列问题
(1)基态硫原子电子占据的最高能层符号为______ ,核外有______ 种能量不同的电子,硫原子核外电子有______ 种空间运动状态。
(2)与S同主族,位于第四周期的元素的符号是______ ,其价电子排布式为______
(3)已知有下列转化:
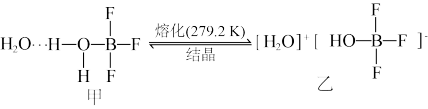
 的VSEPR模型为
的VSEPR模型为______ 。化合物乙中微粒间不存在的化学键有______ (填序号)。
A.离子键 B.共价键 C. 键 D.
键 D. 键 E.氢键
键 E.氢键
(4)相同条件下 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是______ (写分子式),理由是______ 。 中的
中的 键角
键角______ (填“>”“<”或“=”) 中的
中的 键角。
键角。
(5)已知 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为______ ,其中 键与
键与 键的个数比为
键的个数比为______ 。
(1)基态硫原子电子占据的最高能层符号为
(2)与S同主族,位于第四周期的元素的符号是
(3)已知有下列转化:
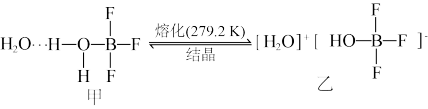
 的VSEPR模型为
的VSEPR模型为A.离子键 B.共价键 C.
 键 D.
键 D. 键 E.氢键
键 E.氢键(4)相同条件下
 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是 中的
中的 键角
键角 中的
中的 键角。
键角。(5)已知
 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为 键与
键与 键的个数比为
键的个数比为
您最近半年使用:0次
名校
9 . NA设为阿伏加德罗常数的值,下列说法正确的是
| A.40g处于基态的氩气中含有的p轨道电子总数为12NA |
| B.0.1mol/L的CH3COOH溶液中H+数目一定小于0.1NA |
| C.电解精炼含锌等杂质的粗铜,阴极增加64g,转移电子总数小于2NA |
D.100mL0.1mol/L的K2Cr2O7溶液中, 数目为0.01NA 数目为0.01NA |
您最近半年使用:0次
10 . 下列说法不正确 的是
A.氧原子可以形成 、 、 ,也可能形成 ,也可能形成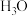 |
B.氯化铯晶体中,每个 周围紧邻且距离相等的 周围紧邻且距离相等的 共有6个 共有6个 |
C.同一原子中, 、 、 、 、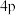 能级的轨道数目相等 能级的轨道数目相等 |
| D.缺角的氯化钠晶体在饱和氯化钠溶液中慢慢变为完美的立方体块 |
您最近半年使用:0次



