1 . 硅是典型的半导体元素,在电子、材料等领域应用广泛。请回答下列问题:
(1)基态硅(Si)原子的核外电子排布式为_______ 。
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为_______ ;基态C原子核外电子的空间运动状态有_______ 种。
②基态Si原子的核外电子占据_______ 个能层,_______ 个能级。
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的相互作用是_______ 。
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是_______ 。
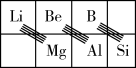
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式_______ 。
(1)基态硅(Si)原子的核外电子排布式为
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为
②基态Si原子的核外电子占据
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式

您最近一年使用:0次
2 . 能层
(1)含义:多电子原子核外电子的能量是不同的,核外电子按___________ 分成能层。
(2)原子核外电子的排布规律
①
②能量规律:原子核外电子总是可能先排布在能量___________ 的电子层上,然后由内向外依次排布在能量___________ 的电子层。即:能层的高低顺序为___________ 。
③数量规律:每层容纳的电子数不超过___________ 。
最外层电子数不超过___________ (K层为最外层时,电子数不超过___________ )
次外层电子数不超过18
倒数第三层电子数不超过32
(1)含义:多电子原子核外电子的能量是不同的,核外电子按
(2)原子核外电子的排布规律
①
| 电子层数 | 一 | 二 | 三 | 四 | 五 | 六 | 七 |
| 符号 | |||||||
| 每层最多容纳电子数 |
③数量规律:每层容纳的电子数不超过
最外层电子数不超过
次外层电子数不超过18
倒数第三层电子数不超过32
您最近一年使用:0次
2022-02-16更新
|
527次组卷
|
2卷引用:河南省平顶山市龙河实验高级中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
3 . 第四周期中的18 种元素具有重要的用途,在现代工业中备受青睐。
(1)其中,未成对电子数最多的元素名称为_______ ,该元素的基态原子中,电子占据的最高能层具有的原子轨道数为_______ 。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是_______ 。
(3)AsH3 中心原子杂化的类型为_______ ,分子构型为_______
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为_______ 。
(5)与CN-互为等电子体的一种分子为_______ (填化学式);1.5mol [Fe(CN)6]3-中含有键的数目为_______
(1)其中,未成对电子数最多的元素名称为
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是
(3)AsH3 中心原子杂化的类型为
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为
(5)与CN-互为等电子体的一种分子为
您最近一年使用:0次
2021-05-29更新
|
112次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题
4 . 某元素原子的电子排布式为1s22s22p63s23p1。该原子核外共__ 个电子层,有__ 种能量不同的电子。核外电子占有的轨道总数是__ 个,有___ 种不同运动状态的电子。
您最近一年使用:0次
2019-11-11更新
|
156次组卷
|
2卷引用:上海市宝山中学2017-2018学年高三第一学期期中考化学试题
5 . (1)某元素的原子序数为13,则:
①此元素原子的电子总数是________ ;②有________ 个能层,________ 个能级;
(2)写出C、Cl-的电子排布式:
①Cl-:____________________________________________________________ ;
②C:___________________________________________________________ ;
①此元素原子的电子总数是
(2)写出C、Cl-的电子排布式:
①Cl-:
②C:
您最近一年使用:0次
2019-05-02更新
|
195次组卷
|
2卷引用:吉林省汪清县第六中学2018-2019学年高二下学期期中考试化学试题



