1 . 光伏材料是指能将太阳能直接转换成电能的材料,光伏材料又称太阳能材料,只有半导体材料具有这种功能。硅(Si)、镓(Ga)、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:___________ 。硅烷很难像烷烃一样形成长链,这是因为硅的原子半径___________ (填“大于”“小于”或“等于”)碳的原子半径,因此键长___________ (填“长”或“短”),键能小。丁硅烯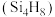 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是___________ 。
(3)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是___________ 。
(4)硅和锗都能与氯元素形成四氯化物 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:___________ 。
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
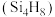 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近半年使用:0次
2 . 电子层数与该电子层中的能级数、原子轨道数有什么关系?能级与原子轨道数之间又有什么关系?______
您最近半年使用:0次
3 . 回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ,Sm的价层电子排布式4f66s2,Sm3+的价层电子排布式为___________ 。
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子占据最高能级的电子云轮廓图为___________ 形。
②离子半径Li+___________ H-(填“>”“=”或“<”)。
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是___________ (填“金属”或“非金属”),该化合物中显负价的是___________ (填“X”或“Y”)。
(4) 的空间构型为
的空间构型为___________ ;O3是___________ 分子(填“极性”或“非极性”)。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为
②离子半径Li+
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是
(4)
 的空间构型为
的空间构型为
您最近半年使用:0次
4 . 回答下列问题:
(1)第四周期中,未成对电子数最多的元素是_______ 。(填名称)
(2)它位于第_______ 族。
(3)核外电子排布式是_______ 。
(4)它有_______ 个能层,_______ 个能级,_______ 种运动状态不同的电子。
(5)价电子排布图_______ 。
(6)属于_______ 区。
(1)第四周期中,未成对电子数最多的元素是
(2)它位于第
(3)核外电子排布式是
(4)它有
(5)价电子排布图
(6)属于
您最近半年使用:0次
21-22高二下·全国·单元测试
解题方法
5 . 原子轨道与能层序数的关系
(1)不同能层的同种能级的原子轨道形状_______ ,只是半径_______ 。能层序数n越_______ ,原子轨道的半径越_______ 。如:
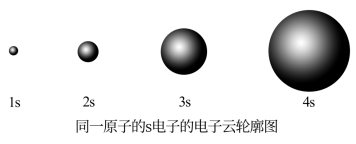
(2)s能级只有1个原子轨道。p能级有3个原子轨道,它们互相垂直,分别以px、py、pz表示。在同一能层中px、py、pz的能量_______ 。
(3)原子轨道数与能层序数(n)的关系:原子轨道数目=_______ 。
(1)不同能层的同种能级的原子轨道形状

(2)s能级只有1个原子轨道。p能级有3个原子轨道,它们互相垂直,分别以px、py、pz表示。在同一能层中px、py、pz的能量
(3)原子轨道数与能层序数(n)的关系:原子轨道数目=
您最近半年使用:0次
6 . 第四周期是周期表中的第一个长周期,元素种类丰富,其中有一种未成对电子数最多的元素,完成以下填空:
(1)该元素是_______ (填名称),它位于第_______ 族。
(2)核外电子排布式是_______ ,最高能层符号为_______ 。
(3)它有_______ 个能层,_______ 个能级,_______ 种运动状态不同的电子。
(4)价电子排布式:_______ ,价电子排布图:_______ 。
(5)属于_______ 区。
(1)该元素是
(2)核外电子排布式是
(3)它有
(4)价电子排布式:
(5)属于
您最近半年使用:0次
解题方法
7 . 按要求填空:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_____ 。
(2)基态Ti原子的核外电子排布式为_____ 。
(3)Fe基态核外电子排布式为_____ 。
(4)氮原子价层电子的轨道表达式(电子排布图)为_____ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)基态Ti原子的核外电子排布式为
(3)Fe基态核外电子排布式为
(4)氮原子价层电子的轨道表达式(电子排布图)为
您最近半年使用:0次
解题方法
8 . 按要求填空:
(1)基态Si原子中,电子占据的能量最高的电子层符号为_______ ,该电子层具有的原子轨道数为_______ ,具有的电子数为_______
(2)基态N原子中,核外电子占据_______ 个电子层,_______ 个原子轨道,共有_______ 种运动状态;电子占据的能量最高的原子轨道的形状为_______ 。
(1)基态Si原子中,电子占据的能量最高的电子层符号为
(2)基态N原子中,核外电子占据
您最近半年使用:0次
2022-08-22更新
|
239次组卷
|
2卷引用:专题2 原子结构与元素性质 第一单元 原子核外电子的运动 第1课时 人类对原子结构的认识 原子核外电子的运动特征
9 . 硅是典型的半导体元素,在电子、材料等领域应用广泛。请回答下列问题:
(1)基态硅(Si)原子的核外电子排布式为_______ 。
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为_______ ;基态C原子核外电子的空间运动状态有_______ 种。
②基态Si原子的核外电子占据_______ 个能层,_______ 个能级。
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的相互作用是_______ 。
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是_______ 。
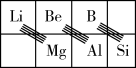
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式_______ 。
(1)基态硅(Si)原子的核外电子排布式为
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为
②基态Si原子的核外电子占据
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式

您最近半年使用:0次
10 . 总结:
(1)原子核外电子总是先排能力_______ 的电子层,然后有里向外,依次排布即排满了_______ 层才能排L层,排满了_______ 层才能排M层。
(2)原子核外每个电子层最多容纳_______ 个电子(n为电子层序数)
(3)原子最外层电子数不超过_______ 个电子(K层为最外层时,不超过_______ 个电子)。
(4)原子次外层电子数不超过_______ 个电子。
(5)倒数第三层不超过_______ 个电子
(1)原子核外电子总是先排能力
(2)原子核外每个电子层最多容纳
(3)原子最外层电子数不超过
(4)原子次外层电子数不超过
(5)倒数第三层不超过
您最近半年使用:0次



