2020高三·全国·专题练习
1 . (1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
您最近一年使用:0次
解题方法
2 . 根据题给要求填空
(1)某元素的基态原子最外层电子排布式为3s23p2,它的次外层上电子云形状有________ 种,原子中所有电子占有________ 个轨道,核外共有________ 种运动状态不同的电子。
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是_______ 。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是________ ,F2-的电子排布式是______ 。
(4)M能层上有________ 个能级,有________ 个轨道,作为内层最多可容纳________ 个电子,作为最外层时,最多可含有________ 个未成对电子。
(1)某元素的基态原子最外层电子排布式为3s23p2,它的次外层上电子云形状有
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是
(4)M能层上有
您最近一年使用:0次
名校
解题方法
3 . 氮、磷、砷、铁等元素及其化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)基态砷原子中核外电子占据最高能层的符号为__ ,该能层的原子轨道数有__ 个。
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为__ 杂化,基态N原子电子占据最高能级的电子云轮廓图为___ 形。
②肼与氨气熔点、沸点差异最主要的原因是__ 。
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有__ (填序号)。
A.离子键 B.极性键 C.配位键 D.氢键
(1)基态砷原子中核外电子占据最高能层的符号为
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为
②肼与氨气熔点、沸点差异最主要的原因是
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有
A.离子键 B.极性键 C.配位键 D.氢键
您最近一年使用:0次
解题方法
4 . K层有_____________ 个能级,用符号表示为_____________ ;L层有_____________ 个目自级,用符号表示为_____________ ;M层有_____________ 个能级,用符号表示为_____________ 。由此可推知第n(n为正整数)电子层最多可能有_____________ 个能级,当 时,能量最低的两个能级的符号分别为
时,能量最低的两个能级的符号分别为_____________ ,它们的原子轨道形状分别为_____________ 、_____________ 。
 时,能量最低的两个能级的符号分别为
时,能量最低的两个能级的符号分别为
您最近一年使用:0次
解题方法
5 . 有两种气态单质 和
和 ,已知
,已知 和
和 所含的原子个数相等,分子数之比为
所含的原子个数相等,分子数之比为 。
。 和
和 的原子核内质子数都等于中子数,
的原子核内质子数都等于中子数, 原子
原子 层电子数是
层电子数是 层的3倍。
层的3倍。
(1) 、
、 的元素符号分别为
的元素符号分别为_______ 。
(2) 中的
中的 值为
值为_______ 。
(3) 的能层数目为
的能层数目为_______ 。
(4) 、
、 形成的一种气态化合物与水反应能生成由
形成的一种气态化合物与水反应能生成由 、
、 形成的另一种气态化合物,写出该反应的化学方程式:
形成的另一种气态化合物,写出该反应的化学方程式:_______ 。
 和
和 ,已知
,已知 和
和 所含的原子个数相等,分子数之比为
所含的原子个数相等,分子数之比为 。
。 和
和 的原子核内质子数都等于中子数,
的原子核内质子数都等于中子数, 原子
原子 层电子数是
层电子数是 层的3倍。
层的3倍。(1)
 、
、 的元素符号分别为
的元素符号分别为(2)
 中的
中的 值为
值为(3)
 的能层数目为
的能层数目为(4)
 、
、 形成的一种气态化合物与水反应能生成由
形成的一种气态化合物与水反应能生成由 、
、 形成的另一种气态化合物,写出该反应的化学方程式:
形成的另一种气态化合物,写出该反应的化学方程式:
您最近一年使用:0次
2020-03-04更新
|
184次组卷
|
2卷引用:人教化学选修3第一章第一节课时1
解题方法
6 . 根据 、
、 、
、 、
、 、
、 五种元素的原子结构,回答下列问题:
五种元素的原子结构,回答下列问题:
(1)只有 层与
层与 层的原子有
层的原子有______ ;
(2)含有 层的原子有
层的原子有______ ;
(3)最外层电子数相同的原子有______ ;
 、
、 、
、 、
、 、
、 五种元素的原子结构,回答下列问题:
五种元素的原子结构,回答下列问题:(1)只有
 层与
层与 层的原子有
层的原子有(2)含有
 层的原子有
层的原子有(3)最外层电子数相同的原子有
您最近一年使用:0次
2020-03-04更新
|
149次组卷
|
2卷引用:人教化学选修3第一章第一节课时1
7 . 某元素原子的电子排布式为1s22s22p63s23p1。该原子核外共__ 个电子层,有__ 种能量不同的电子。核外电子占有的轨道总数是__ 个,有___ 种不同运动状态的电子。
您最近一年使用:0次
2019-11-11更新
|
156次组卷
|
2卷引用:上海市宝山中学2017-2018学年高三第一学期期中考化学试题
8 . (1)某元素的原子序数为13,则:
①此元素原子的电子总数是________ ;②有________ 个能层,________ 个能级;
(2)写出C、Cl-的电子排布式:
①Cl-:____________________________________________________________ ;
②C:___________________________________________________________ ;
①此元素原子的电子总数是
(2)写出C、Cl-的电子排布式:
①Cl-:
②C:
您最近一年使用:0次
2019-05-02更新
|
195次组卷
|
2卷引用:吉林省汪清县第六中学2018-2019学年高二下学期期中考试化学试题
名校
解题方法
9 . 请回答下列问题
(1)某元素的原子序数为33,则:此元素原子的电子总数是______ ;有_____ 个不同运动状态的电子,有____ 个电子层,____ 个能级;简化的电子排布式为__________ 。
(2)1s22s22p63s23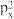 违背了
违背了____________ 。核电荷数为24的元素,其价电子排布的轨道表示式______ ,其原子的最外层电子数和未成对电子数分别为_____ 和_____ 。
(3)电子排布式为1s22s22p63s23p6某微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是________ , 原子核外电子云有________ 种不同的伸展方向。
(1)某元素的原子序数为33,则:此元素原子的电子总数是
(2)1s22s22p63s23
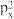 违背了
违背了(3)电子排布式为1s22s22p63s23p6某微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是
您最近一年使用:0次



