1 . 下列化学用语表示正确的是
A.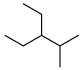 的名称:2-甲基-3-乙基戊烷 的名称:2-甲基-3-乙基戊烷 |
B. 的价层电子对互斥 的价层电子对互斥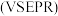 模型: 模型: |
C. 的电子式: 的电子式: |
D.氮的基态原子轨道表示式: |
您最近一年使用:0次
2 . 橄榄石型 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过 ,
, 与
与 溶液发生共沉淀反应制得,反应方程式为
溶液发生共沉淀反应制得,反应方程式为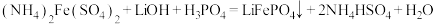 。下列说法正确的是
。下列说法正确的是
 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过 ,
, 与
与 溶液发生共沉淀反应制得,反应方程式为
溶液发生共沉淀反应制得,反应方程式为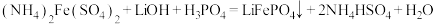 。下列说法正确的是
。下列说法正确的是A. 的空间填充模型: 的空间填充模型: |
B. 键角: 键角: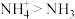 |
C.基态 原子的价层电子轨道表示式: 原子的价层电子轨道表示式: |
D.用电子式表示 的形成过程: 的形成过程: |
您最近一年使用:0次
解题方法
3 . 以辉铋矿(主要成分为Bi2S3,含有FeS2、SiO2杂质)和软锰矿(主要成分为MnO2)为原料制备超细氧化铋的工艺流程如下: ,
, 易发生水解,其反应的离子方程式为:
易发生水解,其反应的离子方程式为: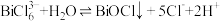 。
。
(1)Bi元素位于第6周期VA族,其价电子轨道表示式为___________ ,BiOCl叫氯氧化铋而不叫次氯酸铋,从化合价角度分析原因为___________ 。
(2)“联合焙烧”时,Bi2S3和MnO2在空气中反应生成Bi2O3和MnSO4.该反应的化学方程式为___________ 。
(3)BiCl 能被有机萃取剂(TBP)苯取,其萃取原理可表示为:
能被有机萃取剂(TBP)苯取,其萃取原理可表示为: 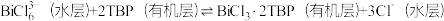 。
。
①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图所示。c(Cl-)最佳为1.3mol·L-1的可能原因是___________ 。
②萃取后分液所得水相中的主要阳离子为___________ (填化学式)。___________ 。
(5)在空气中加热分解草酸铋晶体,测得升温加热过程中剩余固体的质量与起始Bi2(C2O4)3·7H2O的质量的比值随温度变化的关系如图所示。400℃时制得超细氧化铋,其化学式为___________ 。(M[Bi2(C2O4)3·7H2O]=808g·mol-1)

 ,
, 易发生水解,其反应的离子方程式为:
易发生水解,其反应的离子方程式为: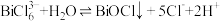 。
。(1)Bi元素位于第6周期VA族,其价电子轨道表示式为
(2)“联合焙烧”时,Bi2S3和MnO2在空气中反应生成Bi2O3和MnSO4.该反应的化学方程式为
(3)BiCl
 能被有机萃取剂(TBP)苯取,其萃取原理可表示为:
能被有机萃取剂(TBP)苯取,其萃取原理可表示为: 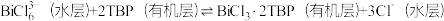 。
。①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图所示。c(Cl-)最佳为1.3mol·L-1的可能原因是
②萃取后分液所得水相中的主要阳离子为

(5)在空气中加热分解草酸铋晶体,测得升温加热过程中剩余固体的质量与起始Bi2(C2O4)3·7H2O的质量的比值随温度变化的关系如图所示。400℃时制得超细氧化铋,其化学式为

您最近一年使用:0次
名校
解题方法
4 . 下列化学用语的表达正确的是
A.2-丁烯的键线式: |
B. 的电子式: 的电子式: |
C.基态碳原子价层电子轨道表示式: |
D.四氯化碳的球棍模型: |
您最近一年使用:0次
7日内更新
|
77次组卷
|
2卷引用:湖北省宜荆荆随恩2023-2024学年高二下学期5月联考化学试题
名校
5 . 冰晶石(Ng3AlF6)是电解铝工业的助熔剂、制造乳白色玻璃和搪瓷的遮光剂。制取冰晶石的反应为 ,下列有关化学用语表示正确的是
,下列有关化学用语表示正确的是
 ,下列有关化学用语表示正确的是
,下列有关化学用语表示正确的是A.基态Al原子的价层电子轨道表示式: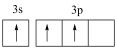 |
B.CO2的电子式: |
C.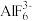 的结构式: 的结构式: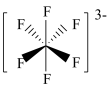 |
D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
7日内更新
|
204次组卷
|
3卷引用:甘肃省兰州市第二中学2023-2024学年高三下学期第十次月考化学试题
6 . 烧碱溶液可以侵蚀玻璃,反应为SiO2+2NaOH =Na2SiO3+H2O。下列说法正确的是
A.Na+结构示意图: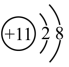 | B.基态Si原子价电子轨道式: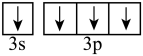 |
| C.SiO2结构式:O=Si=O | D.H2O电子式: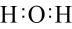 |
您最近一年使用:0次
7 . 氯及其化合物应用广泛。 易液化,可储存于钢瓶中。氯气可用于生产
易液化,可储存于钢瓶中。氯气可用于生产 、
、 、
、 、
、 等化工产品。
等化工产品。 和
和 的化学性质相似,能与
的化学性质相似,能与 反应生成两种酸。
反应生成两种酸。 (其中
(其中 为
为 价)可用于漂白和杀菌消毒,其水解可生成
价)可用于漂白和杀菌消毒,其水解可生成 和
和 。
。 水解的反应原理示意图如图所示。下列说法正确的是
水解的反应原理示意图如图所示。下列说法正确的是
 易液化,可储存于钢瓶中。氯气可用于生产
易液化,可储存于钢瓶中。氯气可用于生产 、
、 、
、 、
、 等化工产品。
等化工产品。 和
和 的化学性质相似,能与
的化学性质相似,能与 反应生成两种酸。
反应生成两种酸。 (其中
(其中 为
为 价)可用于漂白和杀菌消毒,其水解可生成
价)可用于漂白和杀菌消毒,其水解可生成 和
和 。
。 水解的反应原理示意图如图所示。下列说法正确的是
水解的反应原理示意图如图所示。下列说法正确的是
A. 的结构式为 的结构式为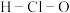 |
B. 中 中 、 、 之间的共用电子对偏向于 之间的共用电子对偏向于 |
C.基态 原子的轨道表示式为 原子的轨道表示式为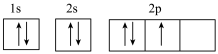 |
D. 的水解过程中 的水解过程中 原子的杂化轨道类型发生了变化 原子的杂化轨道类型发生了变化 |
您最近一年使用:0次
8 . 有 A 、B 、C 、D四种短周期主族元素,它们的原子序数依次增大,其中 A元素原子核外仅有一个非空原子轨道,也是宇宙中最丰富的元素;B元素原子核外 p电子数比 s电子数少1;C为金属元素且原子核外 p电子数和 s电子数相等;D元素的原子核外所有 p轨道为全充满或半充满状态。
(1)写出四种元素的元素名称:A___________ ,B___________ ,C___________ ,D___________ 。
(2)写出 C 、D 两种元素基态原子的核外电子排布图(轨道表示式):
C:___________ ;D:___________ 。
(3)B 、C 两种元素的单质在一定条件下反应的化学方程式___________ ,该产物溶于水产生白色沉淀,同时有刺激性气味的气体产生,发生反应方程式为 ___________ 。
(4)B元素的单质的电子式为___________ ,其最简单氢化物的电子式为 ___________ 。
(1)写出四种元素的元素名称:A
(2)写出 C 、D 两种元素基态原子的核外电子排布图(轨道表示式):
C:
(3)B 、C 两种元素的单质在一定条件下反应的化学方程式
(4)B元素的单质的电子式为
您最近一年使用:0次
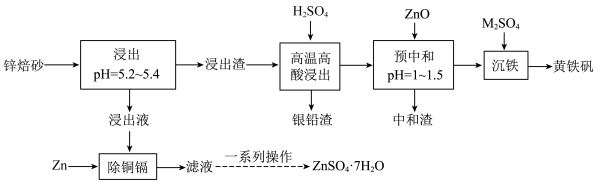
9 . 锌焙砂是锌精矿经焙烧后所得的产物,是褐色微颗粒状固体,其主要成分为ZnO,还含有Fe2O3、ZnFe2O4和少量Pb、Ag、Cd、Cu,以锌焙砂为原料制备ZnSO4·7H2O和黄铁矾的工艺流程如下:
②25℃下,Zn2+和Fe3+开始沉淀和沉淀完全(c=1×10-5mol·L-1)时的pH如下表:
回答下列问题:
(1)基态Fe原子价层电子轨道表示式为___________ ,铜元素的焰色为绿色,该光谱属于___________ (填“发射”或“吸收”)光谱。
(2)欲提高pH在5.2~5.4时的“浸出”速率,可采用的方法是___________ (写两种)。
(3)在pH=5.2~5.4“浸出”时,锌焙砂中的铜转化为Cu2+反应的离子方程式为___________ 。
(4)pH=6.2时,漫出液中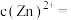
___________ mol·L-1。
(5)当有k+、Na+或 存在时,调节含Fe3+溶液的pH,即可生成黄铁矾,不同种类的阳离子“沉铁”效果如图,则工艺流程中,MnSO4最好选用
存在时,调节含Fe3+溶液的pH,即可生成黄铁矾,不同种类的阳离子“沉铁”效果如图,则工艺流程中,MnSO4最好选用___________ (填化学式)。___________ 、___________ 、过滤、洗涤、干燥。
②25℃下,Zn2+和Fe3+开始沉淀和沉淀完全(c=1×10-5mol·L-1)时的pH如下表:
| 金属离子 | pH | |
| 开始沉淀 | 沉淀完全 | |
| Zn2+ | 6.2 | 8.2 |
| Fe3+ | 1.5 | 3.2 |
(1)基态Fe原子价层电子轨道表示式为
(2)欲提高pH在5.2~5.4时的“浸出”速率,可采用的方法是
(3)在pH=5.2~5.4“浸出”时,锌焙砂中的铜转化为Cu2+反应的离子方程式为
(4)pH=6.2时,漫出液中
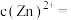
(5)当有k+、Na+或
 存在时,调节含Fe3+溶液的pH,即可生成黄铁矾,不同种类的阳离子“沉铁”效果如图,则工艺流程中,MnSO4最好选用
存在时,调节含Fe3+溶液的pH,即可生成黄铁矾,不同种类的阳离子“沉铁”效果如图,则工艺流程中,MnSO4最好选用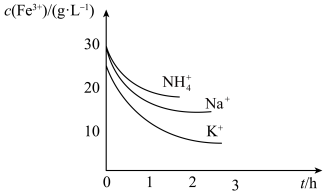
您最近一年使用:0次
10 . 下列表达式错误的是
| A.基态铬原子(24Cr)的价层电子排布式:3d54s1 |
B.氮原子的L层电子的轨道表示式:  |
C.碳-12原子: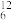 C C |
| D.S2-的核外电子排布式:1s22s22p63s23p4 |
您最近一年使用:0次



