1 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的_______ 区,其价电子排布式为_______ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+_______ Fe2+(填“大于”或“小于”)。
(5)下列各组多电子原子的能级能量比较不正确的是_______。
①2p=3p②4s>2s③4p>4f④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p
 d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是_______。
①2p=3p②4s>2s③4p>4f④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近半年使用:0次
2 . 化学与生活密切相关,下列说法错误的是
| A.GaN具有半导体的性质,常用作 LED 灯的芯片,属于新型无机非金属材料 |
| B.宇航服中气密限制层使用的涤纶属于合成纤维 |
| C.推广使用煤液化技术,可减少二氧化碳的排放 |
| D.霓虹灯的发光机制与氢原子光谱形成的机制基本相同 |
您最近半年使用:0次
3 . 下列说法正确的是
①基态碳原子电子排布式 违反了洪特规则
违反了洪特规则
②最外层电子数为 的元素都在元素化学性质都相似
的元素都在元素化学性质都相似
③充有氖气的霓虹灯管通电时会发出红光的主要原因,是电子由基态向激发态跃迁时吸收除红光以外的光
④某价层电子排布为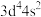 的基态原子,该元素位于周期表中第四周期第ⅥB族
的基态原子,该元素位于周期表中第四周期第ⅥB族
⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
①基态碳原子电子排布式
 违反了洪特规则
违反了洪特规则②最外层电子数为
 的元素都在元素化学性质都相似
的元素都在元素化学性质都相似③充有氖气的霓虹灯管通电时会发出红光的主要原因,是电子由基态向激发态跃迁时吸收除红光以外的光
④某价层电子排布为
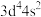 的基态原子,该元素位于周期表中第四周期第ⅥB族
的基态原子,该元素位于周期表中第四周期第ⅥB族⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
| A.③⑤ | B.①②⑤ | C.②③④ | D.①⑤ |
您最近半年使用:0次
解题方法
4 . 化合物 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为____________ 。
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的________ 区。
(3)Fe能与CO、 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有________ mol配位原子, 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为_________ 。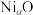 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为________ 。
(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于_________ (填“共价”“离子”或“分子”)晶体,_________ (填“是”或“否”)含有配位键,晶体中P原子的配位数为__________ 。 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为___________ 。
 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的
(3)Fe能与CO、
 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为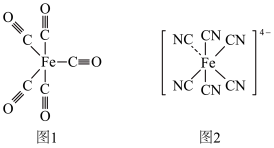
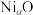 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于

 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为
您最近半年使用:0次
解题方法
5 . 下列物质的结构或性质不能 解释其用途的是
| 选项 | 结构或性质 | 用途 |
| A | 植物油可加氢硬化 | 植物油可制肥皂 |
| B |  水解生成 水解生成 胶体 胶体 | 明矾可作净水剂 |
| C | 金属原子核外电子跃迁 | 烟花中加入金属化合物产生五彩缤纷的焰火 |
| D | 聚丙烯酸钠中含有亲水基团 | 聚丙烯酸钠可作高分子吸水材料 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
6 . 下列有关物质的分离或鉴别说法正确的是
| A.重结晶法提纯苯甲酸要用的仪器有:漏斗,烧杯,冷凝管 |
| B.分液操作时应先将下层液体从分液漏斗下口放出后再将上层液体继续放出 |
| C.酒精不能萃取水中的溶质,但是能萃取苯中的溶质 |
| D.原子光谱上的特征谱线,可用于元素鉴定 |
您最近半年使用:0次
7 . 化学与生活、生产、科技等密切相关。下列说法正确的是
| A.“杯酚”能分离C60和C70,体现了超分子的“分子识别”特性 |
| B.牙膏中添加氟化物用于预防龋齿是利用了氧化还原反应的原理 |
| C.“神州十七号”使用砷化镓(GaAs)太阳能电池,供电时GaAs发生了电子转移 |
| D.钾盐可用作紫色烟花的原料是因为电子跃迁到激发态过程中释放能量产生紫色光 |
您最近半年使用:0次
8 . 太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
您最近半年使用:0次
9 . 1913年,玻尔提出氢原子模型,解释了氢原子的光谱。关于玻尔原子结构模型,下列说法中正确的是
| A.玻尔原子结构模型可以解释多电子原子的光谱 |
| B.原子中的电子在定态轨道上运动时,可能会辐射能量 |
| C.电子在不同能量的两个轨道之间发生跃迁时,会辐射或吸收能量 |
| D.电子在定态轨道上的运动状态被称为基态 |
您最近半年使用:0次
2024-04-22更新
|
55次组卷
|
3卷引用:上海交通大学附属中学2023-2024学年高二下学期期中考试化学试题
10 . 工业合成氨中,常用亚铜盐的氨水溶液除去原料气中的 以防止催化剂中毒,反应的离子方程式为
以防止催化剂中毒,反应的离子方程式为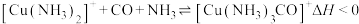 。吸收CO时,溶液中[Cu(NH3)2]+和[Cu(NH3)2CO]+的浓度(mol·L-1)变化情况如下:
。吸收CO时,溶液中[Cu(NH3)2]+和[Cu(NH3)2CO]+的浓度(mol·L-1)变化情况如下:
1.欲充分吸收CO,适宜的条件是_____。(不定项)
2.前30min[Cu(NH3)2]+的平均反应速率为_____ 。
3.60min时改变的条件可能是_____ 。
4.其他条件不变时,下列说法正确的有_____。(不定项)
5.基态铜原子的未成对电子数为_____ ,铜元素的焰色试验为绿色,为_____ (填“发射”或“吸收”)光谱。
6.无色的亚铜盐的氨水溶液放置一段时间的话,会变成深蓝色的溶液,请解释可能的原因_____ 。
 以防止催化剂中毒,反应的离子方程式为
以防止催化剂中毒,反应的离子方程式为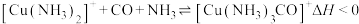 。吸收CO时,溶液中[Cu(NH3)2]+和[Cu(NH3)2CO]+的浓度(mol·L-1)变化情况如下:
。吸收CO时,溶液中[Cu(NH3)2]+和[Cu(NH3)2CO]+的浓度(mol·L-1)变化情况如下:| 0min | 30min | 45min | 60min | 90min | |
| [Cu(NH3)2]+ | 2.0 | 1.2 | 0.9 | 0.9 | 1.8 |
| [Cu(NH3)2CO]+ | 0 | a | 1.1 | 1.1 | 0.2 |
| A.升高温度 | B.增大压强 | C.增大亚铜盐浓度 | D.加水 |
3.60min时改变的条件可能是
4.其他条件不变时,下列说法正确的有_____。(不定项)
A. 与 与 的浓度相等时,反应达到平衡 的浓度相等时,反应达到平衡 |
B.平衡后增大 的浓度, 的浓度, 的转化率增大 的转化率增大 |
C.平衡后加水稀释, 与 与 的浓度之比增大 的浓度之比增大 |
D.可采用加热 溶液的方法实现 溶液的方法实现 的再生 的再生 |
6.无色的亚铜盐的氨水溶液放置一段时间的话,会变成深蓝色的溶液,请解释可能的原因
您最近半年使用:0次



