锂在电池领域的消费量最大,被称为“21世纪的能源金属”。
以β-锂辉矿石(主要成分为Li
2O·Al
2O
3·4SiO
2,还含有铁、镁、铝及钙的氧化物等杂质)为原料来制取碳酸锂的一种工艺流程如图:
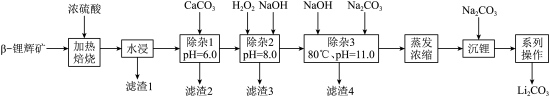
已知:Al
2O
3、SiO
2加热焙烧时不溶于浓硫酸。
浓硫酸的沸点是330℃。
部分金属离子沉淀的pH如下表:
| 金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ | Ca2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 2.2 | 3.7 | 7.5 | 9.6 | 13.37 |
| 沉淀完全时(c=1.0×10-5mol/L)的pH | 3.2 | 4.7 | 9.0 | 11.0 | — |
40.滤渣2的主要成分是
_____,“除杂2”步骤中氧化剂和还原剂的理论物质的量之比是
_____。
已知Li
2CO
3和CaCO
3在不同温度下的K
sp:
| 20℃ | Ksp(Li2CO3)=2.5×10-2 | Ksp (CaCO3)=2.8×10-9 |
| 80℃ | Ksp (Li2CO3)=6.0×10-3 | Ksp (CaCO3)=4.0×10-9 |
41.“除杂3”步骤中,原溶液中Ca
2+和Li
+浓度分别为4.0×10
-4mol·L
-1和5.0mol·L
-1.通过列式计算说明不损失Li
+的情况下,Ca
2+是否能除尽(工业离子除尽要求是浓度小于1.0×10
-6mol·L
-1)
_____。
42.Li
2CO
3在不同温度下的溶解度是:0℃1.54g,20℃1.33g,80℃0.85g,则系列操作为
_____。