1 . 不同元素的第一电离能 如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
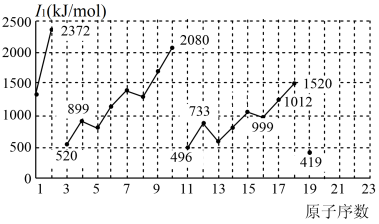
(1)总结同主族内不同元素的 变化的特点
变化的特点______ 。
(2)同周期内,随原子序数增大, 增大。但个别元素的
增大。但个别元素的 出现反常,试预测下列关系中正确的是
出现反常,试预测下列关系中正确的是_______ (填序号)。
① (砷)>
(砷)>  (硒) ②
(硒) ② (砷)<
(砷)<  (硒)
(硒)
③ (溴) >
(溴) >  (硒) ④
(硒) ④ (溴) <
(溴) <  (硒)
(硒)
(3)解释10号元素 较大的原因
较大的原因______ 。
(4)请估计1mol气态基态Ca原子失去最外层一个电子所需能量E的范围______ 。
 如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)总结同主族内不同元素的
 变化的特点
变化的特点(2)同周期内,随原子序数增大,
 增大。但个别元素的
增大。但个别元素的 出现反常,试预测下列关系中正确的是
出现反常,试预测下列关系中正确的是①
 (砷)>
(砷)>  (硒) ②
(硒) ② (砷)<
(砷)<  (硒)
(硒)③
 (溴) >
(溴) >  (硒) ④
(硒) ④ (溴) <
(溴) <  (硒)
(硒)(3)解释10号元素
 较大的原因
较大的原因(4)请估计1mol气态基态Ca原子失去最外层一个电子所需能量E的范围
您最近一年使用:0次
2 . 下表为 、
、 、
、 的部分电离能(
的部分电离能( )数值。
)数值。
分析上表中各元素电离能的变化,回答下列问题:
(1) 、
、 、
、 元素的第一电离能从大到小的顺序是
元素的第一电离能从大到小的顺序是__________
(2)为什么同一元素的各级电离能逐级增大?__________
(3)上表中所呈现的电离能变化规律与三种元素的原子结构有什么关联?__________
 、
、 、
、 的部分电离能(
的部分电离能( )数值。
)数值。| 电离能 | 元素 | ||
 |  |  | |
 | 496 | 738 | 577 |
 | 4562 | 1451 | 1817 |
 | 6912 | 7733 | 2745 |
 | 9543 | 10540 | 11575 |
(1)
 、
、 、
、 元素的第一电离能从大到小的顺序是
元素的第一电离能从大到小的顺序是(2)为什么同一元素的各级电离能逐级增大?
(3)上表中所呈现的电离能变化规律与三种元素的原子结构有什么关联?
您最近一年使用:0次
3 . 试用原子结构的知识解释下列实验事实。
(1)在第2周期元素中,氖的第一电离能最大。_______
(2)磷的第一电离能比硫的第一电离能大。_______
(3)在化学反应中,镁原子通常失去两个电子,形成镁离子( )。
)。_______
(4) 是离子化合物,
是离子化合物, 是共价化合物。
是共价化合物。_______
(1)在第2周期元素中,氖的第一电离能最大。
(2)磷的第一电离能比硫的第一电离能大。
(3)在化学反应中,镁原子通常失去两个电子,形成镁离子(
 )。
)。(4)
 是离子化合物,
是离子化合物, 是共价化合物。
是共价化合物。
您最近一年使用:0次
4 . 在下列空格中,填上适当的元素符号。
(1)在第3周期中,第一电离能最小的元素是_______ ,第一电离能最大的元素是_______ 。
(2)在元素周期表中,电负性最大的元素是_______ ,电负性最小的元素是_______ 。
(3)在第4周期元素中,原子的4p轨道半充满的是_______ ,3d轨道半充满的_______ ,4s轨道半充满的是_______ ,外围电子中s电子数与d电子数相同的是_______ 。
(1)在第3周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)在第4周期元素中,原子的4p轨道半充满的是
您最近一年使用:0次
2022-11-25更新
|
1026次组卷
|
3卷引用:苏教2020版选择性必修2专题2第二单元 元素性质的递变规律课后习题
5 . 回答下列问题:
(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)_______ I1(Cu)(填“大于”或“小于”)。原因是_______ 。
(2)元素Mn与O中,第一电离能较大的是_______ 。
(3)根据元素周期律,原子半径Ga_______ As,第一电离能Ga_______ As(填“大于”或“小于”)。
(4)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是_______ (填元素符号),e的价层电子排布图为_______ 。
(5)第一电离能介于B、N之间的第二周期元素有_______ 种。
(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(2)元素Mn与O中,第一电离能较大的是
(3)根据元素周期律,原子半径Ga
(4)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是
(5)第一电离能介于B、N之间的第二周期元素有
您最近一年使用:0次
21-22高二·全国·课时练习
解题方法
6 . 电离能是指1 mol气态基态原子(或阳离子)失去1 mol电子形成1 mol气态阳离子(或更高价阳离子)所吸收的能量。现有核电荷数小于18的元素A,其电离能(单位为eV·mol-1)数据如下。
(1)外层电子离核越远,能量越高,电离能越_______ (填“大”或“小”);阳离子电荷数越高,再失去电子时,电离能越_______ (填“大”或“小”)。
(2)上述失去的11个电子分属_______ 个电子层。
(3)失去11个电子后,该元素原子核外还有_______ 个电子。
(4)该元素的最高价氧化物对应的水化物的化学式是_______ 。
| I1 | I2 | I3 | I4 | I5 | I6 | I7 | I8 | I9 | I10 | I11 | |
| 电离能 | 7.64 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 | 224.9 | 226.0 | 327.9 | 367.4 | 1761 |
(1)外层电子离核越远,能量越高,电离能越
(2)上述失去的11个电子分属
(3)失去11个电子后,该元素原子核外还有
(4)该元素的最高价氧化物对应的水化物的化学式是
您最近一年使用:0次
21-22高二·全国·课时练习
7 . 回答下列问题:
(1)Mg元素的第一电离能比Al元素的_______ ,第2周期元素中,元素的第一电离能比铍大的有_______ 种。
(2)碳原子的核外电子排布式为_______ 。与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是_______ 。
(3)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:_______ 。
(1)Mg元素的第一电离能比Al元素的
(2)碳原子的核外电子排布式为
(3)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 899 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
您最近一年使用:0次
8 . 回答下列问题:
(1)氮原子价电子的轨道表示式为_______ 。
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第2周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是_______ ;氮元素的E1呈现异常的原因是_______ 。

(1)氮原子价电子的轨道表示式为
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第2周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是

您最近一年使用:0次
解题方法
9 . 按要求完成下列问题。
(1)完成下列关于磷与硫的比较(用“>”或“<”或“=”)。
原子半径:P____ S;非金属性:P___ S;电负性:P____ S;第一电离能:P____ S。
(2)第一电离能介于B、N之间的第二周期元素有_______ 种。
(1)完成下列关于磷与硫的比较(用“>”或“<”或“=”)。
原子半径:P
(2)第一电离能介于B、N之间的第二周期元素有
您最近一年使用:0次
10 . 完成下列填空
(1)写出下列基态原子的核外电子排布式。
Li:___________ ;N:___________ ;Ti:___________ ;Cu___________ 。
(2)钒元素在元素周期表中的位置是___________ 。
(3)X元素位于第三周期,同周期元素中其第一电离能最小,X的元素符号是___________ 。
(1)写出下列基态原子的核外电子排布式。
Li:
(2)钒元素在元素周期表中的位置是
(3)X元素位于第三周期,同周期元素中其第一电离能最小,X的元素符号是
您最近一年使用:0次
2021-10-03更新
|
382次组卷
|
3卷引用:1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)
(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)北京市昌平区2020-2021学年高二下学期期末考试化学试题湖北省潜江市华中师范大学潜江附属中学高二上学期12月月考化学试题



