1 .  在元素周期表中的位置是第
在元素周期表中的位置是第___________ 周期___________ 族,除去稀有气体,Cu元素所在周期原子半径最小的元素是___________ (填写元素符号);元素周期表中电负性大于氧元素的是___________ (填写元素符号)。
 在元素周期表中的位置是第
在元素周期表中的位置是第
您最近一年使用:0次
解题方法
2 . 电负性是由美国化学家鲍林提出的。下列不能根据元素电负性判断的是
| A.元素原子的得电子能力 |
| B.元素形成化合物中的化合价正、负 |
| C.不同元素之间形成的化学键类型 |
| D.氢化物水溶液的酸性 |
您最近一年使用:0次
2024-02-22更新
|
97次组卷
|
2卷引用:河南省濮阳市2023-2024学年高二上学期1月期末化学试题
解题方法
3 . 食用碱是人们生活中常用的食品疏松剂和肉类嫩化剂,其成分为纯碱 和小苏打
和小苏打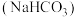 。下列说法正确的是
。下列说法正确的是
 和小苏打
和小苏打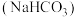 。下列说法正确的是
。下列说法正确的是A.离子半径: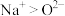 | B.电负性: |
C.非金属性: | D.第一电离能: |
您最近一年使用:0次
2023-12-01更新
|
550次组卷
|
5卷引用:河北省邯郸市六校联考2023-2024学年高二上学期11月月考化学试题
4 . 柠檺酸铁铵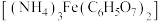 可用作铁质强化剂,以铁、硫酸、柠檬酸、过氧化氢、氨水等为原料可制备柠檬酸铁铵。下列说法中错误的是
可用作铁质强化剂,以铁、硫酸、柠檬酸、过氧化氢、氨水等为原料可制备柠檬酸铁铵。下列说法中错误的是
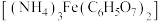 可用作铁质强化剂,以铁、硫酸、柠檬酸、过氧化氢、氨水等为原料可制备柠檬酸铁铵。下列说法中错误的是
可用作铁质强化剂,以铁、硫酸、柠檬酸、过氧化氢、氨水等为原料可制备柠檬酸铁铵。下列说法中错误的是A.基态 的价层电子轨道表示式为 的价层电子轨道表示式为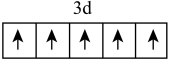 |
| B.铁是金属晶体,硫酸是离子晶体 |
C.电负性: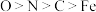 |
D.过氧化氢分子中只存在 键 键 |
您最近一年使用:0次
2023-07-18更新
|
215次组卷
|
3卷引用:海南省省直辖县级行政单位2022-2023学年高二下学期期末考试化学试题
解题方法
5 . 判断化学键的类型。
(1)一般来说,如果两种成键元素的电负性差值大于1.7,它们之间通常形成__________ 。
(2)一般来说,如果两种成键元素的电负性差值小于1.7,它们之间通常形成__________ 。
(1)一般来说,如果两种成键元素的电负性差值大于1.7,它们之间通常形成
(2)一般来说,如果两种成键元素的电负性差值小于1.7,它们之间通常形成
您最近一年使用:0次
解题方法
6 . 主族元素电负性的变化规律
同一周期,主族元素的电负性从左到右依次_______ ,表明其吸引电子的能力逐渐_______ ,_______ 逐渐减弱,_________ 逐渐增强。
同一主族,元素的电负性从上到下呈现_______ 的趋势,表明其吸引电子的能力逐渐_______ ,_______ 逐渐增强,__________ 逐渐减弱。
同一周期,主族元素的电负性从左到右依次
同一主族,元素的电负性从上到下呈现
您最近一年使用:0次
解题方法
7 . 新型冠状病毒疫情已经流行长达三年之久,依然没有很好的解决办法,但是我们需要勤开窗通风,合理使用消毒液,医用酒精等措施来有效的预防病毒,现按要求回答下列问题:
(1)消毒液的组成元素中,基态O原子的电子排布式是_______ ,基态Cl原子未成对电子数为_______ 个
(2)C2H5OH分子中碳原子的杂化方式为_______ ,组成元素电负性大小顺序为_______ ,1mol乙醇分子中含有σ键数目为_______
(3)与氧元素相邻的N元素的第一电离能的大小顺序为_______ (填元素符号),H2O分子的空间构型为_______ ,中心原子的杂化方式为_______ ,熔沸点:H2O_______ H2S(填“>”或“<”)
(4)水中不存在的作用力_______
A.离子键 B.共价键 C.氢键
(1)消毒液的组成元素中,基态O原子的电子排布式是
(2)C2H5OH分子中碳原子的杂化方式为
(3)与氧元素相邻的N元素的第一电离能的大小顺序为
(4)水中不存在的作用力
A.离子键 B.共价键 C.氢键
您最近一年使用:0次
2022-12-02更新
|
745次组卷
|
2卷引用:宁夏银川市景博中学2022-2023学年高二上学期期中考试化学试题
8 . 第四周期的元素形成的化合物在生产生活中有着重要的用途。
(1)镍铬钢抗腐蚀性能强,基态铬原子(24Cr)的核外电子排布式为_______ ,按照电子排布式,镍元素(28Ni)在周期表中位于_______ 区。
(2)硒(34Se)常用作光敏材料,基态硒原子的价电子排布式为_______ 。
(3)“玉兔二号”月球车是通过砷化镓(GaAs)太阳能电池提供能量进行工作的。基态砷原子(33As)的电子占据最高能级的电子云轮廓图为_______ 形。基态镓原子(31Ga)的核外有_______ 个未成对电子。砷的电负性比镓_______ (填“大”或“小”)。
(1)镍铬钢抗腐蚀性能强,基态铬原子(24Cr)的核外电子排布式为
(2)硒(34Se)常用作光敏材料,基态硒原子的价电子排布式为
(3)“玉兔二号”月球车是通过砷化镓(GaAs)太阳能电池提供能量进行工作的。基态砷原子(33As)的电子占据最高能级的电子云轮廓图为
您最近一年使用:0次
9 . 在现代工业中,锰及其化合物应用于国民经济的各个领域,其中钢铁工业是最重要的领域,用锰量占90%—95%,主要作为炼铁炼钢过程中的脱氧剂和脱硫剂。在自然界中,锰有II、III、IV及VII价态,对于基态锰原子,下列叙述错误的是
| A.基态锰原子核外电子的运动状态有25种 |
| B.4s电子能量较高,总是在比3s电子离核更远的地方运动 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
| D.锰元素位于周期表的d区 |
您最近一年使用:0次
2021-12-17更新
|
526次组卷
|
2卷引用:辽宁省名校联盟2021-2022学年高二12月联考化学试题



