名校
解题方法
1 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 酸性: | 电负性: |
B | 碳酸氢钠用作面团膨松剂 | 碳酸氢钠可以与碱反应 |
C | 马口铁(镀锡铁)出现刮痕后浸泡在饱和食盐水中,一段时间后,滴入几滴 | 锡做原电池的负极 |
D | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝会变红色 | 乙醇具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-24更新
|
335次组卷
|
4卷引用:广东省东莞中学、广州二中、惠州一中等六校联考2023-2024学年高三下学期(第六次)开学化学试题
名校
解题方法
2 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH和原子半径、原子序数的关系如图所示。下列说法不正确的是
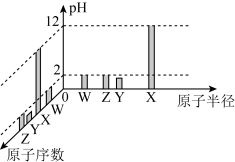

| A.电负性:Z>Y>X |
| B.简单离子的半径:Y>Z>W>X |
| C.同浓度氢化物水溶液的酸性:Z<Y |
| D.Z的单质具有强氧化性 |
您最近一年使用:0次
名校
3 . 现有四种元素的基态原子的电子排布式如下:①[Ne]3s23p3; ②[Ne]3s23p4;③1s22s22p63s23p5。则下列有关比较中正确的是
| A.最高正化合价:①>③>② |
| B.单质氧化性:①>②>③ |
| C.电负性:①>③>② |
| D.最高价氧化物的水合物的酸性:③>②>① |
您最近一年使用:0次
2018-01-31更新
|
404次组卷
|
5卷引用:云南省昆明市官渡区第二中学2023-2024学年高三上学期开学化学试题
(已下线)云南省昆明市官渡区第二中学2023-2024学年高三上学期开学化学试题四川省遂宁市2017-2018学年高二上学期期末考试化学试题山西省大同市第三中学2017-2018学年高二下学期4月月考化学试题内蒙古集宁一中2017-2018学年高二下学期第二次月考理科考试综合化学试题湖北省十堰市六县市区一中教联体2023-2024学年高二上学期12月联考化学试题
真题
名校
4 . 日光灯中用到的某种荧光粉的主要成分为3W3(ZX4)2·WY2。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
| A.电负性:X>Y>Z>W |
| B.原子半径:X<Y<Z<W |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
您最近一年使用:0次
2023-06-16更新
|
11316次组卷
|
25卷引用:江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题
江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题山东省东营市第一中学2023-2024学年高二下学期开学收心考试化学试题2023年高考湖南卷化学真题(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)2023年湖南卷高考真题变式题(选择题6-10)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第19讲元素周期律与元素周期表安徽省亳州市第二完全中学2022-2023学年高二下学期期末考试化学(A卷)试题(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)湖北省武汉市第六中学2023-2024学年高三上学期第一次月考化学试题天津市耀华中学2023-2024学年高三上学期第一次月考化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省厦门第一中学2024届高三上学期10 月月考化学试题河北省迁安市2023-2024学年高三上学期期中考试化学试题福州市福州高级中学2023-2024学年高三上学期10月月考化学试题福建省厦门第一中学2024届高三上学期第一次月考化学试题重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷北京市第二十中学2023-2024学年高三上学期10月月考化学试题(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)福建省福州高级中学2023-2024学年高三上学期第一阶段考试化学试卷(已下线)FHgkyldyjhx12
名校
5 . 某食品添加剂的主要成分为WZ(RY4)2·12X2Y。已知X、Y、Z、R、W为原子序数依次增大的前20号元素,X、Z的周期序数等于主族序数,Y和R位于同主族,基态X、W原子最外层电子排布式为ns1。下列叙述正确的是
| A.原子半径:W>R>Z>Y> X |
| B.电负性:Y>R>X>Z> W |
| C.常温下,Z、W单质都能与水发生置换反应 |
| D.R的最高价氧化物对应水化物一定有强氧化性 |
您最近一年使用:0次
2023-08-16更新
|
252次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高三上学期入学考试(暑假作业检测)化学试题
6 . 日光灯中用到的某种荧光粉的主要成分为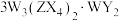 。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
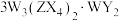 。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是| A.电负性:Y>X>Z>W |
| B.原子半径:X<Y<Z<W |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
您最近一年使用:0次
名校
7 . 下列结构或性质的比较中,正确的是
A.微粒半径: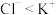 | B.电负性: |
| C.碱性:NaOH>CsOH | D.酸性:HCOOH>CH3COOH |
您最近一年使用:0次
名校
解题方法
8 . 中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转化为甲烷的新型催化转化方法:CO2+4H2=CH4+2H2O,这是迄今最接近人造光合作用的方法。下列有关CO2、CH4的说法正确的是
| A.CO2转化为CH4利用了CO2的氧化性 | B.CO2的空间构型是V形 |
| C.CH4是极性共价键构成的极性分子 | D.电负性由大到小的顺序是C>O>H |
您最近一年使用:0次
名校
9 . 非金属元素形成的相关物质在生产、生活中应用广泛。
(1)上述非金属元素在周期表中处于___________ 区。
(2)卤族元素化合物的性质有相似性和递变性,H-O-X(X代表Cl、Br、I)的酸性随着X的原子序数递增逐渐___________ (填“增强”或“减弱”)。
(3)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,下列判断不正确 的是___________。

(4)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3.NH3极易溶于水的原因是___________ ,反应时,向饱和NaCl溶液中先通入___________ 。
②NaHCO3分解得Na2CO3, 空间结构为
空间结构为___________ 。
(5)NF3的结构与NH3类似,但是性质差异较大。NH3具有碱性(可与H+结合)而NF3没有碱性,原因是___________ 。
(6)离子液体具有较好的化学稳定性、较低的熔点以及对多种物质有良好的溶解性,因此被广泛应用于有机合成、分离提纯以及电化学研究中。下图为某一离子液体的结构。下列判断正确的是___________

| 元素 | H | B | N | F | Cl | Br | I |
| 电负性 | 2.1 | 2.0 | 3.0 | 4.0 | 3.0 | 2.8 | 2.5 |
(2)卤族元素化合物的性质有相似性和递变性,H-O-X(X代表Cl、Br、I)的酸性随着X的原子序数递增逐渐
(3)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,下列判断

| A.NaX均为离子晶体 |
| B.随X半径的增大,NaX的离子键减弱,熔点逐渐降低 |
| C.TiF4的熔点反常升高是由于氢键的作用 |
| D.TiCl4、TiBr4、TiI4的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高 |
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3.NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3,
 空间结构为
空间结构为(5)NF3的结构与NH3类似,但是性质差异较大。NH3具有碱性(可与H+结合)而NF3没有碱性,原因是
(6)离子液体具有较好的化学稳定性、较低的熔点以及对多种物质有良好的溶解性,因此被广泛应用于有机合成、分离提纯以及电化学研究中。下图为某一离子液体的结构。下列判断正确的是___________

| A.该离子液体能与水分子形成氢键 |
| B.该结构中不存在手性碳原子 |
| C.该结构中C原子的轨道杂化类型有3种 |
D. 中存在配位键,B原子的轨道杂化类型为sp3 中存在配位键,B原子的轨道杂化类型为sp3 |
您最近一年使用:0次
20-21高三·江苏·开学考试
10 . 2020年11月6日,长征六号运载火箭成功将NewSat9-18卫星送入预定轨道,提供动力的化学反应为:C2H8N2+2N2O4=3N2+2CO2+4H2O。下列说法错误的是
A.N2的电子式: | B.CO2的空间充填模型: |
| C.氧化性:N2O4>CO2 | D.电负性大小:O>N |
您最近一年使用:0次



 溶液,出现蓝色沉淀
溶液,出现蓝色沉淀

