名校
解题方法
1 . Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Co原子的价电子排布式为_______ ,Co2+核外3d能级上有_____ 对成对电子。
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是________ 。1 mol配离子中所含σ键的数目为________ ,配位体N3-中心原子的杂化类型为________ 。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是_________________________________________________ 。
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为________ ,立方体中Fe2+间连接起来形成的空间构型是________ 。K+空缺率(体心中没有K+的占总体心的百分比)为_____________ 。
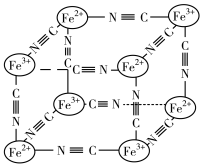
(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为________ 。
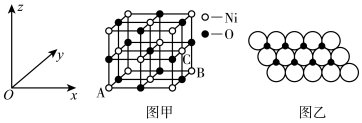
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为________ g(用含a、NA的代数式表示)。
(1)基态Co原子的价电子排布式为
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为

(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为
您最近一年使用:0次
2 . Ⅰ、用下列:①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤Cl2 ⑥Ar ⑦CO2 等物质填空。 (1—4小题填序号)
(1) 由离子键和非极性键构成的是_________________
(2) 由极性键和非极性键构成的是_________________
(3) 不存在化学键的是________
(4) 共价化合物有_________________
(5) 写出下列物质的电子式:Na2O2___________
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,属________ 区元素
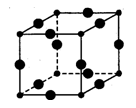
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为____ ,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为_________ g·cm-3。(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)
(1) 由离子键和非极性键构成的是
(2) 由极性键和非极性键构成的是
(3) 不存在化学键的是
(4) 共价化合物有
(5) 写出下列物质的电子式:Na2O2
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为

您最近一年使用:0次



