1 . 洲际弹道导弹DF—31A的制造材料中包含了Fe、Cr、Ni、C等多种元素。
(1)基态铁原子的价电子排布式为___________ ,Cr的未成对电子个数___________ ,Ni位于周期表的___________ 区。
(2)Fe、Co均能与CO形成配合物,如Fe(CO)5、Co2(CO)8,其结构分别如图1、图2所示,

则Fe(CO)5中σ键与π键的个数比___________ ,图2中C的杂化方式有___________ ,形成上述两种化合物的四种元素中电负性最大的是___________ (填元素符号),写出一种与CO互为等电子体的分子___________ 。
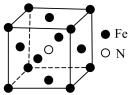
(3)铁与氮形成的化合物的立方晶胞结构如图所示,N位于有Fe构成的___________ 的体心(填“正四面体”或“八面体”或“立方体”),若晶体密度为b ,则顶点Fe与N的距离为
,则顶点Fe与N的距离为__________ pm。(用含NA、b的代数式表示,NA为阿伏加德罗常数的值)
(1)基态铁原子的价电子排布式为
(2)Fe、Co均能与CO形成配合物,如Fe(CO)5、Co2(CO)8,其结构分别如图1、图2所示,

则Fe(CO)5中σ键与π键的个数比
(3)铁与氮形成的化合物的立方晶胞结构如图所示,N位于有Fe构成的
 ,则顶点Fe与N的距离为
,则顶点Fe与N的距离为
您最近一年使用:0次
名校
解题方法
2 . 锗(Ge)、碲化镉(CdTe)等是优良的半导体材料。回答下列问题:
(1)Ge在元素周期表中的位置___________ ,Ge的逐级电离能I4≪I5的原因是___________ 。
(2)经X射线衍射实验证明在碲酸( )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为___________ 。
(3)锗可以形成无机化合物 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为___________ ,锗也可以形成类似于烷烃结构的 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为___________ , 该分子中含有的
该分子中含有的 键数目为
键数目为___________ 。
(4)锗的氯化物 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是___________ , 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有___________ 个。
(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为___________ 空隙(填几何构型名称),若CdTe的摩尔质量为 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离___________ nm。(用含M、 、
、 的代数式表示)
的代数式表示)

(1)Ge在元素周期表中的位置
(2)经X射线衍射实验证明在碲酸(
 )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为(3)锗可以形成无机化合物
 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为 该分子中含有的
该分子中含有的 键数目为
键数目为(4)锗的氯化物
 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为
 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
名校
3 . 二茂铁( )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
(1) 在周期表中的
在周期表中的___________ 区,受热后 的1个
的1个 电子会跃迁至
电子会跃迁至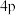 轨道,写出
轨道,写出 的该激发态电子排布式:
的该激发态电子排布式:
___________ 。
(2)铁系元素能与 形成
形成 等金属羰基化合物,已知室温下
等金属羰基化合物,已知室温下 为浅黄色液体,沸点为
为浅黄色液体,沸点为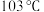 ,则
,则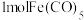 分子中含有
分子中含有___________  键,
键, 中含有的化学键类型包括
中含有的化学键类型包括___________ 。
A.离子键 B.极性共价键 C.配位键 D.金属键
(3)二茂铁的衍生物可和 等微粒产生静电作用,
等微粒产生静电作用, 和
和 的电负性由大到小的顺序为
的电负性由大到小的顺序为___________ ; 中氧原子的杂化方式为
中氧原子的杂化方式为___________ , 空间构型为
空间构型为___________ 。
(4)石墨烯的结构如图甲所示,二维结构内有大量碳六元环相连,每个碳六元环类似于苯环(但无H原子相连),石墨烯的某种氧化物的结构如图乙所示,该物质易溶于水,而石墨烯难溶于水,易溶于非极性溶剂。解释石墨烯及其氧化物的溶解性差异的原因:___________ 。

(5)石墨烷是石墨烯与 发生加成反应的产物,完全氢化的石墨烷具有
发生加成反应的产物,完全氢化的石墨烷具有___________ (填“导电性”“绝缘性”或“半导体性”)。
(6)石墨烯可作电池材料。某锂离子电池的负极材料是将 嵌入到两层石墨烯层中间,石墨烯层间距为
嵌入到两层石墨烯层中间,石墨烯层间距为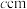 ,其晶胞结构如图所示。其中一个晶胞的质量m=
,其晶胞结构如图所示。其中一个晶胞的质量m=___________ g(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。(1)
 在周期表中的
在周期表中的 的1个
的1个 电子会跃迁至
电子会跃迁至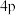 轨道,写出
轨道,写出 的该激发态电子排布式:
的该激发态电子排布式:
(2)铁系元素能与
 形成
形成 等金属羰基化合物,已知室温下
等金属羰基化合物,已知室温下 为浅黄色液体,沸点为
为浅黄色液体,沸点为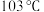 ,则
,则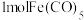 分子中含有
分子中含有 键,
键, 中含有的化学键类型包括
中含有的化学键类型包括A.离子键 B.极性共价键 C.配位键 D.金属键
(3)二茂铁的衍生物可和
 等微粒产生静电作用,
等微粒产生静电作用, 和
和 的电负性由大到小的顺序为
的电负性由大到小的顺序为 中氧原子的杂化方式为
中氧原子的杂化方式为 空间构型为
空间构型为(4)石墨烯的结构如图甲所示,二维结构内有大量碳六元环相连,每个碳六元环类似于苯环(但无H原子相连),石墨烯的某种氧化物的结构如图乙所示,该物质易溶于水,而石墨烯难溶于水,易溶于非极性溶剂。解释石墨烯及其氧化物的溶解性差异的原因:

(5)石墨烷是石墨烯与
 发生加成反应的产物,完全氢化的石墨烷具有
发生加成反应的产物,完全氢化的石墨烷具有(6)石墨烯可作电池材料。某锂离子电池的负极材料是将
 嵌入到两层石墨烯层中间,石墨烯层间距为
嵌入到两层石墨烯层中间,石墨烯层间距为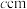 ,其晶胞结构如图所示。其中一个晶胞的质量m=
,其晶胞结构如图所示。其中一个晶胞的质量m= 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
4 . 明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载。锌及其化合物在生产、生活中有着重要的用途。锌是生命体必需的微量元素,被称为“生命之花”。
(1)基态Zn原子核外电子共有____ 种空间运动状态。
(2)锌与铜在周期表中的位置相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10失去1个电子需要的能量由大到小排序是____ (填字母)。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。其中CO 的空间构型为
的空间构型为____ (用文字描述)。与CO 互为等电子体的分子是
互为等电子体的分子是____ (写一种即可)。
(4)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。

①葡萄糖酸锌组成元素中电负性最大的元素为____ ,其中C原子的杂化方式为____ 。
②1mol葡萄糖酸分子中含有____ molσ键。葡萄糖酸的熔点小于葡萄糖酸锌的熔点原因是____ 。
(5)ZnS是一种性能优异的荧光材料,在自然界中有立方ZnS和六方ZnS两种晶型,其晶胞结构如图所示:

①立方ZnS中,Zn2+填充在S2—形成的____ 空隙中;
②六方ZnS的晶体密度为____ g·cm-3(设NA为阿伏加德罗常数的值)。
(1)基态Zn原子核外电子共有
(2)锌与铜在周期表中的位置相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10失去1个电子需要的能量由大到小排序是
| A.④②①③ | B.④②③① | C.①②④③ | D.①④③② |
 的空间构型为
的空间构型为 互为等电子体的分子是
互为等电子体的分子是(4)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。

①葡萄糖酸锌组成元素中电负性最大的元素为
②1mol葡萄糖酸分子中含有
(5)ZnS是一种性能优异的荧光材料,在自然界中有立方ZnS和六方ZnS两种晶型,其晶胞结构如图所示:

①立方ZnS中,Zn2+填充在S2—形成的
②六方ZnS的晶体密度为
您最近一年使用:0次
2022-05-24更新
|
546次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2024届高三上学期一诊模拟考试理综化学试题



