锗(Ge)、碲化镉(CdTe)等是优良的半导体材料。回答下列问题:
(1)Ge在元素周期表中的位置___________ ,Ge的逐级电离能I4≪I5的原因是___________ 。
(2)经X射线衍射实验证明在碲酸( )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为___________ 。
(3)锗可以形成无机化合物 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为___________ ,锗也可以形成类似于烷烃结构的 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为___________ , 该分子中含有的
该分子中含有的 键数目为
键数目为___________ 。
(4)锗的氯化物 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是___________ , 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有___________ 个。
(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为___________ 空隙(填几何构型名称),若CdTe的摩尔质量为 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离___________ nm。(用含M、 、
、 的代数式表示)
的代数式表示)

(1)Ge在元素周期表中的位置
(2)经X射线衍射实验证明在碲酸(
 )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为(3)锗可以形成无机化合物
 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为 该分子中含有的
该分子中含有的 键数目为
键数目为(4)锗的氯化物
 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为
 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离 、
、 的代数式表示)
的代数式表示)
更新时间:2023-10-02 21:09:46
|
相似题推荐
解答题-有机推断题
|
较难
(0.4)
【推荐1】化合物G是一种重要的药物中间体,其合成路线如图:
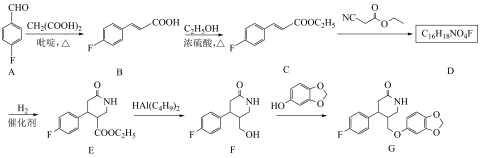
(1)分子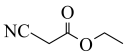 中
中 键和
键和 键数目之比为
键数目之比为___________ 。
(2)F→G的反应类型为___________ 。
(3)C→D发生的反应类型为加成反应,写出D的结构简式___________ 。
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式___________ 。
①能与 溶液发生显色反应,分子中含有1个手性碳原子;②分子中有4种不同化学环境的氢。
溶液发生显色反应,分子中含有1个手性碳原子;②分子中有4种不同化学环境的氢。
(5)已知:①苯酚和 ,
, 不饱和羰基化合物在一定条件下可以发生反应:
不饱和羰基化合物在一定条件下可以发生反应:
① ;②
;②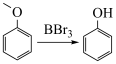 。写出
。写出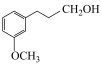 、
、 、和
、和 为原料制备
为原料制备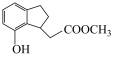 的合成路线流程图
的合成路线流程图________ 。

(1)分子
 中
中 键和
键和 键数目之比为
键数目之比为(2)F→G的反应类型为
(3)C→D发生的反应类型为加成反应,写出D的结构简式
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
①能与
 溶液发生显色反应,分子中含有1个手性碳原子;②分子中有4种不同化学环境的氢。
溶液发生显色反应,分子中含有1个手性碳原子;②分子中有4种不同化学环境的氢。(5)已知:①苯酚和
 ,
, 不饱和羰基化合物在一定条件下可以发生反应:
不饱和羰基化合物在一定条件下可以发生反应:①
 ;②
;② 。写出
。写出 、
、 、和
、和 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】国内外学者近年来对金属-有机框架(MOFs)作为催化剂光解制氢和还原CO2等方面的研究取得了丰硕的成果。其中Masaya 等人利用Ti- MOF-NH2、H2PtCl6、 DMF 等原料制备了催化剂Pt/Ti- MOF-NH2。回答下列问题:
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是___________ ,处于_____ 区,未成对电子数是________ 。
(2)PtCl 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是___________ , 中心原子采用的杂化类型可能是___________ (填 “dsp2”“sp3”“sp2”或“sp3d2”)。

(3)DMF的结构是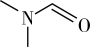 ,σ键与π键的数目比是
,σ键与π键的数目比是___________ ,其中N原子的杂化方式是___________ 。
(4)已知pKa=—lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因______ 。
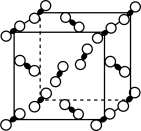
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有___________ 个。若阿伏加德罗常数为NA, 干冰的密度为ρg·cm-3, 则晶胞体对角线长度是___________ cm。
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是
(2)PtCl
 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
(3)DMF的结构是
 ,σ键与π键的数目比是
,σ键与π键的数目比是(4)已知pKa=—lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】以CO2为原料催化加氢可以制备CH4、CH3OH、C2H4,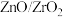 为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
(1)基态 原子电子排布式为
原子电子排布式为______ ,其核外电子空间运动状态有______ 种。
(2)每个基态氧原子含有未成对电子的数目为______ ,同一周期第一电离能大趋势在逐渐增大,但是存在反常,比如 ,请解释原因:
,请解释原因:________________________ 。
(3) 催化加氢制备
催化加氢制备 的化学方程式为
的化学方程式为 。
。
①等物质的量的CH3OH和CO2分子中 键数目之比为
键数目之比为______ 。
②沸点:CH3OH______ (填“>”或“<”)CH4,其原因为______ 。
(4)四方体 晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置,
晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置, 、
、 、
、 原子的坐标参数分别为
原子的坐标参数分别为 、
、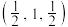 ,
, 。
。

①R原子的坐标参数为______ 。
②假设ZrO2的密度为 ,摩尔质量为
,摩尔质量为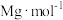 ,
, 表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为
表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为______  (列出算式即可)。
(列出算式即可)。
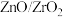 为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:(1)基态
 原子电子排布式为
原子电子排布式为(2)每个基态氧原子含有未成对电子的数目为
 ,请解释原因:
,请解释原因:(3)
 催化加氢制备
催化加氢制备 的化学方程式为
的化学方程式为 。
。①等物质的量的CH3OH和CO2分子中
 键数目之比为
键数目之比为②沸点:CH3OH
(4)四方体
 晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置,
晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置, 、
、 、
、 原子的坐标参数分别为
原子的坐标参数分别为 、
、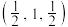 ,
, 。
。
①R原子的坐标参数为
②假设ZrO2的密度为
 ,摩尔质量为
,摩尔质量为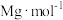 ,
, 表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为
表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为 (列出算式即可)。
(列出算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】碱金属及HNO3、CH3COOH、AsF5等物质可插入石墨层间,所得石墨插层化合物在电池材料、超导性等方面具有广泛的应用前景。回答下列问题:
(1)基态As原子的价电子轨道表示式为___________ , 的空间构型为
的空间构型为___________ ,C、N、O三种元素的第二电离能由小到大的顺序是___________ 。
(2)石墨层的结构如图所示,则石墨中碳原子的杂化类型是___________ ,在层中碳原子的配位数为___________ 。
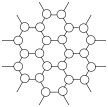
(3)下表列举了部分碳族晶体的熔点数据。
则金刚石、碳化硅、晶体硅的熔点逐渐变小的原因是___________ 。
(4)钾(K)的石墨插层化合物具有超导性,其中K层平行于石墨层,图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。
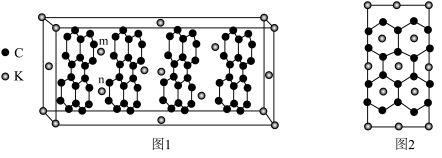
每个晶胞中含有K原子的数目为___________ ,C—C键的键长为anm,则K层中m与n两个K原子之间的距离为___________ nm,设NA为阿伏加德罗常数的值,若晶胞参数分别为xpm、ypm、zpm,则该石墨插层化合物的晶胞密度为___________ g·cm3(用含x、y、z、NA的代数式表示)。
(1)基态As原子的价电子轨道表示式为
 的空间构型为
的空间构型为(2)石墨层的结构如图所示,则石墨中碳原子的杂化类型是

(3)下表列举了部分碳族晶体的熔点数据。
| 晶体 | 熔点/℃ |
| 金刚石(C) | 大于3500 |
| 碳化硅(SiC) | 2830 |
| 晶体硅(Si) | 1412 |
(4)钾(K)的石墨插层化合物具有超导性,其中K层平行于石墨层,图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。

每个晶胞中含有K原子的数目为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】随着环境污染及能源短缺的日益严重,汽车行业掀起了电动车热潮。2020年全球新能源汽车领导者比亚迪推出了“刀片电池”,大幅度提高了续航里程。刀片电池称为超级磷酸铁锂电池,其正极材料为 ,总反应式为:
,总反应式为: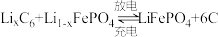 。回答下列问题:
。回答下列问题:
(1)Fe在元素周期表中的位置为___________ 。基态 比
比 结构稳定的原因可解释为
结构稳定的原因可解释为___________ 。
(2) 中Fe的化合价为
中Fe的化合价为___________ ,其离子常用___________ 试剂检验, 的空间构型为
的空间构型为___________ 。
(3)电池负极为嵌入Li的石墨烯层,其晶胞结构如下图。

①石墨烯是由碳原子形成的六元环状二维空间结构,其中C原子的杂化方式为___________ 。
②设 为阿伏加德罗常数的数值,该晶胞密度为
为阿伏加德罗常数的数值,该晶胞密度为___________  (列出计算式即可)。
(列出计算式即可)。
 ,总反应式为:
,总反应式为: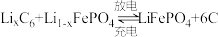 。回答下列问题:
。回答下列问题:(1)Fe在元素周期表中的位置为
 比
比 结构稳定的原因可解释为
结构稳定的原因可解释为(2)
 中Fe的化合价为
中Fe的化合价为 的空间构型为
的空间构型为(3)电池负极为嵌入Li的石墨烯层,其晶胞结构如下图。

①石墨烯是由碳原子形成的六元环状二维空间结构,其中C原子的杂化方式为
②设
 为阿伏加德罗常数的数值,该晶胞密度为
为阿伏加德罗常数的数值,该晶胞密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】化合物X在工业、农业生产中都有重要用途,X由4种常见元素组成,某兴趣小组展开如图实验(气体的体积均在标准状况下测得):

已知:①X的摩尔质量为454g•mol-1;②化合物B常温下是常见的液体;③混合气体C能使品红溶液褪色,气体E能使带火星的木条复燃。
请回答:
(1)白色沉淀F的化学式是____ 。
(2)化合物X的组成元素是___ (填元素符号)。
(3)B的电子式为____ ,其空间构型为____ 。
(4)混合气体C与足量氯水反应的离子方程式是____ 。
(5)化合物X高温分解的化学方程式是____ 。

已知:①X的摩尔质量为454g•mol-1;②化合物B常温下是常见的液体;③混合气体C能使品红溶液褪色,气体E能使带火星的木条复燃。
请回答:
(1)白色沉淀F的化学式是
(2)化合物X的组成元素是
(3)B的电子式为
(4)混合气体C与足量氯水反应的离子方程式是
(5)化合物X高温分解的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钼系催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从废催化剂(主要成分为MoS、NiS、V2O5、Al2O3)中提取V2O3和 ,其工艺流程如图甲所示。
,其工艺流程如图甲所示。

已知:①MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
②高温下,NH4VO3易分解。
③溶液的酸性较强时,+5价钒主要以 的形式存在。
的形式存在。
请回答下列问题:
(1)研磨的目的是_______ (答出一点即可)。
(2)X中生成的气体主要有_______ (填化学式)。
(3)沉钼过程中,发生的主要化学方程式为_______ 。
(4)沉钒过程中,一般要加入过量NH4Cl,其原因是_______ 。
(5)沉钒过程中,沉钒率随溶液pH的变化如图乙所示。沉钒率随溶液pH的增加先升高后降低的原因可能是_______ 。

(6)金属钼的晶胞如图丙所示,已知钼的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则钼原子的配位数是
。则钼原子的配位数是_______ ,钼原子的半径_______ pm。

 ,其工艺流程如图甲所示。
,其工艺流程如图甲所示。
已知:①MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
②高温下,NH4VO3易分解。
③溶液的酸性较强时,+5价钒主要以
 的形式存在。
的形式存在。请回答下列问题:
(1)研磨的目的是
(2)X中生成的气体主要有
(3)沉钼过程中,发生的主要化学方程式为
(4)沉钒过程中,一般要加入过量NH4Cl,其原因是
(5)沉钒过程中,沉钒率随溶液pH的变化如图乙所示。沉钒率随溶液pH的增加先升高后降低的原因可能是

(6)金属钼的晶胞如图丙所示,已知钼的密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则钼原子的配位数是
。则钼原子的配位数是
您最近一年使用:0次
【推荐2】从高铁炉渣(含 、
、 、
、 、
、 、
、 、
、 、
、 等)中回收
等)中回收 及制得
及制得 的工艺流程如下图1所示.
的工艺流程如下图1所示. )
)
回答下列问题:
(1)为提高酸浸效率,可以采取的措施为__________ (答出一条即可)。
(2)除铁外,滤渣2的主要成分为__________ ; 的作用为
的作用为__________ 。
(3)观察图2,常温下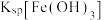
_____ (填“>”“<”或“=”) ;
; 时,溶液中
时,溶液中 的浓度为
的浓度为__________ 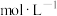 。
。__________ ;煅烧时发生反应的化学方程式为__________ 。
(5)镍能形成多种不同的化合物.图3是镍的一种螯合物(含有多个配位原子的配体与同一中心离子通过螯合配位成环而形成的配合物为螯合物)的结构示意图,图3是一种镍的氧化物的晶胞示意图. 该配合物通过螯合作用形成的配位键为
该配合物通过螯合作用形成的配位键为__________  。
。
②图4所示晶胞的化学式为__________ ;与 配位的
配位的 形成的空间构型为
形成的空间构型为__________ .若晶胞参数 ,该晶体的密度为
,该晶体的密度为__________  (设
(设 为阿伏加德罗常数的值,列出计算式即可)。
为阿伏加德罗常数的值,列出计算式即可)。
 、
、 、
、 、
、 、
、 、
、 、
、 等)中回收
等)中回收 及制得
及制得 的工艺流程如下图1所示.
的工艺流程如下图1所示.
 )
)回答下列问题:
(1)为提高酸浸效率,可以采取的措施为
(2)除铁外,滤渣2的主要成分为
 的作用为
的作用为(3)观察图2,常温下
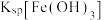
 ;
; 时,溶液中
时,溶液中 的浓度为
的浓度为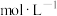 。
。
(5)镍能形成多种不同的化合物.图3是镍的一种螯合物(含有多个配位原子的配体与同一中心离子通过螯合配位成环而形成的配合物为螯合物)的结构示意图,图3是一种镍的氧化物的晶胞示意图.

 该配合物通过螯合作用形成的配位键为
该配合物通过螯合作用形成的配位键为 。
。②图4所示晶胞的化学式为
 配位的
配位的 形成的空间构型为
形成的空间构型为 ,该晶体的密度为
,该晶体的密度为 (设
(设 为阿伏加德罗常数的值,列出计算式即可)。
为阿伏加德罗常数的值,列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】磷和砷的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)红磷是巨型共价分子,无定形结构,下列方法能证明红磷是非晶体的是______ 。
A.质谱法 B.原子发射光谱法 C.核磁共振谱法 D.X射线衍射法
(2) 分子中心原子的杂化方式为
分子中心原子的杂化方式为______ 。
(3)基态 原子的核外电子排布式为
原子的核外电子排布式为______ , 原子的逐级电离能数据如下:
原子的逐级电离能数据如下:
为什么第五电离能与第六电离能相差较大?______ 。
(4)黑磷是新型二维半导体材料,具有片层结构(如图所示), 原子的杂化方式为
原子的杂化方式为______ ,层与层之间的相互作用为______ 。

(5) 的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为______ ,每个 原子周围最近的
原子周围最近的 原子数目为
原子数目为______ ,一个 晶胞中配位键的数目为
晶胞中配位键的数目为______ 。

(6)已知 的密度为
的密度为 ,摩尔质量为
,摩尔质量为 ,阿伏加德罗常数用
,阿伏加德罗常数用 表示,则晶胞中最近的
表示,则晶胞中最近的 和
和 原子核间距为
原子核间距为______  (列式表示)。
(列式表示)。
(1)红磷是巨型共价分子,无定形结构,下列方法能证明红磷是非晶体的是
A.质谱法 B.原子发射光谱法 C.核磁共振谱法 D.X射线衍射法
(2)
 分子中心原子的杂化方式为
分子中心原子的杂化方式为(3)基态
 原子的核外电子排布式为
原子的核外电子排布式为 原子的逐级电离能数据如下:
原子的逐级电离能数据如下:第一电离能 | 第二电离能 | 第三电离能 | 第四电离能 | 第五电离能 | 第六电离能 |
| 947.0 | 1798 | 2735 | 4837 | 6043 | 12310 |
(4)黑磷是新型二维半导体材料,具有片层结构(如图所示),
 原子的杂化方式为
原子的杂化方式为
(5)
 的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为 原子周围最近的
原子周围最近的 原子数目为
原子数目为 晶胞中配位键的数目为
晶胞中配位键的数目为
(6)已知
 的密度为
的密度为 ,摩尔质量为
,摩尔质量为 ,阿伏加德罗常数用
,阿伏加德罗常数用 表示,则晶胞中最近的
表示,则晶胞中最近的 和
和 原子核间距为
原子核间距为 (列式表示)。
(列式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有_______ 种,若其电子排布式表示为[ Ne]3s2 违背了
违背了_______ 。
(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3_______ SiCl4(填“>”或“<”),与SiCl4互为等电子体的离子为_______ (任写1种即可)。已知电负性:H>Si,则SiHCl3充分水解的化学方程式为_______ 。
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是_______ (填字母标号)。
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度_______ (填“高”或“低”),解释原因_______ 。
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则r(Ti3+)为_______ D,该氮化钛的密度_______ g· cm-3(列出计算式即可)。

(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有
 违背了
违背了(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则r(Ti3+)为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】Ⅰ.硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是___________ ,最高能级电子所在的原子轨道为___________ 形。
(2)①硫单质的一种结构为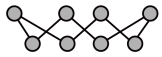 ,S原子杂化方式为
,S原子杂化方式为___________ ; 分子的空间构型是
分子的空间构型是___________ 。
② 、
、 、
、 键角由大到小的顺序是
键角由大到小的顺序是___________ 。
③比较沸点高低: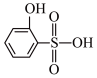
___________ (填“>”或“<”)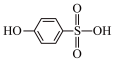 。
。
(3)Fe位于周期表的___________ 区,基态Fe原子的核外电子有___________ 种空间运动状态,Fe与CO形成的化合物Fe(CO)5常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于___________ (填晶体类型)。
(4)ZnS晶胞如图所示:
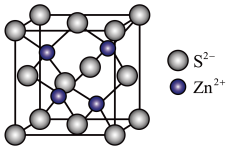
①由图可知,每个 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有___________ 个。
②已知该晶胞密度为 ,阿伏加德罗常数为NA,则晶胞边长为
,阿伏加德罗常数为NA,则晶胞边长为___________ pm。
(学法题)根据所学知识分析归纳,计算晶体密度的关键是___________
(5)早在西汉时期的《淮南万毕术》中记载“曾青得铁则化为铜”,这是有关“湿法炼铜”最早文献记录。若向盛有硫酸铜的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。
①写出蓝色沉淀溶解的离子方程式___________ ;
②若向该深蓝色透明溶液中加入溶剂___________ ,将有深蓝色晶体析出,写出该晶体的化学式___________ 。
(1)基态硫原子的价层电子排布图是
(2)①硫单质的一种结构为
 ,S原子杂化方式为
,S原子杂化方式为 分子的空间构型是
分子的空间构型是②
 、
、 、
、 键角由大到小的顺序是
键角由大到小的顺序是③比较沸点高低:

 。
。(3)Fe位于周期表的
(4)ZnS晶胞如图所示:

①由图可知,每个
 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有②已知该晶胞密度为
 ,阿伏加德罗常数为NA,则晶胞边长为
,阿伏加德罗常数为NA,则晶胞边长为(学法题)根据所学知识分析归纳,计算晶体密度的关键是
(5)早在西汉时期的《淮南万毕术》中记载“曾青得铁则化为铜”,这是有关“湿法炼铜”最早文献记录。若向盛有硫酸铜的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。
①写出蓝色沉淀溶解的离子方程式
②若向该深蓝色透明溶液中加入溶剂
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】I.非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态 原子核外电子的运动状态有
原子核外电子的运动状态有___________ 种
(2) 、
、 、
、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为___________ 。
(3) 中
中 的杂化类型是
的杂化类型是___________ ; 分子的空间结构为
分子的空间结构为___________ 。
(4) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) ,原因是
,原因是___________ 。
II.过渡金属元素铬()是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(5)对于基态 原子,下列叙述正确的是
原子,下列叙述正确的是___________ 。
A.轨道处于半充满时体系总能量低,核外电子排布应为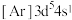
B. 电子能量较高,总是在比
电子能量较高,总是在比 电子离核更远的地方运动
电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(1)基态
 原子核外电子的运动状态有
原子核外电子的运动状态有(2)
 、
、 、
、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(3)
 中
中 的杂化类型是
的杂化类型是 分子的空间结构为
分子的空间结构为(4)
 的熔、沸点
的熔、沸点 ,原因是
,原因是II.过渡金属元素铬()是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(5)对于基态
 原子,下列叙述正确的是
原子,下列叙述正确的是A.轨道处于半充满时体系总能量低,核外电子排布应为
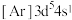
B.
 电子能量较高,总是在比
电子能量较高,总是在比 电子离核更远的地方运动
电子离核更远的地方运动C.电负性比钾高,原子对键合电子的吸引力比钾大
您最近一年使用:0次



