名校
解题方法
1 . 硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:________ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是__________ 。
(3)BF3分子中中心原子的杂化轨道类型是____ 。又知若有d轨道参与杂化,能大大提高中心原子的成键能力,分析BF3、SiF4水解的产物中, 除了相应的酸外,前者生成BF4-而后者生成SiF62-的原因:_______________ 。
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为_________ ,其中三种元素的电负性由大到小的顺序是_______________ 。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是______________ (填字母)。

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
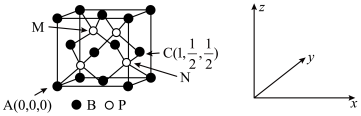
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的_____ (填“立方体”“正四面体”或“正八面体”)空隙。建立如图所示坐标系,可得晶胞中A、C处原子的分数坐标,则N处的P原子分数坐标为______ 。若晶胞中硼原子和磷原子之间的最近核间距为a pm,则晶胞边长为____________ cm。
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是
(3)BF3分子中中心原子的杂化轨道类型是
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的

您最近一年使用:0次
2020-04-09更新
|
197次组卷
|
2卷引用:安徽省合肥市肥东县综合高中2021-2022学年高三下学期期中考试理科综合化学试题
名校
2 . 一种新型陶瓷的化学成分为BN晶体,该晶体具有高熔点、高硬度的特性,关于BN晶体的说法不正确的是( )
| A.该晶体为原子晶体,具有金刚石的结构特征 |
| B.该晶体中B的杂化类型是sp2杂化 |
| C.该晶体中存在配位键 |
| D.该晶体可作耐高温、耐磨材料 |
您最近一年使用:0次
2018-04-19更新
|
896次组卷
|
6卷引用:安徽省滁州市定远县育才学校2021-2022学年高二分层班下学期期中考试化学试题
安徽省滁州市定远县育才学校2021-2022学年高二分层班下学期期中考试化学试题黑龙江省牡丹江市第一高级中学2017-2018学年高二4月月考化学试题吉林省白山市第七中学2018-2019学年高二下学期期中考试化学试题高二选择性必修2(人教版2019)第三章 晶体结构与性质 专题2 晶体类型的判断与晶胞结构的有关计算(已下线)3.2 分子晶体与共价晶体(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)浙江省宁波市北仑中学2021-2022学年高二上学期期中考试化学(育英班)试题



