1 . 以下哪个说法是正确的
| A.同核双原子分子的分子轨道,如果对于分子中心反对称,那么是反键轨道 |
| B.杂化轨道是体系几何构型的反映,它不是真实存在的 |
| C.分子的几何构型可通过计算中心原子的价层电子对数来判断 |
D.根据电子云的重叠形式可以把共价键分成 和 和 成键形式 成键形式 |
您最近半年使用:0次
解题方法
2 . VIA族的氧、硫、硒(Se)、碲(Te)等元素的化合物在科学研究和工业生产中有许多重要用途。回答下列问题:
(1)基态O原子中,未成对电子数与成对电子数之比为_______ 。
(2)亚硫酰氯 在有机合成中有重要应用,分子中S原子的杂化轨道类型为
在有机合成中有重要应用,分子中S原子的杂化轨道类型为_______ ,分子的空间结构为_______ 。
(3)气态电中性基态原子得到一个电子转化为气态基态负离子所放出的能量叫做第一电子亲和能。S、Se、Te三种元素的第一电子亲和能由大到小的顺序是_______ , 、
、 和
和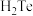 键角最小的是
键角最小的是_______ ,稳定性最强的是_______ 。
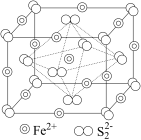
(4)黄铁矿是工业生产硫酸的原料,其晶胞结构如图所示,晶胞参数为anm,该晶体的电子式为_______ , 的配位数为
的配位数为_______ ,晶体的密度为_______  ,在1个晶胞中,由
,在1个晶胞中,由 围成的正八面体的个数为
围成的正八面体的个数为_______ 。
(1)基态O原子中,未成对电子数与成对电子数之比为
(2)亚硫酰氯
 在有机合成中有重要应用,分子中S原子的杂化轨道类型为
在有机合成中有重要应用,分子中S原子的杂化轨道类型为(3)气态电中性基态原子得到一个电子转化为气态基态负离子所放出的能量叫做第一电子亲和能。S、Se、Te三种元素的第一电子亲和能由大到小的顺序是
 、
、 和
和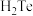 键角最小的是
键角最小的是(4)黄铁矿是工业生产硫酸的原料,其晶胞结构如图所示,晶胞参数为anm,该晶体的电子式为
 的配位数为
的配位数为 ,在1个晶胞中,由
,在1个晶胞中,由 围成的正八面体的个数为
围成的正八面体的个数为
您最近半年使用:0次
名校
解题方法
3 . 据报道,新疆南部发现稀有金属、铅、锌、铁、锰和金矿带约600 m。回答下列问题:
(1)基态锰的价层电子排布式为___________ ;预测:锰的第三电离能( )
)________ (填“大于”“小于”或“等于”)铁的第三电离能( )。
)。
(2)氧化锰能催化氧化HCHO生成 和
和 。
。
①等物质的量的HCHO、 分子中
分子中 键数目之比为
键数目之比为____________________ 。
②在HCHO、 、
、 中,空间构型呈V形的分子是
中,空间构型呈V形的分子是____________________ 。
③HCHO中C原子的杂化类型是____________________ 。
(3) [Zn(NH3)4]SO4中不存在的作用力类型是____________________ (填字母)。
A.非极性键 B.配位键 C.离子键 D.金属键
(4)配合物在水中的颜色与d轨道的分裂能有关。d轨道的分裂能是1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量。预测分裂能:
_______ (填“>”“<”或“=”) ,理由是
,理由是_________________ 。
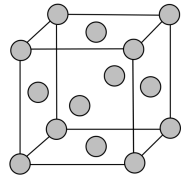
(5)铅晶胞如图所示。
已知:铅晶胞密度为 ,
, 代表阿伏加德罗常数的值。
代表阿伏加德罗常数的值。
晶胞中两个面心上铅原子的最短距离为__________________ pm。
(1)基态锰的价层电子排布式为
 )
) )。
)。(2)氧化锰能催化氧化HCHO生成
 和
和 。
。①等物质的量的HCHO、
 分子中
分子中 键数目之比为
键数目之比为②在HCHO、
 、
、 中,空间构型呈V形的分子是
中,空间构型呈V形的分子是③HCHO中C原子的杂化类型是
(3) [Zn(NH3)4]SO4中不存在的作用力类型是
A.非极性键 B.配位键 C.离子键 D.金属键
(4)配合物在水中的颜色与d轨道的分裂能有关。d轨道的分裂能是1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量。预测分裂能:

 ,理由是
,理由是(5)铅晶胞如图所示。
已知:铅晶胞密度为
 ,
, 代表阿伏加德罗常数的值。
代表阿伏加德罗常数的值。晶胞中两个面心上铅原子的最短距离为

您最近半年使用:0次



