名校
解题方法
1 . 由原子序数依次增大的短周期元素X、Y、Z、W、R组成的一种离子液体(其阳离子中五元环上5个原子共面),其结构如图。Z的最简单氢化物易液化,可用作制冷剂。W的氢化物的水溶液能腐蚀玻璃,Z、R为同一主族元素。下列说法错误的是
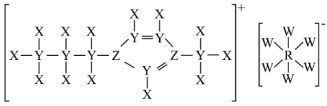
| A.电负性:W>Z>Y |
| B.该离子液体中的Z原子的杂化方式均为sp2 |
C.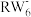 空间结构为正八面体形 空间结构为正八面体形 |
| D.最简单氢化物的沸点:Z<R |
您最近一年使用:0次
2024-05-26更新
|
199次组卷
|
3卷引用:河北省石家庄市河北正定中学2023-2024学年高三下学期4月模拟考试化学试题
名校
解题方法
2 . 下列化学用语表示正确的是
A. 分子的空间结构模型; 分子的空间结构模型; |
B.基态Cu原子的价层电子的轨道表示式: |
C.Cl-Cl形成的p-pσ键模型: |
D.用电子式表示 的形成过程: 的形成过程: |
您最近一年使用:0次
解题方法
3 . 下列表示不正确 的是
A.质子数为92、中子数为146的U原子: |
B.HClO的电子式: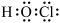 |
C.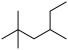 的名称:2,2,4-三甲基己烷 的名称:2,2,4-三甲基己烷 |
D.H2S的价层电子对互斥(VSEPR)模型: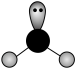 |
您最近一年使用:0次
2024-05-13更新
|
701次组卷
|
3卷引用:河北省重点高中2023-2024学年高三下学期5月高考模拟化学试题(二)
名校
4 . 氢元素有氕(H)、氘(D)、氚(T)三种核素,NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24LT2含有的中子数为0.4NA |
| B.1gD2O中,中心原子上的孤电子对数为0.2 NA |
| C.1L0.1mol/LFeCl3溶液中含有的Fe3+数为0.1NA |
| D.电解水(H2O)生成0.2gH2,外电路通过的电子数为0.1NA |
您最近一年使用:0次
名校
解题方法
5 . 下列化学用语表述错误的是
A.CO2的电子式: |
B.中子数为20的氯原子: Cl Cl |
C.PH3分子的VSEPR模型: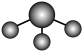 |
D.基态Fe原子的价层电子排布图: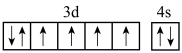 |
您最近一年使用:0次
2023-09-15更新
|
1072次组卷
|
3卷引用:河北省唐山市2023-2024学年高三上学期摸底演练化学试题
河北省唐山市2023-2024学年高三上学期摸底演练化学试题河北省衡水市武强中学2023-2024学年高三上学期期末考试化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
6 . 羟胺 易溶于水,其水溶液是比肼还弱的碱溶液。羟胺可与
易溶于水,其水溶液是比肼还弱的碱溶液。羟胺可与 形成
形成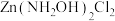 ,已知反应:
,已知反应: 。下列有关说法正确的是
。下列有关说法正确的是
 易溶于水,其水溶液是比肼还弱的碱溶液。羟胺可与
易溶于水,其水溶液是比肼还弱的碱溶液。羟胺可与 形成
形成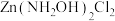 ,已知反应:
,已知反应: 。下列有关说法正确的是
。下列有关说法正确的是A. 很稳定是因为分子间含有氢键 很稳定是因为分子间含有氢键 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 与 与 中 中 的键角相同 的键角相同 |
D. 、 、 与 与 的VSEPR模型相同 的VSEPR模型相同 |
您最近一年使用:0次
2023-05-11更新
|
434次组卷
|
5卷引用:河北省衡水市部分重点高中2023届高三二模化学试题
河北省衡水市部分重点高中2023届高三二模化学试题辽宁省抚顺市重点高中六校协作体2023届高三下学期二模联考化学试题(已下线)选择题6-10(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)第4讲 空间构型
名校
解题方法
7 . 下列说法正确的是
A. 的 的 模型为四面体形,属于极性分子 模型为四面体形,属于极性分子 |
B. 中σ键类型为“头碰头”形式形成的 中σ键类型为“头碰头”形式形成的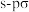 键和 键和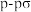 键 键 |
C. 的空间构型为正四面体形,键角是 的空间构型为正四面体形,键角是 |
D.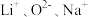 的离子半径依次增大 的离子半径依次增大 |
您最近一年使用:0次
2022-09-05更新
|
272次组卷
|
4卷引用:河北省昌黎第一中学2023届高三下学期第五次调研考试化学试题
名校
解题方法
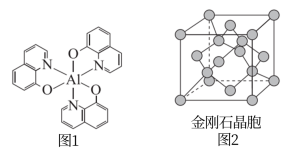
8 . 光电材料在能源军事等领域有重要应用,分为无机光电材料如ZnS、ZnSe、GaAs、 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:
(1)基态Zn原子的价层电子排布图为_____ ;Ga、As、Se的第一电离能由大到小的顺序为___________ 。
(2)图1所示化合物中所含有的化学键类型有_____ (填选项字母),N原子的杂化方式为_____ 。
A.共价键 B.离子键 C.配位键 D.氢键
(3)在水溶液中,以 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:
①表中氧化物之间沸点差异的原因为___________ 。
② 的VSEPR模型为
的VSEPR模型为___________ 。
③ 和
和 分子中,键角更大的是
分子中,键角更大的是___________ 。
(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为___________ 。
②若阿伏加德罗常数的值为 ,ZnS晶体的密度为
,ZnS晶体的密度为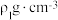 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为___________ 。
 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:(1)基态Zn原子的价层电子排布图为
(2)图1所示化合物中所含有的化学键类型有
A.共价键 B.离子键 C.配位键 D.氢键

(3)在水溶液中,以
 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:| 氧化物 |  |  |  |
| 沸点/℃ | 100 | -10 | -78.5 |
②
 的VSEPR模型为
的VSEPR模型为③
 和
和 分子中,键角更大的是
分子中,键角更大的是(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为
②若阿伏加德罗常数的值为
 ,ZnS晶体的密度为
,ZnS晶体的密度为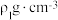 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
您最近一年使用:0次
2022-03-23更新
|
295次组卷
|
2卷引用:河北省张家口市2022届高三第一次模拟考试化学试题
名校
解题方法
9 . 铜是人类广泛使用的第一种金属,含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)基态 原子最高能层的电子排布式为
原子最高能层的电子排布式为___________ 。
(2) 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。
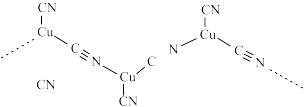
(3) 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为___________ 。
(4)铜能与拟卤素 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸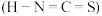 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为___________ ;写出一种与 互为等电子体的分子式
互为等电子体的分子式___________ 。
(5) 可形成
可形成 ,其中
,其中 代表
代表 。
。
①该化合物分子中, 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有___________ 个。
②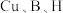 的电负性由大到小的顺序为
的电负性由大到小的顺序为___________ 。
(6)一种由 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
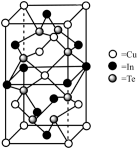
① 的配位数为
的配位数为___________ ;晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ 。
②若晶胞底边的边长均为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态
 原子最高能层的电子排布式为
原子最高能层的电子排布式为(2)
 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。A. | B. | C. | D. |
 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为
(4)铜能与拟卤素
 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸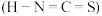 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为 互为等电子体的分子式
互为等电子体的分子式(5)
 可形成
可形成 ,其中
,其中 代表
代表 。
。①该化合物分子中,
 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有②
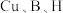 的电负性由大到小的顺序为
的电负性由大到小的顺序为(6)一种由
 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
①
 的配位数为
的配位数为 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为②若晶胞底边的边长均为
 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2021-12-03更新
|
1002次组卷
|
5卷引用:河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题
河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题河北省石家庄市2022届高三上学期教学质量检测(一)化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】20(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广东省佛山市李兆基中学、郑裕彤中学两校2021-2022学年高三下学期3月联考化学试题



