1 . 下列分子或离子之间互为等电子体的是
| A.CS2和 NO2 | B.NH3和 NH | C.N2和 CO | D.CO2 和 SO2 |
您最近一年使用:0次
解题方法
2 . 下列判断正确的是( )
| A.BF3是三角锥形分子 |
| B.铵根离子呈平面形结构 |
| C.甲烷分子中的4个C-H键都是氢原子的1s轨道与碳原子的p轨道形成的s-pσ键 |
| D.甲烷分子中的4个C-H键都是氢原子的1s轨道与碳原子的4个sp3杂化轨道重叠形成的σ键 |
您最近一年使用:0次
2020-12-10更新
|
370次组卷
|
5卷引用:江苏省盐城市东台市创新学校2019-2020学年高二下学期5月份月检测化学试题
江苏省盐城市东台市创新学校2019-2020学年高二下学期5月份月检测化学试题辽宁省南台、岫二、牛庄、海城三中、腾鳌、析木等高级中学2020-2021学年高二上学期期末考试化学试题(已下线)第2章 微粒间相互作用与物质性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)专题4 综合检测(提升卷)福建省建瓯市芝华中学2021-2022学年高二下学期第一次阶段考化学试题
名校
解题方法
3 . 甲烷分子(CH4)失去一个H+,形成甲基阴离子( ),在这个过程中,下列描述不合理的是
),在这个过程中,下列描述不合理的是
 ),在这个过程中,下列描述不合理的是
),在这个过程中,下列描述不合理的是| A.碳原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
您最近一年使用:0次
2020-10-24更新
|
254次组卷
|
10卷引用:福建省龙海市第二中学2019-2020学年高二下学期期末考试化学试题
福建省龙海市第二中学2019-2020学年高二下学期期末考试化学试题(已下线)2012-2013学年湖北省武汉二中高二下学期期中考试化学试卷(已下线)2013-2014学年湖北省襄阳市四校高二下学期期中联考化学试卷(已下线)2014届江苏省启东中学第二学期期中考试高二化学试卷2016届安徽省六安一中高三上第四次月考化学试卷河北省唐山市第一中学2016-2017学年高二下学期期中考试化学试题河北省唐山一中2016-2017学年高二下学期期中考试化学试题福建省晋江市季延中学2018-2019学年高二下学期期中考试化学试题(已下线)第2章 微粒间相互作用与物质性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)福建省建瓯市芝华中学2021-2022学年高二下学期第一次阶段考化学试题
名校
解题方法
4 . 下列分子或离子中,VSEPR模型名称与分子或离子的立体构型名称不一致的是
| A.CO2 | B.H2O | C. | D.CCl4 |
您最近一年使用:0次
2020-09-07更新
|
797次组卷
|
32卷引用:2014-2015学年陕西西北大学附中高二下期末化学试卷
2014-2015学年陕西西北大学附中高二下期末化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题陕西省黄陵中学2017-2018学年高二(重点班)下学期期末考试化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高二上学期期末考试化学试题湖北省沙市中学2019-2020学年高二上学期期末考试化学试题福建省福州第一中学2019-2020学年高二下学期期末考试化学试题新疆昌吉回族自治州呼图壁县第一中学2019-2020学年高二下学期期末考试化学试题2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年辽宁省葫芦岛市六校协作体联考高二下期中化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测【全国百强校】福建省三明市第一中学2019届高三第二次返校考试化学试题【全国百强校】福建省厦门第一中学2018-2019学年高二上学期期中考试化学试题内蒙古包头市包钢第四中学2018-2019学年高二下学期4月月考化学试题辽宁省凌源市第二高级中学2019-2020学年高二下学期第二次网测化学试题宁夏银川市长庆高级中学2019-2020学年高二下学期期中考试化学试题山东省泰安市2020届高三第二次模拟考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题(已下线)练习14 分子的空间结构-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题(已下线)模块同步卷12 综合检测卷(提升卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)福建省建瓯市芝华中学2020-2021学年高二下学期第一阶段考试化学试题四川省西昌市2020-2021学年高二下学期期中检测化学试题海南省东方中学2021-2022学年高二下学期第一次月考化学试题新疆莎车县第一中学2021-2022学年高二下学期期中考试化学试题天津市宁河区芦台第一中学2021-2022学年高二下学期线上第一次月考化学试题贵州省凯里学院附属中学2021-2022学年高二下学期3月月考化学试题新疆疏勒县实验学校2021-2022学年高二下学期期中考试化学试题广东省湛江市第二中学2021-2022学年高二下学期第14周(5.21)周练化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题山东省临沂市平邑县第一中学西校区2023-2024学年高二下学期四月份阶段性考试化学试题
名校
5 . 下列说法中正确的是
| A.气体单质中,一定有σ 键,可能有π 键 |
| B.PCl3分子是非极性分子 |
| C.甲醛(HCHO)、苯和二氧化碳中碳原子均采用 sp2杂化 |
D. 的 VSEPR 模型与离子的空间立体构型一致 的 VSEPR 模型与离子的空间立体构型一致 |
您最近一年使用:0次
2020-09-01更新
|
483次组卷
|
2卷引用:四川省成都外国语学校2019-2020学年高二5月月考化学试题
名校
解题方法
6 . 按要求填空:
(1)质量数为37的氯原子符号为
(2)NH 的电子式
的电子式
(3)X射线衍射测定等发现,I3AsF6中存在I 离子。I
离子。I 离子的几何构型为
离子的几何构型为
(4)与O3分子互为等电子体的一种阴离子为
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-C1键的键能(242.7kJ/mol),原因是
您最近一年使用:0次
2020-08-23更新
|
297次组卷
|
2卷引用:陕西省西安市西安高新第一中学2018-2019学年高二下学期期末考试化学试题
名校
解题方法
7 . 下列分子中的中心原子的杂化方式为sp杂化,分子的空间构型为直线形且分子中没有形成π键的是
| A.CH≡CH | B.CH2=CH2 | C.BeCl2 | D.NH3 |
您最近一年使用:0次
名校
解题方法
8 . 用价层电子对互斥理论判断NO 的立体构型
的立体构型
 的立体构型
的立体构型| A.正四面体 | B.V形 | C.三角锥形 | D.平面三角形 |
您最近一年使用:0次
2020-08-19更新
|
116次组卷
|
5卷引用:河北省唐山市路北区第十一中学2019-2020学年高二下学期期末考试化学试题
河北省唐山市路北区第十一中学2019-2020学年高二下学期期末考试化学试题(已下线)练习14 分子的空间结构-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)新疆疏勒县第一中学2020--2021学年高二下学期期末考试化学试题四川省雅安中学2022-2023学年高二上学期10月月考化学试题广东省湛江市第二中学2021-2022学年高二下学期第14周(5.21)周练化学试题
解题方法
9 . W、X、Y、Z为原子序数依次增大的短周期主族元素,其原子序数之和为30,w与X、Y、Z都能形成二元共价化合物,Y、W形成的常见化合物溶于水显碱性,Z为p区元素,其基态原子有1个未成对电子,四种元素形成的某种化合物Q的结构式为 。回答下列问题:
。回答下列问题:
(1)四种元素中不属于p区的为______ (填元素名称),未成对电子数目最多的基态原子的电子排布式为______ ,同周期第一电离能介于X和Y之间的元素有_______ 种。
(2)XZ3中心原子杂化方式为________ , YW3分子空间构型为__________ 。
(3) Q分子中含有的化学键有_________ 。
 。回答下列问题:
。回答下列问题:(1)四种元素中不属于p区的为
(2)XZ3中心原子杂化方式为
(3) Q分子中含有的化学键有
您最近一年使用:0次
解题方法
10 . 下列微粒的空间构型与 相同的是
相同的是
 相同的是
相同的是A.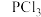 | B.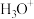 | C. | D. |
您最近一年使用:0次



