名校
解题方法
1 . 下表中各粒子对应的空间结构及解释均正确的是
| 选项 | 粒子 | 空间结构 | 解释 |
| A | 氨基负离子( ) ) | 直线形 | N原子采取 杂化 杂化 |
| B | 二氧化硫( ) ) | V形 | S原子采取 杂化 杂化 |
| C | 碳酸根离子( ) ) | 三角锥形 | C原子采取 杂化 杂化 |
| D | 乙炔( ) ) | 直线形 | C原子采取 杂化且C原子的价电子均参与成键 杂化且C原子的价电子均参与成键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-07更新
|
295次组卷
|
27卷引用:2015-2016学年江苏省泰州中学高二下期中化学试卷
2015-2016学年江苏省泰州中学高二下期中化学试卷四川省新津中学2019-2020学年高二下学期4月月考(入学)化学试题四川省成都外国语学校2019-2020学年高二下学期期中考试化学试题陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题四川绵阳南山中学双语学校2020-2021学年高二上学期10月月考化学试题湖南师范大学附属中学2020-2021学年高二上学期第三次大练习化学试题湖南省邵阳市新邵县2021-2022学年高二上学期期末考试化学试题天津市耀华中学2022-2023学年高二上学期期末考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 B素养拓展区河南省名校联盟2020-2021学年高二下学期开学考试化学试题(已下线)2.2 分子的空间结构(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)山东省泰安市宁阳一中2020-2021学年高二下学期3月月考化学试题(已下线)作业04 分子的空间结构-2021年高二化学暑假作业(人教版2019)(已下线)2.2.2 杂化轨道理论(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第2.2.2讲 杂化轨道理论-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)专题4 分子空间结构与物质性质 专题强化练5 分子(离子)的空间结构与杂化轨道类型的判断第二节 分子的空间结构 第2课时 杂化轨道理论福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(1卷)试题陕西省武功县普集高级中学2022-2023学年高二下学期第一次月考化学试题广东省阳山县南阳中学2022-2023学年高二下学期第一次月考化学试题广东省深圳龙岗四校2022--2023学年高二下学期期中考试化学试题安徽省颍上第一中学2022-2023学年高二下学期5月月考化学试题黑龙江省大庆市肇州县第二中学2023-2024学年高二上学期12月月考化学试题湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题四川省内江市威远县威远中学校2023-2024学年高二下学期第一次月考化学试卷四川省绵阳市东辰学校2023-2024学年高二上学期第四次月考化学试题
名校
解题方法
2 . 下列图像正确的是
A. 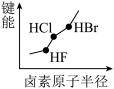 | B. 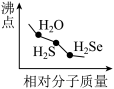 |
C. 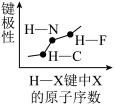 | D. 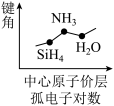 |
您最近一年使用:0次
2023-03-26更新
|
424次组卷
|
9卷引用:山东省济宁市兖州区2019-2020学年高二5月阶段性测试化学试题
山东省济宁市兖州区2019-2020学年高二5月阶段性测试化学试题江苏省泰州中学2020-2021学年高一下学期期末考试化学试题河北省沧州市2021-2022学年高二下学期期末考试化学试题(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)黑龙江省佳木斯市第十二中学2021-2022学年高二下学期期中考试化学试题河南省洛阳强基联盟2022-2023学年高二下学期3月联考化学试题湖北省宜昌市协作体2022-2023学年高二下学期期中考试化学试题湖南省岳阳市郡华学校2023-2024学年高二下学期入学考试化学试题江西省萍乡市2023-2024学年高二下学期4月期中考试化学试题
2008·全国·高考真题
3 . 下列叙述中正确的是
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的稳定性依次增强 |
| D.CS2、H2O、C2H2都是直线形分子 |
您最近一年使用:0次
2022-10-18更新
|
2599次组卷
|
78卷引用:2011-2012学年新疆农七师高级中学高二下学期期末考试试化学试卷
(已下线)2011-2012学年新疆农七师高级中学高二下学期期末考试试化学试卷(已下线)2012-2013学年河北省衡水市第十四中学高二下学期期末考试化学试卷(已下线)2012-2013学年河北省唐山市第一中学高二下学期期末考试化学试卷陕西省黄陵中学2017-2018学年高二(重点班)下学期期末考试化学试题云南省普洱市孟连县一中2018-2019学年高二下学期期末考试化学试题云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一模块(期末)考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题安徽省六安中学2019-2020学年高二下学期期末考试化学试题新疆昌吉回族自治州呼图壁县第一中学2019-2020学年高二下学期期末考试化学试题福建省龙海市第二中学2019-2020学年高二下学期期末考试化学试题2008年理综全国卷Ⅰ高考试题化学试题(已下线)2012届广西桂林十八中高三第一次月考化学试卷(已下线)2011-2012学年山西大同实验中学高二下学期期中考试化学试卷(已下线)2011-2012学年福建省漳州立人学校高二下学期期中考试化学试卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2013届山西省山西大学附中高三9月月考化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2015-2016学年重庆市第八中学高二下第三次月考化学试卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年内蒙古元平煤高中高二实验班下期中化学卷2015-2016学年重庆四十二中高一下期中化学试卷(已下线)同步君 选修3 第二章 第三节 键的极性和分子的极性2016-2017学年宁夏育才中学孔德校区高二下学期第一次(3月)月考化学试卷2016-2017学年山东省淄博市高青一中、淄博实验中学高二下学期期中联考化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题陕西省黄陵中学2016-2017学年高二(重点班)下学期第三学月考化学试题河南省焦作市博爱一中2016-2017学年高二下学期第一次月考化学试题高中化学人教版 选修三 第2章 分子结构与性质 键的极性和分子的极性(已下线)【段考模拟】高二化学下学期第一次月考(3月)原创B卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题贵州省遵义市正安县第一中学2018-2019学年高二上学期期中考试化学试题云南省元江哈尼族彝族傣族自治县一中2018-2019学年高二上学期12月考试化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题(已下线)2019年6月12日 《每日一题》 选修3-物质类别、键的极性及分子的极性之间的关系安徽省淮北师范大学附属实验中学2018-2019学年高二下学期第二次月考化学试题吉林省长春市汽车经济开发区第三中学2018-2019学年高二下学期期中考试化学试题上海市青浦二中2016届高三上学期8月摸底考试化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题吉林省长春市第二十九中学2019-2020学年高二下学期线上检测化学试题河北省唐山市路北区第十一中学2019-2020学年高二期中考试化学试题辽宁省六校协作体2019-2020高二下学期期初考试化学试卷吉林省舒兰市实验中学2019-2020学年高二下学期期中考试化学试题福建省龙岩市武平县第一中学2021届高三上学期10月月考化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题四川省绵阳市江油中学2020-2021学年高二上学期期中考试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高二下学期期中考试化学试题广东省广州市第三中学2022-2023学年高二上学期期末测试化学试题(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 章末综合检测卷辽宁省阜新二高2020-2021学年高二下学期期中考试化学试题云南省通海县一中2020-2021学年高二下学期期中考试化学试题人教2019选择性必修2第二章 分子结构与性质复习与提高黑龙江省绥化市第九中学2021-2022学年高二4月月考化学试题新疆乌鲁木齐市第四中学2021-2022学年高二下学期期中考试化学试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题宁夏贺兰县景博中学2021-2022学年高二下学期第一次月考化学试题四川省绵阳市盐亭中学2022-2023学年高二上学期第一次月考教学质量检测化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测山东省威海市文登新一中2021-2022学年高二上学期期中考试化学试题广东省台山市第一中学2022-2023学年高二下学期第一次月考化学试题江西省景德镇市2022-2023学年高二下学期4月期中测试化学试题广东省深圳市观澜中学2022-2023学年高二下学期月考(物质结构)化学试题福建省德化第二中学2022-2023学年高二下学期期中考试化学试题安徽省合肥市第七中学2022-2023学年高二下学期期中检测化学试题广东省珠海市第三中学2023-2024学年高二下学期3月月考化学试卷河北省衡水市枣强中学2023-2024学年高二下学期第一次调研考试化学试题河南省焦作市2022-2023学年第四中学高二下学期期中考试 化学试卷广东省四会中学、广信中学2023-2024学年高二下学期第一次联合考试化学试题四川省富顺一中2023-2024学年高二下学期第一次月考化学试题广东省惠州市华罗庚中学2023-2024学年高二下学期3月月考化学试题广东梅州五华县中英文实验学校2023-2024学年高二下学期3月考试化学试题
名校
解题方法
4 . 某化合物的分子式为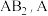 属
属 族元素,B属
族元素,B属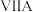 族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98,已知
族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98,已知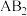 分子的键角为
分子的键角为 。下列推断不正确的是
。下列推断不正确的是
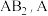 属
属 族元素,B属
族元素,B属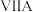 族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98,已知
族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98,已知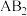 分子的键角为
分子的键角为 。下列推断不正确的是
。下列推断不正确的是A.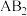 分子的空间构型为"V"形 分子的空间构型为"V"形 |
B.A-B键为极性共价键,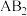 分子为非极性分子 分子为非极性分子 |
C.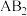 与 与 相比, 相比,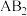 的熔点、沸点比 的熔点、沸点比 的低 的低 |
D.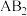 分子中无氢原子,分子间不能形成氢键,而 分子中无氢原子,分子间不能形成氢键,而 分子间能形成氢键 分子间能形成氢键 |
您最近一年使用:0次
2022-10-18更新
|
525次组卷
|
27卷引用:2015-2016学年湖北省天门、仙桃、潜江市高二下学期期末化学试卷
2015-2016学年湖北省天门、仙桃、潜江市高二下学期期末化学试卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省习水县一中2018-2019学年高二上学期12月份月考化学试题贵州省息烽县一中2018-2019学年高二11月份考试化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题河南省林州市第一中学2019-2020学年高二3月线上调研考试化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题河南省林州市第一中学2019-2020学年高二4月月考(实验班)化学试题山西省晋中市平遥中学2019-2020高二下学期在线学习质量检测化学试题辽宁省大连市大连海湾高级中学2019-2020学年高二下学期第一次质量检测化学试题(已下线)河北省石家庄市第二中学2016-2017学年高二下学期3月份月考化学试题吉林省吉化第一高级中学校2021-2022学年高二上学期期末考试化学试题天津市耀华中学2022-2023学年高二上学期期末考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 B素养拓展区(已下线)模块同步卷06 阶段性检测卷-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)黑龙江省大庆中学2020—2021学年高二下学期第一次月考化学试题山东省泰安市宁阳一中2020-2021学年高二下学期3月月考化学试题河北省石家庄市第二十三中学2021-2022学年高二下学期期中考试化学试题山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题第三节 分子结构与物质的性质 第2课时 分子间作用力 分子的手性四川省绵阳市盐亭中学2022-2023学年高二上学期第一次月考教学质量检测化学试题山东省乳山市银滩高级中学2022-2023学年高一下学期3月月考化学试题广东番禺中学2022-2023学年高二下学期科开学考试化学试题四川省广安市第二中学校2022-2023学年高二下学期期中考试化学试题河北省沧州市东光县等三县联考2022-2023学年高二下学期4月月考化学试题宁夏石嘴山市平罗中学2023-2024学年高二上学期第一次月考化学试题天津市朱唐庄中学2023-2024学年高二下学期3月检测化学试卷
名校
解题方法
5 . 下列说法正确的是
| A.Na+的电子排布式为1s22s22p63s1 |
| B.SO2分子的立体构型是V形 |
| C.HF的分子间作用力大于HCl,故HF比HCl更稳定 |
| D.有机物CH2=CH-CH3中杂化类型有sp3 和sp2,其中有一个π键,2个σ键 |
您最近一年使用:0次
2022-05-11更新
|
93次组卷
|
4卷引用:四川省遂宁市2019-2020学年高二上学期期末教学水平监测化学试题
6 . 下列分子或离子之间互为等电子体的是
| A.CS2和 NO2 | B.NH3和 NH | C.N2和 CO | D.CO2 和 SO2 |
您最近一年使用:0次
9-10高二下·福建漳州·期末
名校
解题方法
7 . 下列叙述正确的是
A. 是极性分子,分子中氮原子是在3个氢原子所构成的三角形的中心 是极性分子,分子中氮原子是在3个氢原子所构成的三角形的中心 |
B. 是非极性分子,分子中碳原子处在4个氯原子所构成的正方形的中心 是非极性分子,分子中碳原子处在4个氯原子所构成的正方形的中心 |
C. 是极性分子,分子中氧原子不处在2个氢原子所连成的直线的中间 是极性分子,分子中氧原子不处在2个氢原子所连成的直线的中间 |
D. 是非极性分子,分子中碳原子不处在2个氧原子所连成的直线的中间 是非极性分子,分子中碳原子不处在2个氧原子所连成的直线的中间 |
您最近一年使用:0次
2021-02-16更新
|
933次组卷
|
39卷引用:2010年福建省华安一中高二下学期期末考试化学试题
(已下线)2010年福建省华安一中高二下学期期末考试化学试题2014-2015黑龙江省哈尔滨六中高二上期末化学试卷甘肃省临泽一中2018-2019学年高二下学期期末模拟化学试题贵州省罗甸县第一中学2019-2020学年高二上学期期末考试化学试题(已下线)2011届上海市南汇中学高三上学期期中考试化学卷(已下线)2010-2011学年山西省吕梁市高二下学期期中考试化学试卷(已下线)2011-2012学年江苏省泰州中学高二上学期期中考试化学(选修)试卷(已下线)2011-2012学年甘肃省甘谷一中高二下学期期中考试化学试卷(已下线)2011-2012学年福建省四地六校高二下学期第三次月考化学试卷2014-2015学年辽宁实验分校高二下6月阶段测试化学试卷2015-2016学年湖北省黄石市有色一中高二下学期期中考试化学试卷河北省蠡县中学2016-2017学年高二6月月考化学试题2018版化学(苏教版)高考总复习专题十一课时跟踪训练--分子空间结构与物质性质河南省济源第一中学2017-2018学年高二下期6月月考化学试题(已下线)2018年11月30日 《每日一题》一轮复习-键的极性与分子的极性云南省彝良县民族中学2018-2019学年高二上学期12月份考试化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高二下学期第一次月考化学试题(已下线)2019年4月12日 《每日一题》选修3-分子的极性判断吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题【全国百强校】贵州省思南中学2018-2019学年高二下学期期中考试化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高二下学期期中考试化学试题【校级联考】福建省宁德市高中同心顺联盟校2018-2019学年高二下学期期中考试化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题河南省林州市第一中学2019-2020学年高二3月线上调研考试化学试题课时3 分子的空间构型与分子性质——A学习区 夯实基础(鲁科版选修3)宁夏回族自治区银川一中2019-2020学年高二下学期期中考试化学试题山西省太原市实验中学校2019-2020学年高二下学期期中考试化学试题河北省唐山市开滦第二中学2019-2020学年高二6月月考化学试题安徽省滁州市定远县炉桥中学2021-2022学年高二下学期期末考试化学试卷(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 第1课时 共价键的极性高二选择性必修2(人教版2019)第二章 分子结构与性质 第三节 分子结构与物质的性质 课时1 共价键的极性(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构 第2课时 分子的空间结构与分子性质山东省泰安市宁阳一中2020-2021学年高二下学期3月月考化学试题人教2019选择性必修2第二章第三节 分子结构与物质的性质课后习题(已下线)第31讲 分子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题2019鲁科版高中化学选择性必修2第2章第2节 共价键与分子的空间结构课后习题福建省宁德第一中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
8 . 锂离子电池已破广泛用作便携式电源。正极材料为LiCoO2、LiFePO4等,负极材料一般为石墨碳,以溶有LiPF6、LiBF4等的碳酸二乙酯无水溶液作电解液。回答下列问题:
(1)基态锂原子的电子排布图为________ 。基态磷原子子中,电子占据的最高能层符号为_____________ 。
(2)PO 的空间构型为
的空间构型为_______________ 。
(3)[Co(NH3)3Cl3]中Co3+的配位数为6,该配合物中的配位原子为____________ 。
(4)碳酸二乙酯的分子结构如图1所示,分子中所含元素的电负性由小到大的顺序为_____ ,分子中碳原子的杂化轨道类型为____ ,1 mol碳酸二乙酯中含有σ键的数目为_____ NA(NA为阿伏加德罗常数的值)。

(5)在元素周期表中,铁元素位于____ 区(填“s”“p”“d”或“ds”)。γ—Fe 的堆积方式如图2所示,其空间利用率为________ (用含π的式子表示)。
(6)氮化锂是一种新型无机贮氢材料,如图3所示,该晶体的化学式为____________ 。
(1)基态锂原子的电子排布图为
(2)PO
 的空间构型为
的空间构型为(3)[Co(NH3)3Cl3]中Co3+的配位数为6,该配合物中的配位原子为
(4)碳酸二乙酯的分子结构如图1所示,分子中所含元素的电负性由小到大的顺序为

(5)在元素周期表中,铁元素位于
(6)氮化锂是一种新型无机贮氢材料,如图3所示,该晶体的化学式为
您最近一年使用:0次
2020-12-31更新
|
231次组卷
|
3卷引用:安徽省皖南八校2021届高三第二次联考(12月)理综合化学试题
20-21高二·江苏南通·阶段练习
名校
解题方法
9 . 硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,回答下列问题:
(1)基态Ni2+的电子排布式为_______ 。
(2)①在1mol[Ni(NH3)6]2+中含有σ键的数目为_______ 。
②Ni、N、O三种元素的第一电离能由小到大的顺序是为_____ 。
③液氨中存在电离平衡2NH3⇌NH + NH
+ NH ,根据价层电子对互斥理论,可推知NH2—的空间构型为
,根据价层电子对互斥理论,可推知NH2—的空间构型为_______ ,液氨体系内,氮原子的杂化轨道类型为_____ 。NH3比PH3更容易液化的原因为_____ 。
(3)氧化镍晶胞如图所示,镍离子的配位数为_______ 。
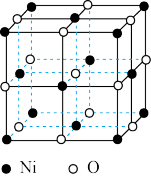
已知晶胞参数为a cm,NA为阿伏加德罗常数的值,则氧化镍晶体密度为______ g/cm3。
(1)基态Ni2+的电子排布式为
(2)①在1mol[Ni(NH3)6]2+中含有σ键的数目为
②Ni、N、O三种元素的第一电离能由小到大的顺序是为
③液氨中存在电离平衡2NH3⇌NH
 + NH
+ NH ,根据价层电子对互斥理论,可推知NH2—的空间构型为
,根据价层电子对互斥理论,可推知NH2—的空间构型为(3)氧化镍晶胞如图所示,镍离子的配位数为

已知晶胞参数为a cm,NA为阿伏加德罗常数的值,则氧化镍晶体密度为
您最近一年使用:0次
解题方法
10 . 下列判断正确的是( )
| A.BF3是三角锥形分子 |
| B.铵根离子呈平面形结构 |
| C.甲烷分子中的4个C-H键都是氢原子的1s轨道与碳原子的p轨道形成的s-pσ键 |
| D.甲烷分子中的4个C-H键都是氢原子的1s轨道与碳原子的4个sp3杂化轨道重叠形成的σ键 |
您最近一年使用:0次
2020-12-10更新
|
366次组卷
|
5卷引用:江苏省盐城市东台市创新学校2019-2020学年高二下学期5月份月检测化学试题
江苏省盐城市东台市创新学校2019-2020学年高二下学期5月份月检测化学试题辽宁省南台、岫二、牛庄、海城三中、腾鳌、析木等高级中学2020-2021学年高二上学期期末考试化学试题(已下线)第2章 微粒间相互作用与物质性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)专题4 综合检测(提升卷)福建省建瓯市芝华中学2021-2022学年高二下学期第一次阶段考化学试题



