17. 随着化石能源的减少,新能源的开发利用日益迫切。对化石能源燃烧产生的CO、CO
2的研究和深度的应用对构建生态文明社会也具有重要的意义。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
SO
2(g)+I
2(g)+2H
2O(g)=2HI(g)+H
2SO
4(l) Δ
H1=a kJ·mol
-12H
2SO
4(l)=2H
2O(g)+2SO
2(g)+O
2(g) Δ
H2=b kJ·mol
-12HI(g)=H
2(g)+I
2(g) Δ
H3=c kJ·mol
-1则:2H
2O(g)=2H
2(g)+O
2(g) Δ
H=
____ kJ·mol
-1。
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为2H
2(g)+SiCl
4(g)=Si(s)+4HCl(g) Δ
H=+240.4 kJ·mol
-1。若将生成的HCl通入100 mL1 mol·L
-1的NaOH溶液中恰好完全反应,则在此制备纯硅反应过程中的热效应是
____kJ。
(3)使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如下左图所示。这种传感器利用了原电池原理,则该电池的负极反应式为
______。
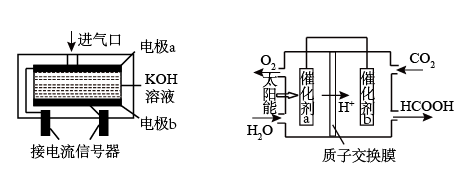
(4)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。右图是通过光电转化原理以廉价原料制备新产品的示意图。催化剂a、b之间连接导线上电子流动方向是
_______(填“a→b”或“b→a”)。
(5)人体血液里主要通过碳酸氢盐缓冲体系(
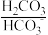
)维持pH稳定。已知正常人体血液在正常体温时,H
2CO
3的一级电离常数
Ka1=10
-6.1,
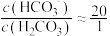
,1g2=0.3。由题给数据可算得正常人体血液的pH约为
______,当过量的酸进入血液中时,血液缓冲体系中
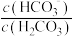
的值将
____(填“变大、变小、不变”)。