解题方法
1 . 下列离子的 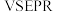 模型与其空间结构一致的是
模型与其空间结构一致的是
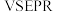 模型与其空间结构一致的是
模型与其空间结构一致的是A. | B. | C.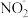 | D. |
您最近半年使用:0次
解题方法
2 . 液氨是一种很好的溶剂,液氨可以微弱的电离产生NH 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 、[Cu(NH3)4]2+的说法正确的是
、[Cu(NH3)4]2+的说法正确的是
 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 、[Cu(NH3)4]2+的说法正确的是
、[Cu(NH3)4]2+的说法正确的是A.NO 的空间构型为三角锥形 的空间构型为三角锥形 | B.NH3中N原子的杂化方式皆为sp2 |
C.NH3的键角比NH 中的大 中的大 | D.1 mol [Cu(NH3)4]2+中含有σ键的数目为12 mol |
您最近半年使用:0次
解题方法
3 . 按要求回答下列问题:
(1)前三周期元素中,基态原子核外有7组成对电子的原子,其价层电子的轨道表示式为___________ 。
(2)已知H2O2的沸点为152℃,H2S的沸点-60.4℃。请解释两者沸点差异的原因___________ 。
(3)BF3和NaBF4是硼的重要化合物,微粒中F-B-F键角:BF3___________  (填“>”、“<”或“=” )。理由是
(填“>”、“<”或“=” )。理由是___________ 。
(4)将CH3COOH、FCH2COOH、CH3CH2COOH的酸性由强到弱排序___________ ,并解释原因___________ 。
(1)前三周期元素中,基态原子核外有7组成对电子的原子,其价层电子的轨道表示式为
(2)已知H2O2的沸点为152℃,H2S的沸点-60.4℃。请解释两者沸点差异的原因
(3)BF3和NaBF4是硼的重要化合物,微粒中F-B-F键角:BF3
 (填“>”、“<”或“=” )。理由是
(填“>”、“<”或“=” )。理由是(4)将CH3COOH、FCH2COOH、CH3CH2COOH的酸性由强到弱排序
您最近半年使用:0次
名校
4 . 类推是化学学习和研究中常用的思维方法。下列类推正确的是
A. 为直线形分子,则 为直线形分子,则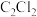 也为直线形分子 也为直线形分子 |
| B.N原子之间可以形成N=N,则P原子之间也可形成P=P |
C. 分子的空间结构为V形,则 分子的空间结构为V形,则 的VSEPR模型也是V形 的VSEPR模型也是V形 |
D.基态V的价层电子排布式为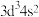 ,基态Cr的价层电子排布式为 ,基态Cr的价层电子排布式为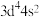 |
您最近半年使用:0次
2024-04-01更新
|
267次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
名校
解题方法
5 . 实验室中常用NaOH对NO、NO2的尾气进行吸收,反应方程式NO+NO2+2NaOH=2NaNO2+H2O,下列说法错误的是
| A.NaNO2中既有共价键也有离子键 |
B.氮原子的价层电子轨道表示式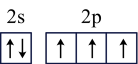 |
| C.水的VSEPR模型为四面体形 |
| D.NO、NO2均为酸性氧化物 |
您最近半年使用:0次
6 . 下列化学用语或表述正确的是
A. 的空间结构:V形 的空间结构:V形 |
B.KI的电子式: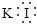 |
C.基态Ni原子价电子轨道表示式: |
D.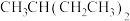 的名称:3-甲基戊烷 的名称:3-甲基戊烷 |
您最近半年使用:0次
名校
解题方法
7 . 价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 与 与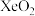 的键角相等 的键角相等 |
B. 和 和 均为非极性分子 均为非极性分子 |
C. 和 和 的空间构型均为平面三角形 的空间构型均为平面三角形 |
D. 和 和 的VSEPR模型均为四面体 的VSEPR模型均为四面体 |
您最近半年使用:0次
2024-03-13更新
|
460次组卷
|
4卷引用:湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷
解题方法
8 . 金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置________ ,Ti2+电子占据的最高能层的电子排布式为_________ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是___________ ,第一电离能介于Al、P之间的第三周期元素为___________ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为___________ ,B原子的杂化方式是___________ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有___________ (填序号)
①σ键②π键③氢键④配位键⑤离子键
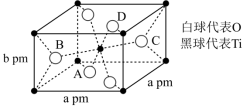
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近半年使用:0次
9 . 根据要求填空:
(1)红宝石是刚玉的一种,主要成分为氧化铝,因含微量杂质元素铬(Cr)而呈红色。基态铬原子的价层电子排布式为___________ 。
(2)铜催化烯烃确化反应时会产生 ,键角:
,键角:
___________ 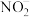 (填“<”或“=”或“>”)
(填“<”或“=”或“>”)
(3)①乙酸;②丙酸;③二氯乙酸的酸性由强到弱的顺序为___________ (填序号)。
(4)有机物吡啶(C5H5N),结构简式为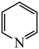 ,其中N的杂化方式为
,其中N的杂化方式为___________ ,吡啶在水中的溶解度远大于在苯中的溶解度,可能原因是:
①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②___________ 。
(1)红宝石是刚玉的一种,主要成分为氧化铝,因含微量杂质元素铬(Cr)而呈红色。基态铬原子的价层电子排布式为
(2)铜催化烯烃确化反应时会产生
 ,键角:
,键角:
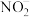 (填“<”或“=”或“>”)
(填“<”或“=”或“>”)(3)①乙酸;②丙酸;③二氯乙酸的酸性由强到弱的顺序为
(4)有机物吡啶(C5H5N),结构简式为
 ,其中N的杂化方式为
,其中N的杂化方式为①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②
您最近半年使用:0次
解题方法
10 . 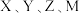 是原子半径依次减小的短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素的第一电离能比Z的第一电离能大,M的电负性比X的小。下列说法
是原子半径依次减小的短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素的第一电离能比Z的第一电离能大,M的电负性比X的小。下列说法不正确 的是
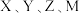 是原子半径依次减小的短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素的第一电离能比Z的第一电离能大,M的电负性比X的小。下列说法
是原子半径依次减小的短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素的第一电离能比Z的第一电离能大,M的电负性比X的小。下列说法A. 中所有原子共直线 中所有原子共直线 |
B.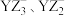 的 的 模型相同 模型相同 |
C. 的简单气态氢化物的沸点依次升高 的简单气态氢化物的沸点依次升高 |
D.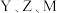 形成的化合物可以是酸、碱或盐 形成的化合物可以是酸、碱或盐 |
您最近半年使用:0次



