名校
1 . 回答下列问题:
(1)根据价层电子对互斥模型, 分子中心原子孤电子对数是
分子中心原子孤电子对数是_______ , 分子的空间构型是
分子的空间构型是_______ 。
(2)气态三氧化硫以单分子形式存在,属于_______ 分子(填“极性”、“非极性”),固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
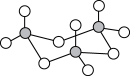
(3) 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,写出一个与 VEEPR模型相同的离子
VEEPR模型相同的离子_______ 。
(4)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:
B.两元素的电负性: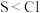
C.高价含氧酸的酸性: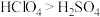
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应: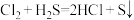
(1)根据价层电子对互斥模型,
 分子中心原子孤电子对数是
分子中心原子孤电子对数是 分子的空间构型是
分子的空间构型是(2)气态三氧化硫以单分子形式存在,属于

(3)
 中心原子的价层电子对数为
中心原子的价层电子对数为 VEEPR模型相同的离子
VEEPR模型相同的离子(4)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:

B.两元素的电负性:
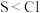
C.高价含氧酸的酸性:
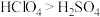
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:
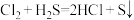
您最近一年使用:0次
解题方法
2 . W、X、Y、Z为原子序数依次增大的短周期主族元素,且原子核外L层的电子数分别为0、5、8、8,其最外层电子数之和为18。下列说法正确的是
| A.XW3分子的构型为平面三角形 |
| B.第一电离能:Y>X |
| C.化合物WZ难溶于水 |
| D.化合物YZ3分子中原子均满足8电子稳定结构 |
您最近一年使用:0次
3 . 用VSEPR 理论判断:
| 物质 | 孤对电子对数 | 轨道杂化形式 | 空间构型 |
| SO3 | |||
PO | |||
| NCl3 | |||
| CO2 |
您最近一年使用:0次
解题方法
4 . 下列分子价层电子对互斥理论模型与分子结构模型一致的是
| A.水 | B.甲烷 | C.氨 | D.二氧化硫 |
您最近一年使用:0次
名校
解题方法
5 . 下列描述中,正确的是
A. 是空间结构为V形的极性分子 是空间结构为V形的极性分子 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 中所有的原子不都在一个平面上 中所有的原子不都在一个平面上 |
D. 和 和 的中心原子的杂化轨道类型均为 的中心原子的杂化轨道类型均为 杂化 杂化 |
您最近一年使用:0次
2021-12-03更新
|
2223次组卷
|
15卷引用:海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题
海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题重庆市巫山县官渡中学2021-2022学年高二下学期期末考试化学试题重庆市万州纯阳中学校2021-2022学年高二下学期期中考试化学试题人教2019选择性必修2第二章 分子结构与性质复习与提高湖北省潜江市华中师范大学潜江附属中学高二上学期12月月考化学试题辽宁省大石桥市第三高级中学2021-2022学年高二12月月考化学试题吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题浙江省宁波市奉化区2022-2023学年高二上学期期末联考化学试题北京市顺义区第一中学2022-2023学年高二下学期3月月考化学试题广东省佛山市顺德区第一中学2022-2023学年高二下学期4月期中考试化学试题广东省云浮市罗定中学2022-2023学年高二下学期第2周周测(分子结构与性质)化学试题广东省深圳市盐田高级中学2023-2024学年高二上学期1月期末化学试题(已下线)热点04 分子的空间结构贵州省安龙县第一中学2023-2024学年高二下学期第一次阶段考试化学试题内蒙古赤峰新城红旗中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
6 . 下列描述中正确的是
| A.CS2分子的立体构型为V形 | B.ClO 的立体构型为平面三角形 的立体构型为平面三角形 |
| C.NH3、CO、CO2都是极性分子 | D.SiF4和SO 的中心原子均采取sp3杂化 的中心原子均采取sp3杂化 |
您最近一年使用:0次
2021-10-09更新
|
317次组卷
|
5卷引用:海南省儋州市鑫源中学2021-2022学年高二上学期期末考试化学试题
海南省儋州市鑫源中学2021-2022学年高二上学期期末考试化学试题(已下线)第2.2.2讲 杂化轨道理论-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)辽宁省清原满族自治县第二高级中学2020-2021学年高二下学期期中考试化学试题浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题新疆乌鲁木齐市第97中学(金英外国语学校)2023-2024学年高三上学期12月月考化学试题
名校
7 . 三价铬离子( )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:
(1)Cr的价层电子排布式为_______ 。
(2)O、N、S的原子半径由大到小的顺序为_______ 。
(3) 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为_______ ,其中心原子的杂化方式为_______ 。
(4)化学式为 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为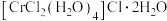 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为_______ ,配位数为_______ 。
(5) 分子可以与
分子可以与 结合生成
结合生成 ,这个过程发生改变的是
,这个过程发生改变的是_______ (填序号)。
a.微粒的空间结构 b.N原子的杂化类型 c.H-N-H键角 d.微粒的电子数
 )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:(1)Cr的价层电子排布式为
(2)O、N、S的原子半径由大到小的顺序为
(3)
 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为(4)化学式为
 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为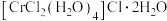 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为(5)
 分子可以与
分子可以与 结合生成
结合生成 ,这个过程发生改变的是
,这个过程发生改变的是a.微粒的空间结构 b.N原子的杂化类型 c.H-N-H键角 d.微粒的电子数
您最近一年使用:0次
2021-06-19更新
|
194次组卷
|
2卷引用:海南省东方市东方中学2021-2022学年高二下学期期中考试化学试题
名校
8 . 水是动物生命活动的必需物质,请判断水分子的VSEPR模型名称和中心原子O采取的杂化方式分别是
A.四面体形、 | B.V形、 | C.平面三角形、 | D.三角锥形、 |
您最近一年使用:0次
2021-04-09更新
|
230次组卷
|
6卷引用:海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题
海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题(已下线)第2.2.2讲 杂化轨道理论-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)专题4 分子空间结构与物质性质 第一单元 分子的空间结构 第1课时 分子的空间结构模型四川省成都外国语学校2020-2021学年高二4月月考化学试题吉林省白城市第一中学2020-2021学年高二下学期期中考试化学试题4.1.1杂化轨道理论 课后
名校
解题方法
9 . 下列说法中正确的是
A. 和 和 都是正四面体型分子,且键角相等 都是正四面体型分子,且键角相等 |
B.乙烯分子中,碳原子的 杂化轨道形成 杂化轨道形成 键,未杂化的 键,未杂化的 轨道形成 轨道形成 键 键 |
C. 成为阳离子时首先失去 成为阳离子时首先失去 轨道电子 轨道电子 |
D. 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱 |
您最近一年使用:0次
2021-03-12更新
|
1021次组卷
|
11卷引用:海南省琼海市嘉积中学2022-2023学年高二上学期第二次月考(期中)化学试题
海南省琼海市嘉积中学2022-2023学年高二上学期第二次月考(期中)化学试题浙江省“南太湖”联盟2021-2022学年高二下学期第一次联考化学试题 安徽省合肥市肥东县综合高中2021-2022学年高二下学期期中考试化学试题四川省雅安中学2022-2023学年高二上学期10月月考化学试题四川省成都市阳安中学2020-2021学年高二下学期3月月考化学试题安徽省宿州市十三所重点中学2020-2021学年高二下学期期中质量检测化学试题山东省临沂市第一中学2020-2021学年高二下学期6月月考化学试题广东省佛山市顺德市李兆基中学2022-2023学年高二下学期3月月考化学试题山东省济宁市2021届高三3月模拟(一模)化学试题(已下线)押山东卷第04题 物质结构与性质选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)专题13 物质结构与性质基础-备战2022年高考化学真题及地市好题专项集训【山东专用】
名校
解题方法
10 . 下列分子或离子中,VSEPR模型名称与分子或离子的立体构型名称不一致的是
| A.CO2 | B.H2O | C. | D.CCl4 |
您最近一年使用:0次
2020-09-07更新
|
797次组卷
|
32卷引用:海南省东方中学2021-2022学年高二下学期第一次月考化学试题
海南省东方中学2021-2022学年高二下学期第一次月考化学试题四川省西昌市2020-2021学年高二下学期期中检测化学试题新疆莎车县第一中学2021-2022学年高二下学期期中考试化学试题天津市宁河区芦台第一中学2021-2022学年高二下学期线上第一次月考化学试题贵州省凯里学院附属中学2021-2022学年高二下学期3月月考化学试题新疆疏勒县实验学校2021-2022学年高二下学期期中考试化学试题广东省湛江市第二中学2021-2022学年高二下学期第14周(5.21)周练化学试题2015-2016学年山西省大同一中高二下3月月考化学试卷2014-2015学年陕西西北大学附中高二下期末化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷2015-2016学年辽宁省葫芦岛市六校协作体联考高二下期中化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测陕西省黄陵中学2017-2018学年高二(重点班)下学期期末考试化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高二上学期期末考试化学试题【全国百强校】福建省厦门第一中学2018-2019学年高二上学期期中考试化学试题湖北省沙市中学2019-2020学年高二上学期期末考试化学试题内蒙古包头市包钢第四中学2018-2019学年高二下学期4月月考化学试题辽宁省凌源市第二高级中学2019-2020学年高二下学期第二次网测化学试题宁夏银川市长庆高级中学2019-2020学年高二下学期期中考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省福州第一中学2019-2020学年高二下学期期末考试化学试题新疆昌吉回族自治州呼图壁县第一中学2019-2020学年高二下学期期末考试化学试题(已下线)练习14 分子的空间结构-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)模块同步卷12 综合检测卷(提升卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)福建省建瓯市芝华中学2020-2021学年高二下学期第一阶段考试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题山东省临沂市平邑县第一中学西校区2023-2024学年高二下学期四月份阶段性考试化学试题【全国百强校】福建省三明市第一中学2019届高三第二次返校考试化学试题山东省泰安市2020届高三第二次模拟考试化学试题



