1 . 铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,与FeS2可联合制备铁粉精(FexOy)和H2SO4。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为_________ 。
(2)比较 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:_________ 。
(3) 与
与 和
和 之间的作用力分别为
之间的作用力分别为_________ 。
ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。
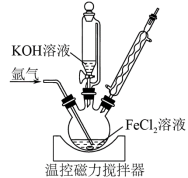
①三颈烧瓶发生反应的离子方程式为_________ 。
②检验反应是否进行完全的操作是_________ 。
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是_________ 。
②计算实验所得产品的产率_________ 。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为
(2)比较
 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:(3)
 与
与 和
和 之间的作用力分别为
之间的作用力分别为ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。

①三颈烧瓶发生反应的离子方程式为
②检验反应是否进行完全的操作是
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是
②计算实验所得产品的产率
您最近一年使用:0次
名校
解题方法
2 . 某小组同学用图装置 略去加热仪器等
略去加热仪器等 制备
制备 。
。
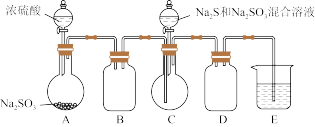
已知烧瓶 中发生反应如下:
中发生反应如下:
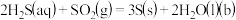

下列说法正确的是
 略去加热仪器等
略去加热仪器等 制备
制备 。
。
已知烧瓶
 中发生反应如下:
中发生反应如下:
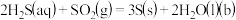

下列说法正确的是
A. 的稳定性比 的稳定性比 强 强 | B. 为 为 形分子 形分子 |
C. 与 与 的反应体现 的反应体现 的还原性 的还原性 | D. 、 、 的中心原子的轨道杂化类型为 的中心原子的轨道杂化类型为 |
您最近一年使用:0次
2022-09-10更新
|
169次组卷
|
3卷引用:江苏省南通市八校2022-2023学年高三上学期期初联考化学试题
3 .  是一种重要的工业原料,常用作媒染剂等。已知
是一种重要的工业原料,常用作媒染剂等。已知 常温下是无色液体,在潮湿空气中易水解,熔点
常温下是无色液体,在潮湿空气中易水解,熔点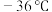 ,沸点
,沸点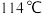 。工业上制备
。工业上制备 的工艺流程如图:
的工艺流程如图:
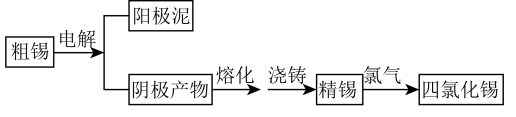
请回答下列问题;
(1)粗锡电解精炼时,常用硅氟酸 和硅氟酸亚锡
和硅氟酸亚锡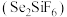 为电解液。已知
为电解液。已知 为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为
为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为___________ 。阴极的电极反应式为___________ ,根据价层电子对互斥理论和杂化轨道理论,判断 离子的空间构型是
离子的空间构型是___________ ,硅的杂化类型是___________ 。
(2)某同学模拟工业制法设计了由 与
与 反应制取
反应制取 的实验装置:
的实验装置:
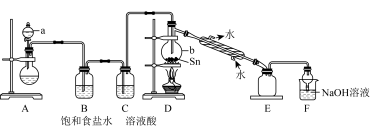
①a中浓盐酸与烧瓶内固体反应生成 ,则烧瓶内固体可以选用
,则烧瓶内固体可以选用___________ ,仪器b的名称为___________ 。
②装置D的主要缺点是___________ ,除此之外,整套装置还有的缺点是___________ 。
③制取 中可能会产生少量
中可能会产生少量 ,为测定产品中
,为测定产品中 的含量,可选用重铬酸钾标准液滴定,准确称取该样品
的含量,可选用重铬酸钾标准液滴定,准确称取该样品 放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成
放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成 溶液,取
溶液,取 于锥形瓶中,用
于锥形瓶中,用 重铬酸钾标准溶液滴定至终点,消耗标准液
重铬酸钾标准溶液滴定至终点,消耗标准液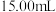 ,则产品中
,则产品中 的含量为
的含量为___________  (用含m的代数式表示),测定
(用含m的代数式表示),测定 含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是
含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是___________ (用离子方程式表示)。
 是一种重要的工业原料,常用作媒染剂等。已知
是一种重要的工业原料,常用作媒染剂等。已知 常温下是无色液体,在潮湿空气中易水解,熔点
常温下是无色液体,在潮湿空气中易水解,熔点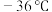 ,沸点
,沸点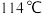 。工业上制备
。工业上制备 的工艺流程如图:
的工艺流程如图:
请回答下列问题;
(1)粗锡电解精炼时,常用硅氟酸
 和硅氟酸亚锡
和硅氟酸亚锡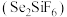 为电解液。已知
为电解液。已知 为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为
为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为 离子的空间构型是
离子的空间构型是(2)某同学模拟工业制法设计了由
 与
与 反应制取
反应制取 的实验装置:
的实验装置:
①a中浓盐酸与烧瓶内固体反应生成
 ,则烧瓶内固体可以选用
,则烧瓶内固体可以选用②装置D的主要缺点是
③制取
 中可能会产生少量
中可能会产生少量 ,为测定产品中
,为测定产品中 的含量,可选用重铬酸钾标准液滴定,准确称取该样品
的含量,可选用重铬酸钾标准液滴定,准确称取该样品 放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成
放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成 溶液,取
溶液,取 于锥形瓶中,用
于锥形瓶中,用 重铬酸钾标准溶液滴定至终点,消耗标准液
重铬酸钾标准溶液滴定至终点,消耗标准液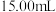 ,则产品中
,则产品中 的含量为
的含量为 (用含m的代数式表示),测定
(用含m的代数式表示),测定 含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是
含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是
您最近一年使用:0次
4 . 合成氨对人类生存具有重大意义,反应为: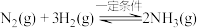
(1) 的空间结构是
的空间结构是_______ 。
(2)传统合成氨工艺是将 和
和 在高温、高压条件下发生反应。若向容积为1.0L的反应容器中投入
在高温、高压条件下发生反应。若向容积为1.0L的反应容器中投入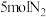 、
、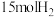 ,在不同温度下分别达平衡时,混合气中
,在不同温度下分别达平衡时,混合气中 的质量分数随压强变化的曲线如图所示。
的质量分数随压强变化的曲线如图所示。
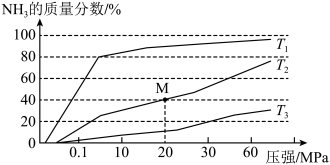
①温度 、
、 、
、 大小关系是
大小关系是_______ 。
②M点的平衡常数K=_______ (可用分数表示)。
(3)目前科学家利用生物燃料电池原理,研究室温下合成氨并取得初步成果,如图所示:

已知:a处通入 ,b处通入
,b处通入 。
。
①该装置中的能量转化形式是:_______ 能转化为_______ 能。
②导线中电子移动方向是_______ (填“a→b”或“b→a”)。
③相比传统工业合成氨,该方法的优点有_______ (任写一点)。
(4)实验室中制备氨气的方式有很多,例如加热浓氨水、加热某些铵盐固体等。
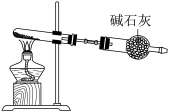
已知: 是强氧化性酸,以下哪个铵盐可置于如图装置试管中,通过加热分解制备少量氨气_______。
是强氧化性酸,以下哪个铵盐可置于如图装置试管中,通过加热分解制备少量氨气_______。
(5)温度为 时,将
时,将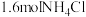 固体置于10L恒容密闭容器中,发生反应:
固体置于10L恒容密闭容器中,发生反应: ,一段时间后达到平衡。反应过程中测定的数据如表:
,一段时间后达到平衡。反应过程中测定的数据如表:
①4~7min,HCl的平均反应速率为_______ 。
②其它条件不变,9min后,向容器中加入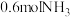 和0.6molHCl,再达平衡时,
和0.6molHCl,再达平衡时,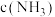
_______ (填“增大”、“减小”或“不变”)。
③下列描述中,可以表明该反应达到化学平衡状态的是_______ 。
A.容器中固体质量不变
B.容器中 的含量不变
的含量不变
C.容器中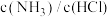 的比值不变
的比值不变
D.容器中气体压强不变
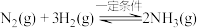
(1)
 的空间结构是
的空间结构是(2)传统合成氨工艺是将
 和
和 在高温、高压条件下发生反应。若向容积为1.0L的反应容器中投入
在高温、高压条件下发生反应。若向容积为1.0L的反应容器中投入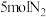 、
、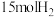 ,在不同温度下分别达平衡时,混合气中
,在不同温度下分别达平衡时,混合气中 的质量分数随压强变化的曲线如图所示。
的质量分数随压强变化的曲线如图所示。
①温度
 、
、 、
、 大小关系是
大小关系是②M点的平衡常数K=
(3)目前科学家利用生物燃料电池原理,研究室温下合成氨并取得初步成果,如图所示:

已知:a处通入
 ,b处通入
,b处通入 。
。①该装置中的能量转化形式是:
②导线中电子移动方向是
③相比传统工业合成氨,该方法的优点有
(4)实验室中制备氨气的方式有很多,例如加热浓氨水、加热某些铵盐固体等。
已知:
 是强氧化性酸,以下哪个铵盐可置于如图装置试管中,通过加热分解制备少量氨气_______。
是强氧化性酸,以下哪个铵盐可置于如图装置试管中,通过加热分解制备少量氨气_______。
A. | B. | C. | D. |
 时,将
时,将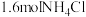 固体置于10L恒容密闭容器中,发生反应:
固体置于10L恒容密闭容器中,发生反应: ,一段时间后达到平衡。反应过程中测定的数据如表:
,一段时间后达到平衡。反应过程中测定的数据如表:| t/min | 2 | 4 | 7 | 9 |
 | 0.4 | 0.5 | 0.6 | 0.6 |
②其它条件不变,9min后,向容器中加入
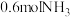 和0.6molHCl,再达平衡时,
和0.6molHCl,再达平衡时,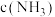
③下列描述中,可以表明该反应达到化学平衡状态的是
A.容器中固体质量不变
B.容器中
 的含量不变
的含量不变C.容器中
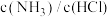 的比值不变
的比值不变 D.容器中气体压强不变
您最近一年使用:0次



