1 . 下列实验方案设计、现象和结论都正确的是
选项 | 实验目的 | 实验方案设计 | 现象和结论 |
A | 验证 与 与 在配合物中存在相互竞争 在配合物中存在相互竞争 | 向 溶液中加入少量 溶液中加入少量 固体 固体 | 溶液由蓝色变为黄绿色,说明发生了 到[ 到[ 的转化 的转化 |
B | 探究不同价态硫元素的转化 | 向 和 和 的混合溶液中加入浓硫酸 的混合溶液中加入浓硫酸 | 溶液变浑浊,证明 和 和 发生了氧化还原反应 发生了氧化还原反应 |
C | 实验室中制取并检验乙烯 | 取 乙醇,加入 乙醇,加入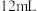 浓硫酸及少量沸石,逐渐升温至 浓硫酸及少量沸石,逐渐升温至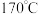 ,将产生的气体依次通过品红和溴水 ,将产生的气体依次通过品红和溴水 | 溴水褪色,说明产物中有乙烯生成 |
D | 检验苯酚中是否混有少量苯甲酸 | 向混合液中加入饱和 溶液 溶液 | 无气泡产生,证明不含苯甲酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
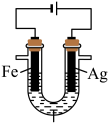
2 . 某兴趣小组探究电镀银实验。回答下列问题:
I.实验准备。
(1)用 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是___________ (填字母)。___________ 。
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与 浓度有关。
浓度有关。
【查阅资料】
络合反应: ,
, 。
。
【设计实验】
【问题讨论】
(3)实验a中,溶液变红色的可能原因是 和
和___________ (用离子方程式表示,已知氧化性: )。
)。
(4)①实验a、b的阴极都伴随有气泡,其原因是___________ (写电极反应式)。
②实验b比实验a产生的镀层光亮、致密,其原理是___________ 。
③一段时间后,实验b中 平衡不移动,其原因是
平衡不移动,其原因是___________ 。
【实验结论】
其他条件不变, 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。
Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与
 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。
表2:其他条件不变,温度对镀层外观的影响。
(5)表1中 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是___________ ;
表2中温度为 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是___________ 。
Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。
(6)使用新配方可以达到同样的目的,其原理是___________ 。已知: 。
。
I.实验准备。
(1)用
 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是A. B.
B. C.
C. D.
D. E.
E.
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与
 浓度有关。
浓度有关。【查阅资料】
络合反应:
 ,
, 。
。【设计实验】
| 实验 | 装置 | 现象 |
| a |
 的 的 溶液(含少量 溶液(含少量 ) ) | 阴极表面有疏松的黑色物质生成并伴随有无色气泡,一段时间后,取阴极区电解质溶液于试管,滴加 溶液,溶液变为红色。 溶液,溶液变为红色。 |
| b |
 的 的 与过量 与过量 混合(含少量 混合(含少量 ) ) | 阴极表面有光亮、致密的银白色物质生成,仍然有少量无色气泡。一段时间后,取少量阴极区溶液于试管,滴加 溶液,溶液不变红。 溶液,溶液不变红。 |
(3)实验a中,溶液变红色的可能原因是
 和
和 )。
)。(4)①实验a、b的阴极都伴随有气泡,其原因是
②实验b比实验a产生的镀层光亮、致密,其原理是
③一段时间后,实验b中
 平衡不移动,其原因是
平衡不移动,其原因是【实验结论】
其他条件不变,
 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与

 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。 含量( 含量( ) ) | 镀层外观表象 |
| 10 | 镀层模糊,无光泽 |
| 25 | 镀层呈雾状,光泽不足 |
| 50 | 镀层光亮、致密 |
温度/ | 镀层外观表象 |
| 25 | 光亮 |
| 35 | 光亮 |
| 40 | 光亮 |
| 55 | 光亮不均匀 |
(5)表1中
 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是表2中温度为
 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由
 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。(6)使用新配方可以达到同样的目的,其原理是
 。
。
您最近一年使用:0次
2024-04-16更新
|
318次组卷
|
5卷引用:2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学
2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学2024届河南省TOP二十名校联考高三下学期5月猜题(一)理科综合试卷-高中化学(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届青海省玉树州高三下学期第四次联考理综试题-高中化学
3 . 某中学同学在做铜与浓硫酸(装置如图)的反应实验时,发现有如下的反应现象:加热初期,铜丝表面变黑;继续加热,有大量气泡产生,品红溶液褪色,溶液变为墨绿色浊液,试管底部开始有灰白色沉淀生成;再加热,试管中出现“白雾”,浊液逐渐变为澄清,溶液颜色慢慢变为浅蓝色,试管底部灰白色沉淀增多;冷却,静置,将试管中液体倒入另一支盛水试管中,管壁发汤,溶液略带蓝色,将灰白色固体倒入水中,形成蓝色溶液。

(1)资料:聚四氯乙烯受热分解产生氯化氢,[CuCl4]2-呈黄色,[Cu(H2O)4]2+呈蓝色,两者混合则成绿色,铜的化合物中CuO、CuS、Cu2S都为黑色,其中CuO溶于盐酸;CuS、Cu2S不溶于稀盐酸,但溶于浓盐酸。该反应中,品红溶液褪色,体现SO2的______ 性,NaOH溶液的作用是______ 。
该中学同学分成几个小组分别对上述现象探究:
(2)甲组同学查相关文献资料获知:在较低温度(100℃)下,浓硫酸氧化性相对较弱,生成的黑色沉淀为Cu2S,溶液变蓝,但没有气泡产生。请根据文献资料写出反应的化学方程式:______ 。
(3)乙组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
请解释形成墨绿色的原因:______ 。
(4)丙组同学对白雾的成分经检验为H2SO4,请设计实验证明该白雾为硫酸:______ 。溶液的蓝色变浅,灰白色沉淀增多,这现象体现浓硫酸的______ 性。
(5)丁组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:
滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有______ 。
滴加适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,溶液呈略黄色[CuCln]2-n(n=1~4)。写出CuS与浓盐酸反应的离子方程式:______ 。
最后,丁组同学经过实验论证证明黑色沉淀中除了有CuS、Cu2S,还有S等。

(1)资料:聚四氯乙烯受热分解产生氯化氢,[CuCl4]2-呈黄色,[Cu(H2O)4]2+呈蓝色,两者混合则成绿色,铜的化合物中CuO、CuS、Cu2S都为黑色,其中CuO溶于盐酸;CuS、Cu2S不溶于稀盐酸,但溶于浓盐酸。该反应中,品红溶液褪色,体现SO2的
该中学同学分成几个小组分别对上述现象探究:
(2)甲组同学查相关文献资料获知:在较低温度(100℃)下,浓硫酸氧化性相对较弱,生成的黑色沉淀为Cu2S,溶液变蓝,但没有气泡产生。请根据文献资料写出反应的化学方程式:
(3)乙组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
| 现象 | ||
| I组 | 取灼烧后的铜丝 | 溶液变蓝 |
| Ⅱ组 | 直接取其铜丝(表面有聚四氯乙烯薄膜) | 溶液变成墨绿色 |
(4)丙组同学对白雾的成分经检验为H2SO4,请设计实验证明该白雾为硫酸:
(5)丁组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:
滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有
滴加适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,溶液呈略黄色[CuCln]2-n(n=1~4)。写出CuS与浓盐酸反应的离子方程式:
最后,丁组同学经过实验论证证明黑色沉淀中除了有CuS、Cu2S,还有S等。
您最近一年使用:0次
4 . 配合物的制备和应用
【活动探究】结合课本完成探究实验,完成下表
【活动探究】结合课本完成探究实验,完成下表
| 实验任务 | 实验过程与现象 | 结论 |
| 1.探究氯化铜固体在溶解并稀释过程中所发生的变化 | ———— | |
| 2.分别以氯化铁和硝酸铁为原料,探究Fe3+溶液显色的原因 | ||
| 3.制备[Ag(NH3)2]+并用于与葡萄糖反应得到银镜 | ||
| 4.对比Cu2+与氨水和OH-反应的差异 |
您最近一年使用:0次
名校
5 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象与结论 | |
| A | 验证压强对化学平衡的影响 | 先将注射器充满NO2气体,然后将活塞往里推压缩体积 | 观察到注射器内气体颜色加深,证明加压平衡朝生成NO2气体的方向移动 |
| B | 铜的电解精炼 | 待精炼的铜和纯铜连接外加直流电源的阳极和阴极,用硫酸铜溶液作电解质电解 | 阳极上铜逐渐溶解,阴极上铜逐渐析出,硫酸铜溶液浓度保持不变 |
| C | 制备[Cu(NH3)4]SO4·H2O晶体 | 向4mL 0.1mol/LCuSO4溶液中滴加氨水,先形成难溶物,并继续滴加沉淀溶解,然后蒸发溶剂析出晶体 | 反应过程中,NH3的N给出孤对电子,Cu2+接受电子对,形成了稳定的配位键[Cu(NH3)4]2+ |
| D | 除去锅炉水垢中的CaSO4 | 先用碳酸钠溶液浸泡水垢,然后再用盐酸除去 | 利用Ksp(CaSO4)> Ksp(CaCO3),实现沉淀的转化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-21更新
|
406次组卷
|
4卷引用:3.4 配合物与超分子-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)
(已下线)3.4 配合物与超分子-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)浙江省富阳区第二中学2021-2022学年高二下学期(3月)检测化学试题 河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题浙江省温州市2021-2022学年高二上学期期末教学质量统一检测化学试题
名校
解题方法
6 . 在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105
Co3++6NH3 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035
iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
(1)探究 的还原性
的还原性
实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。
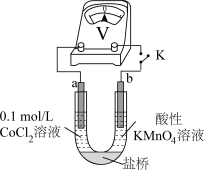
①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,____ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
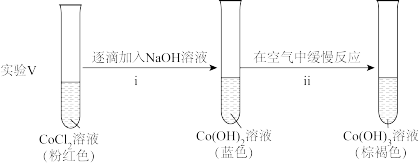
ii中反应的化学方程式是____ 。
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但____ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,____ (补全实验操作及现象),反应的离子方程式是____ 。
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是____ 。
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:____ 。
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:____ 。
示例:Co CoCl2
CoCl2 Co(OH)2
Co(OH)2
 和
和 之间的相互转化。
之间的相互转化。资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3
 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105Co3++6NH3
 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH

(1)探究
 的还原性
的还原性实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,
②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。
ii中反应的化学方程式是
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但
(2)探究
 的氧化性
的氧化性①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:
示例:Co
 CoCl2
CoCl2 Co(OH)2
Co(OH)2
您最近一年使用:0次
2022-05-08更新
|
1342次组卷
|
9卷引用:北京市西城区2022届高三第二次模拟测试化学试题
名校
解题方法
7 . 甘氨酸亚铁晶体是一种新型的固体整合补铁剂。其实验室合成路线为:
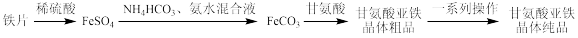
已知:
①相关物质的信息如下表所示
②含有多个配位原子的配体与同一中心离子通过整合配位成环而形成的配合物称为整合物。
(一)FeCO3固体的制备
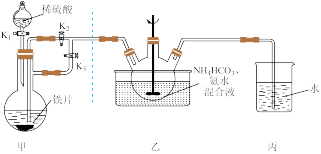
(1)实验开始时应先开K1和___________ ,关___________ (填“K2”或“K3”);一段时间后,改变开关状态,生成FeCO3。
(2)三颈瓶中生成FeCO3沉淀的离子方程式为___________ 。
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是___________ 。
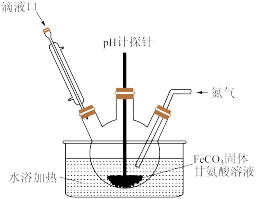
(4)当FeCO3固体完全溶解后,再通过滴液口加入乙醇,其作用是___________ 。
(5)反应结束后,过滤出产品粗品,依次用___________ 、___________ (填序号)洗涤,再经过一系列操作得纯品。
a. 热水 b. 冰水 c. 乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800 g于锥形瓶中,加3mol/LH2SO4溶液15 mL将样品溶解完全后,加入指示剂,立即用0.1000 mol/L(NH4)2Ce(SO4)3标准液滴定至终点,用去标准液20.20 mL(反应为Ce4++Fe2+=Ce3++Fe3+)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20 mL。
回答下列问题:
(6)滴定时应选择___________ 滴定管。
(7)甘氨酸亚铁晶体中Fe的质量分数为___________ %(保留小数点后一位)。
(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有H2NCH2COO-和Fe2+;Fe2+的配位数为6,且存在五元螯合环;该配合物整体量中心对称,甘氨酸亚铁晶体的结构简式为___________ 。
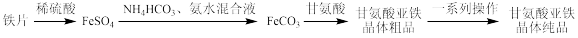
已知:
①相关物质的信息如下表所示
| 物质 | 化学式 | 摩尔质量 | 性质 |
| 甘氨酸 | H2NCH2COOH | 75g/mol | 两性物质,易溶于水,微溶于乙醇 |
| 甘氨酸亚铁晶体 | 易溶于水,溶解度随温度升高而增大;难溶于乙醇,在潮湿的空气中易被氧化 |
(一)FeCO3固体的制备

(1)实验开始时应先开K1和
(2)三颈瓶中生成FeCO3沉淀的离子方程式为
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是

(4)当FeCO3固体完全溶解后,再通过滴液口加入乙醇,其作用是
(5)反应结束后,过滤出产品粗品,依次用
a. 热水 b. 冰水 c. 乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800 g于锥形瓶中,加3mol/LH2SO4溶液15 mL将样品溶解完全后,加入指示剂,立即用0.1000 mol/L(NH4)2Ce(SO4)3标准液滴定至终点,用去标准液20.20 mL(反应为Ce4++Fe2+=Ce3++Fe3+)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20 mL。
回答下列问题:
(6)滴定时应选择
(7)甘氨酸亚铁晶体中Fe的质量分数为
(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有H2NCH2COO-和Fe2+;Fe2+的配位数为6,且存在五元螯合环;该配合物整体量中心对称,甘氨酸亚铁晶体的结构简式为
您最近一年使用:0次