1 . NA表示阿伏加德罗常数的值,配合物Na2[Fe(CN)5(NO)]可用于离子检验。下列说法不正确的是
| A.该配合物中存在离子键、配位键、极性键、非极性键 |
| B.配离子为[Fe(CN)5(NO)]2-,中心离子为Fe3+,配位数为6,配位原子为C和N |
| C.1mol该配合物中σ键数目为6NA |
| D.该配合物为离子化合物,易电离,1mol配合物电离共得到3NA个阴、阳离子 |
您最近一年使用:0次
2 . 已知:铜离子的配位数通常为4, 和
和 均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是
均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是
 和
和 均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是
均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是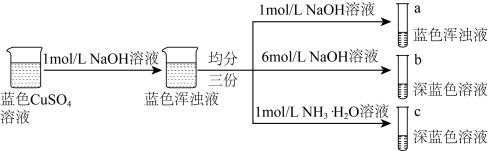
A.b、c溶液中 相同 相同 |
B.b中得到配合物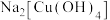 ,其配体为 ,其配体为 |
C.由实验可知, 的配位能力比 的配位能力比 弱 弱 |
D.a、b、c三种溶液中加入 溶液均会产生白色沉淀 溶液均会产生白色沉淀 |
您最近一年使用:0次
解题方法
3 . 从硝酸铜和硝酸银的混合溶液中回收铜和银的流程如图所示。

| A.试剂Ⅰ可以是稀盐酸或稀硫酸 |
| B.流程中涉及的反应均是氧化还原反应 |
C.生成银氨溶液的离子方程式为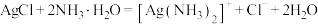 |
D.若试剂Ⅱ是甲醛, 甲醛参加反应最多生成 甲醛参加反应最多生成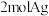 |
您最近一年使用:0次
4 . MnCl2可与NH3反应生成[Mn(NH3)6]Cl2,Mn2+与NH3之间的化学键为什么键
| A.π键 | B.σ键 | C.配位键 | D.离子键 |
您最近一年使用:0次
名校
5 . 下列说法错误的是
| A.硫酸铜的水溶液为蓝色,则无水硫酸铜也为蓝色 |
| B.向硫酸四氨合铜溶液中加入乙醇会析出深蓝色晶体,因为乙醇的极性比水小 |
| C.利用硫氰化铁配离子的颜色,可鉴定溶液中存在铁离子 |
| D.氯化银溶于氨水,是因为反应生成可溶于水的氯化四氨合银 |
您最近一年使用:0次
名校
6 . 钴酞菁(Pc-Co,已知酞菁分子中所有原子共平面)和金属分子笼1通过“一锅法”合成了超分子复合物Pc-Co@1,以Pc-Co@1为催化剂将CO2转化为CO的反应机理如图所示。

| A.酞菁中a、b、c三处氮原子的杂化类型相同 |
B.上述过程总反应式为 |
| C.反应过程中有s-sp3σ键形成 |
| D.钴酞菁分子中两个氮原子提供孤对电子,与Co2+形成配位键 |
您最近一年使用:0次
2024-03-21更新
|
372次组卷
|
2卷引用:河南重点高中2023-2024学年高三下学期阶段性测试(七)理综试题-高中化学
解题方法
7 . 在周期表中钌与铁同列,钌的配位催化有广阔的前景,钌催化反应实例如下图所示:

下列叙述不正确的是

下列叙述不正确的是
A.Ru-1、Ru-2、Ru-3、Ru-4中Ru的化合价分别为 、 、 、 、 、 、 |
B.Ru-1、Ru-2、Ru-3、Ru-4中都含有大 键 键 |
C. 中的 中的 形成3个配位键 形成3个配位键 |
D.该反应的总反应为 |
您最近一年使用:0次
名校
解题方法
8 . 用下列实验方案或装置进行实验,不能达到相应实验目的的是
| 选项 | A | B | C | D |
| 实验方案或装置 |  | 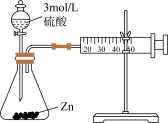 | 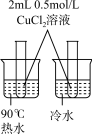 | 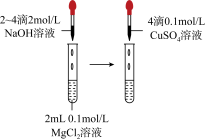 |
| 实验目的 | 中和热的测定 | 测定锌与稀硫酸反应的化学反应速率 | 探究温度对化学平衡的影响 | 比较Mg(OH)2与Cu(OH)2的Ksp大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 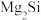 具有反萤石结构,晶胞结构如图所示,其晶胞参数为0.635nm。下列叙述正确的是
具有反萤石结构,晶胞结构如图所示,其晶胞参数为0.635nm。下列叙述正确的是

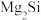 具有反萤石结构,晶胞结构如图所示,其晶胞参数为0.635nm。下列叙述正确的是
具有反萤石结构,晶胞结构如图所示,其晶胞参数为0.635nm。下列叙述正确的是
| A.Si的配位数为4 |
B.紧邻的两个Mg原子的距离为 |
C.紧邻的两个Si原子间的距离为 |
D.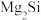 的密度计算式为 的密度计算式为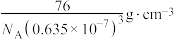 |
您最近一年使用:0次
2023-10-04更新
|
176次组卷
|
2卷引用:河北省石家庄实验中学2022-2023学年高二上学期期末考试化学试题
解题方法
10 . 向硫酸铜溶液里逐滴加入氨水的过程如下图所示。下列说法错误的是


A. 和 和 与 与 的配位能力: 的配位能力: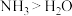 |
B.过程②反应的离子方程式为 |
C.析出的深蓝色晶体是 |
| D.加乙醇的作用是减小溶剂的极性,降低溶质的溶解度 |
您最近一年使用:0次



