解题方法
1 . 硅材料在生活中占有重要地位。
(1)太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为___________ 。单晶硅的晶体类型为___________ 。
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(2)由硅原子核形成的三种微粒,电子排布式分别为:① 、②
、②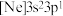 、③
、③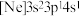 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(3)硅和卤素单质反应可以得到 ,
, 的熔沸点如下表:
的熔沸点如下表:
①气态 分子的空间构型是
分子的空间构型是___________ 。
A.正四面体形 B.三角锥形 C.角形 D.直线形
②0℃时, 、
、 、
、 、
、 呈液态的是
呈液态的是___________ 。
A. B.
B. C.
C. D.
D.
③比较上述 的熔沸点,分析其变化规律及原因
的熔沸点,分析其变化规律及原因___________ 。
(4) 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如下图所示:
,其结构如下图所示:___________ 。
(5)硅合金具有良好的性能。
①下列关于合金的说法错误的是___________ 。
A.熔点高于组成金属 B.可能含有非金属
C.硬度通常比组成金属大 D.一般比单一金属用途更广
②白铜是我国使用最早的合金之一,白铜晶胞结构如图所示(Cu位于面心),该晶胞含有的Cu原子和Ni原子个数分别为___________ 、___________ 。已知晶体密度为dg·cm-3,设NA为阿伏加德罗常数的值。Ni和Ni之间的最短距离为___________ nm。
(1)太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(2)由硅原子核形成的三种微粒,电子排布式分别为:①
 、②
、②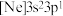 、③
、③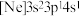 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.得电子能力:①>② |
| B.微粒半径:③>①>② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.电子排布属于基态原子(或离子)的是:①② |
 ,
, 的熔沸点如下表:
的熔沸点如下表: |  |  |  | |
| 熔点/℃ | -90.0 | -69.8 | 5.6 | 120.7 |
| 沸点/℃ | -85.8 | 57.8 | 154.2 | 287.7 |
 分子的空间构型是
分子的空间构型是A.正四面体形 B.三角锥形 C.角形 D.直线形
②0℃时,
 、
、 、
、 、
、 呈液态的是
呈液态的是A.
 B.
B. C.
C. D.
D.
③比较上述
 的熔沸点,分析其变化规律及原因
的熔沸点,分析其变化规律及原因(4)
 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如下图所示:
,其结构如下图所示:
(5)硅合金具有良好的性能。
①下列关于合金的说法错误的是
A.熔点高于组成金属 B.可能含有非金属
C.硬度通常比组成金属大 D.一般比单一金属用途更广
②白铜是我国使用最早的合金之一,白铜晶胞结构如图所示(Cu位于面心),该晶胞含有的Cu原子和Ni原子个数分别为

您最近一年使用:0次



