解题方法
1 . 硅材料在生活中占有重要地位。
(1)太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为___________ 。单晶硅的晶体类型为___________ 。
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(2)由硅原子核形成的三种微粒,电子排布式分别为:① 、②
、②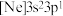 、③
、③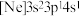 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(3)硅和卤素单质反应可以得到 ,
, 的熔沸点如下表:
的熔沸点如下表:
①气态 分子的空间构型是
分子的空间构型是___________ 。
A.正四面体形 B.三角锥形 C.角形 D.直线形
②0℃时, 、
、 、
、 、
、 呈液态的是
呈液态的是___________ 。
A. B.
B. C.
C. D.
D.
③比较上述 的熔沸点,分析其变化规律及原因
的熔沸点,分析其变化规律及原因___________ 。
(4) 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如下图所示:
,其结构如下图所示:___________ 。
(5)硅合金具有良好的性能。
①下列关于合金的说法错误的是___________ 。
A.熔点高于组成金属 B.可能含有非金属
C.硬度通常比组成金属大 D.一般比单一金属用途更广
②白铜是我国使用最早的合金之一,白铜晶胞结构如图所示(Cu位于面心),该晶胞含有的Cu原子和Ni原子个数分别为___________ 、___________ 。已知晶体密度为dg·cm-3,设NA为阿伏加德罗常数的值。Ni和Ni之间的最短距离为___________ nm。
(1)太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(2)由硅原子核形成的三种微粒,电子排布式分别为:①
 、②
、②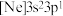 、③
、③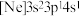 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.得电子能力:①>② |
| B.微粒半径:③>①>② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.电子排布属于基态原子(或离子)的是:①② |
 ,
, 的熔沸点如下表:
的熔沸点如下表: |  |  |  | |
| 熔点/℃ | -90.0 | -69.8 | 5.6 | 120.7 |
| 沸点/℃ | -85.8 | 57.8 | 154.2 | 287.7 |
 分子的空间构型是
分子的空间构型是A.正四面体形 B.三角锥形 C.角形 D.直线形
②0℃时,
 、
、 、
、 、
、 呈液态的是
呈液态的是A.
 B.
B. C.
C. D.
D.
③比较上述
 的熔沸点,分析其变化规律及原因
的熔沸点,分析其变化规律及原因(4)
 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如下图所示:
,其结构如下图所示:
(5)硅合金具有良好的性能。
①下列关于合金的说法错误的是
A.熔点高于组成金属 B.可能含有非金属
C.硬度通常比组成金属大 D.一般比单一金属用途更广
②白铜是我国使用最早的合金之一,白铜晶胞结构如图所示(Cu位于面心),该晶胞含有的Cu原子和Ni原子个数分别为

您最近一年使用:0次
2 . 铜及其化合物在生产和生活中有着广泛的应用。
(1)Cu在元素周期表中的位置为______ 。
(2)基态铜原子有______ 种运动状态不同的电子。
(3)原子核外电子的两种自旋状态分别用+ 和-
和- 表示,称为电子的自旋磁量子数,基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,基态铜原子自旋磁量子数的代数和为______ 。
(4)Cu+比Cu2+更稳定的原因是_______ 。
Cu2+能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
(5)步骤I中反应的离子方程式为________ ;_______ 。
(6)H-N-H键角大小:[Cu(NH3)4]2+_______ NH3(填“>”、“=”或“<”),其原因是_______ 。
(7)该实验能说明,Cu2+与NH3的结合能力_______ (填“大于”“小于”或“等于”)Cu2+与OH-的结合能力。
(8)Cu2+能与乙二胺(H2NCH2CH2NH2)形成[Cu(H2NCH2CH2NH2)2]2+离子,结构如图,关于该配离子的说法正确的是______ 。
(1)Cu在元素周期表中的位置为
(2)基态铜原子有
(3)原子核外电子的两种自旋状态分别用+
 和-
和- 表示,称为电子的自旋磁量子数,基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,基态铜原子自旋磁量子数的代数和为(4)Cu+比Cu2+更稳定的原因是
Cu2+能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
| 序号 | 实验步骤 | 实验现象或结论 |
| I | 向CuSO4溶液中逐滴加入氨水至过量 | 产生蓝色沉淀,随后溶解并得到深蓝色的溶液 |
| Ⅱ | 再加入无水乙醇 | 得到深蓝色晶体 |
| Ⅲ | 测定深蓝色晶体的结构 | 晶体的化学式为[Cu(NH3)4]SO4 H2O H2O |
| Ⅳ | 将深蓝色晶体洗净后溶于水配成溶液,再加入稀NaOH溶液 | 无蓝色沉淀生成 |
(5)步骤I中反应的离子方程式为
(6)H-N-H键角大小:[Cu(NH3)4]2+
(7)该实验能说明,Cu2+与NH3的结合能力
(8)Cu2+能与乙二胺(H2NCH2CH2NH2)形成[Cu(H2NCH2CH2NH2)2]2+离子,结构如图,关于该配离子的说法正确的是
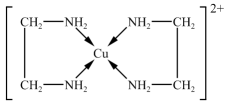
| A.该离子的配位数是4 |
| B.该离子的配体数是4 |
| C.形成配离子前后,Cu的化合价不变 |
| D.该离子中含有离子键、非极性键与极性键 |
您最近一年使用:0次
3 . 镍颜色近似银白色,我国古时使用 “白铜”(一种镍铜合金)制造兵器。现代工业镍及其化合物主要用于生产不锈钢、电池以及催化剂领域。
(1)基态镍原子的价电子排布式为___________ ,镍元素在周期表中的位置为___________ 。
(2)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示,该合金的化学式为___________。

(3)已知NiO、FeO的晶体结构类型均与氯化钠相同,Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO___________ FeO(选填“<””或“>”),理由是___________ 。
(4)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如图所示,下列关于该配合物结构分析正确的是__________。

(5)镍镉(Ni-Cd)可充电电池应用广泛。已知某镍镉电池的电解质溶液为KOH溶液,其充电和放电的反应原理为:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2,有关该电池的说法正确的是_______。
Cd(OH)2+2Ni(OH)2,有关该电池的说法正确的是_______。
(6)工业上通过调节pH除杂并回收废液中的镍,用于制备硫酸镍晶体。常温下,加碱调节pH在7.2~8.7,使Ni2+开始沉淀,至其浓度降为1.0×10−5 mol·L-1,可认为Ni2+已经完全沉淀,则Ni(OH)2的Ksp=___________ 。
(7)硫酸镍溶液在强碱中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式___________ 。
(8)将分离出硫酸镍晶体后的母液收集、循环使用。其主要目的是___________ 。
(1)基态镍原子的价电子排布式为
(2)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示,该合金的化学式为___________。

| A.LaNi5 | B.LaNi6 | C.LaNi8 | D.LaNi9 |
(3)已知NiO、FeO的晶体结构类型均与氯化钠相同,Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO
(4)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如图所示,下列关于该配合物结构分析正确的是__________。

| A.配体的分子式为C8H14N4O4 |
| B.既有内界,又有外界 |
| C.配位数为4 |
| D.氧原子与氢原子之间形成的化学键有共价键和氢键 |
(5)镍镉(Ni-Cd)可充电电池应用广泛。已知某镍镉电池的电解质溶液为KOH溶液,其充电和放电的反应原理为:Cd+2NiOOH+2H2O
 Cd(OH)2+2Ni(OH)2,有关该电池的说法正确的是_______。
Cd(OH)2+2Ni(OH)2,有关该电池的说法正确的是_______。| A.充电时阳极反应:Ni(OH)2+OH——e—=NiOOH+H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时OH—向正极移动 |
(6)工业上通过调节pH除杂并回收废液中的镍,用于制备硫酸镍晶体。常温下,加碱调节pH在7.2~8.7,使Ni2+开始沉淀,至其浓度降为1.0×10−5 mol·L-1,可认为Ni2+已经完全沉淀,则Ni(OH)2的Ksp=
(7)硫酸镍溶液在强碱中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(8)将分离出硫酸镍晶体后的母液收集、循环使用。其主要目的是
您最近一年使用:0次
解题方法
4 . 我国科学家研发的水系可逆Zn-CO2电池可吸收利用CO2.将两组正离子、负离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的H2O解离成H+和OH—,工作原理如图所示:_____ 。
(2)充电时复合膜中向多孔Pd纳米片极移动的离子是_____ ,放电时正极的电极反应式为_____ 。
(3)下列说法中正确的是_____。
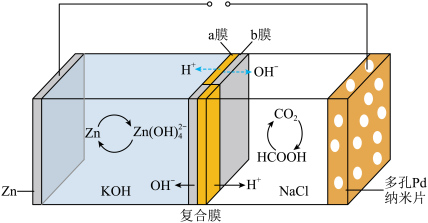
(2)充电时复合膜中向多孔Pd纳米片极移动的离子是
(3)下列说法中正确的是_____。
| A.放电时锌做阳极 |
| B.充电时多孔Pd纳米片极发生还原反应 |
| C.Na2[Zn(OH)4]中只存在离子键和配位键 |
D.Zn(OH) 可在足量稀硫酸中转化为Zn2+ 可在足量稀硫酸中转化为Zn2+ |
您最近一年使用:0次
名校
解题方法
5 . 卤素互化物、拟卤素与卤素单质的结构,性质相似。常见的卤素互化物有ICl、IBr等,拟卤素有(CN)2、(SCN)2等。
(1)卤族元素位于元素周期表的_______ 。
(2)79Br和81Br这两种核素的中子数之差的绝对值为_______ 。
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为_______ 。
(4)①已知CN-与N2结构相似,CN-的电子式为______ 。
②推算HCN分子中σ键与π键数目之比为_______ 。
③关于氨基氰(N≡C-NH2)分子的说法中正确的是_______ 。
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为______ 。
(6)K2[Zn(CN)4]中Au+的配位数为______ 。
(7)i中反应的离子方程式为:_______ 。
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______
(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因_______ 。
(1)卤族元素位于元素周期表的
| A.s区 | B.p区 | C.d区 | D.f区 |
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为
| A.①>②>③ | B.③>②>① | C.②>①>③ | D.③>①>② |
②推算HCN分子中σ键与π键数目之比为
③关于氨基氰(N≡C-NH2)分子的说法中正确的是
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为
(6)K2[Zn(CN)4]中Au+的配位数为
(7)i中反应的离子方程式为:
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因
您最近一年使用:0次
名校
解题方法
6 . 一种含Se的新型AIE分子(IV)的合成路线如图:_______ 。
(2)IV中具有孤电子对的原子有_______ 。
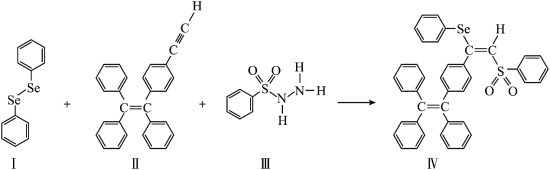
| A.I中仅有σ键 |
| B.I中的Se-Se为非极性共价键 |
| C.II易溶于水 |
| D.II中原子的杂化轨道类型只有sp、sp2、sp3 |
| A.C | B.O | C.S | D.Se |
您最近一年使用:0次
名校
解题方法
7 . ZnS硫化锌是一种重要的半导体材料,广泛应用于发光、传感、红外的窗口材料、光催化等诸多领域。ZnS不溶于水,它溶于硝酸溶液中发生反应:ZnS+HNO3→Zn(NO3)2+S↓+NO↑+H2O(未配平)。
(1)对反应中相关晶体中的作用力判断正确的是______ 。
(2)反应中涉及的非金属元素的微粒半径比较正确的是______ 。
(3)对该反应的说法正确的是______ 。
(4)配平该反应方程式并求示出电子转移的方向和数目。______
_______ZnS+_______HNO3——________Zn(NO3)2+________S↓+_______NO↑+_______H2O
(5)若在反应中ZnS______ (填“失去”或“得到”)0.6mol电子,则可生成_____ L气体(标准状况下测定)。
(6)Zn在周期表中的位置是______ ,S原子的电子排布式是______ 。
(7)已知ZnS有两种晶型,其中一种晶体的晶胞如图所示。1个晶胞中,Zn2+离子的数目为_______ 。已知该晶胞边长为anm,这种ZnS的密度是______ 。

(8)NO 的空间构型为
的空间构型为______ ,其中N原子的轨道杂化类型是______ 。
(9)Zn的氯化物与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有共价键的数目为______ 。
(1)对反应中相关晶体中的作用力判断正确的是
| A.HNO3晶体中含离子键 | B.Zn(NO3)2晶体中含共价键 |
| C.S晶体中只含共价键 | D.H2O晶体只含氢键 |
| A.S<O | B.O>N | C.S2->O2- | D.O2->N3- |
| A.氧化产物是S | B.还原产物是Zn(NO3)2和NO |
| C.氧化性:ZnS>S | D.还原性:HNO3>NO |
_______ZnS+_______HNO3——________Zn(NO3)2+________S↓+_______NO↑+_______H2O
(5)若在反应中ZnS
(6)Zn在周期表中的位置是
(7)已知ZnS有两种晶型,其中一种晶体的晶胞如图所示。1个晶胞中,Zn2+离子的数目为

(8)NO
 的空间构型为
的空间构型为(9)Zn的氯化物与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有共价键的数目为
您最近一年使用:0次
8 . 关于[Cr(H2O)4Br2]Br·2H2O的说法正确的是( )
| A.配体为水分子,配位原子是O,外界为Br- | B.中心原子的配位数为6 |
| C.中心原子Cr采取sp3杂化 | D.中心原子的化合价为+2价 |
您最近一年使用:0次
2017-05-11更新
|
267次组卷
|
4卷引用:沪科版化学拓展性课程2《化学键和晶体结构》测试题



